【Science】 挑战“厘米级”样本!革命性技术VIPS实现10天超清重构小鼠嗅球,数据量突破0.5PB!
[!INFO] ✨文章标题:Mesoscale volumetric fluorescence imaging at nanoscale resolution by photochemical sectioning ✉️作者: Srigokul Upadhyayula and Ruixuan Gao等 📚期刊:Science 🔗链接:https://doi.org/10.1126/science.adr9109
1. 从“痛点”到“突破”
在生物医学影像领域,科学家们长久以来都面临着一个几乎无法调和的矛盾:想看得越清,能看得越小。
我们追求“纳米级”的超高分辨率,去看清神经元的突触、髓鞘的精细结构 。但实现这一目标的高分辨率光学显微镜,其物镜的工作距离却极短 ,只能看清样本的表面。
想象一下,你拿着一个极其精密的放大镜,它能让你看清头发丝上的纹理,但这个放大镜却只能贴着物体表面,根本无法探入一个完整的、厚实的生物器官内部 。
为了解决这个问题,研究人员尝试了“机械切片”,就像切香肠一样,把大样本切成无数薄片 。但对于那些经过“水凝胶”处理而膨胀变大的生物样本(比如,膨胀后的脑组织),这种硬切的方式极其容易引入形变、撕裂和样本丢失 。尤其在进行神经回路追踪时,哪怕丢失一个切片,都可能导致整条回路的重建彻底失败 。
这就像想绘制一张完整的高精度地图,却不得不把地图撕碎成小块,还保证不了每一块都能完好无损地拼接回去。这些限制,让对整个哺乳动物大脑等完整样本进行连续、高保真的纳米级成像,成为了一个“不可能的任务” 。
现在,顶尖科研团队最新的研究中提出了一种颠覆性的解决方案:VIPS(Volumetric Imaging via Photochemical Sectioning,光化学切片式体积成像) 。这一技术巧妙地结合了光化学原理和光学成像,成功跨越了显微镜工作距离的物理限制 。
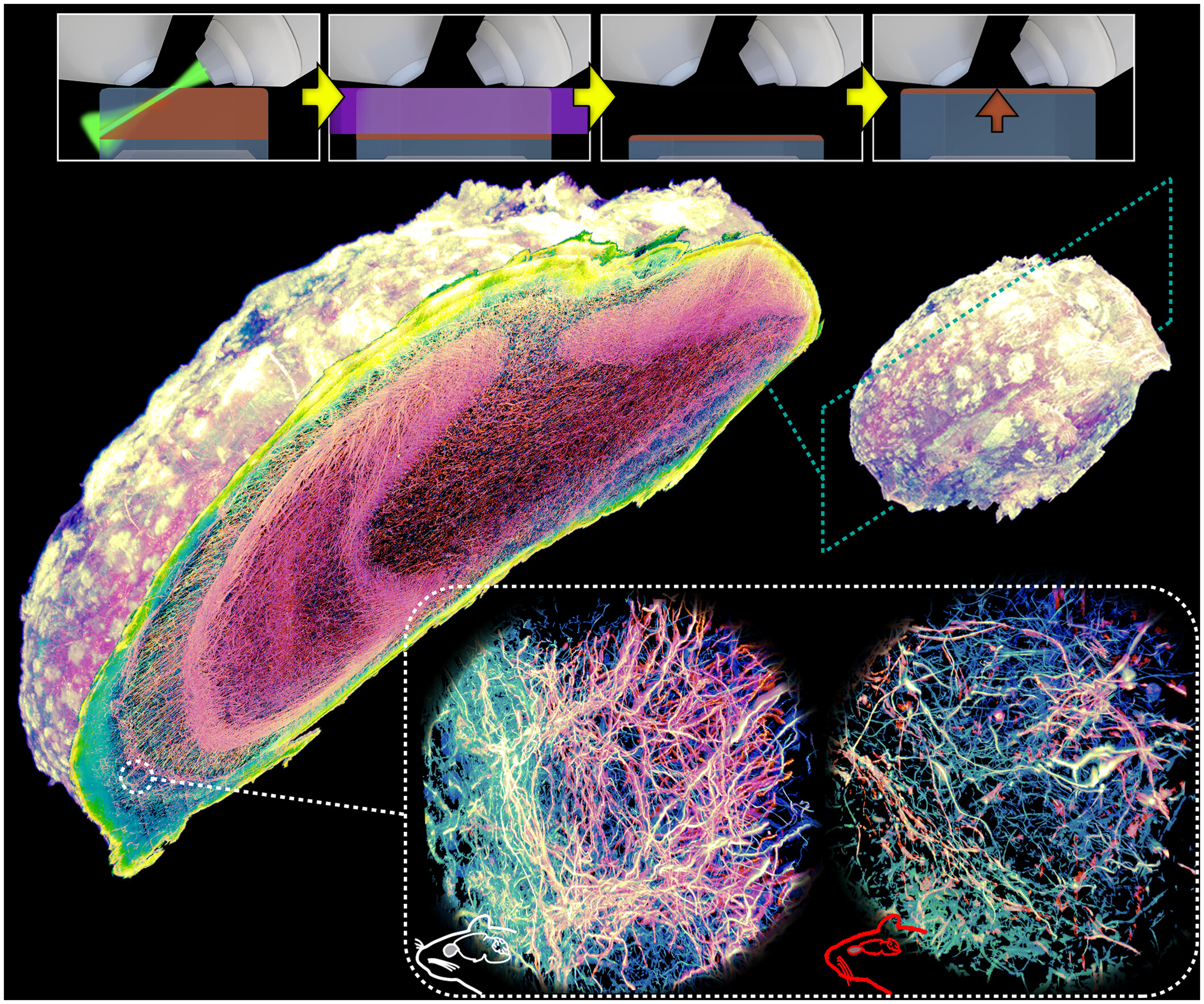
它不仅避开了机械切片带来的所有问题,更首次实现了对一个完整小鼠嗅球(Olfactory Bulb, OB)这种“厘米级”规模的样本进行纳米分辨率的体积成像和完整重构 。这个成就,不仅标志着成像技术的一次巨大飞跃,也为神经科学从“局部采样”迈向“整体定量”分析开辟了全新的道路 。
2. 核心方法与技术细节解密:VIPS的创新机制
VIPS这个名字听起来复杂,但其核心思想却非常精妙:用光来精准地、非接触地“溶解”样本,取代机械刀片。
要理解VIPS,我们首先要理解它的三个关键技术支柱:光可降解水凝胶、光化学切片(PS) 和片上成像(On-block imaging) 。
2.1 创新的“自毁”水凝胶
一切的根基,在于一种特殊的超吸水水凝胶(Superabsorbent Hydrogel)。
这种凝胶的配方很关键,它必须能在紫外线(UV)激发下迅速、彻底地分解 。科学家们为此开发了一种包含光可裂解交联剂(PC) 的聚丙烯酰胺-聚丙烯酸钠凝胶,我们称之为PC-gel 。
想象你建了一座由乐高积木组成的城堡(生物样本),这些积木被一层透明、有弹性的胶水(水凝胶)固定住 。普通的胶水(Bis-gel)一旦固化,就无法拆解 。而PC-gel这种特殊的“胶水”,它的交联点上带有一个“光开关” 。一旦被特定波长的紫外光(或者405nm的蓝光,甚至双光子激发)照射 ,这些光开关就会迅速断裂,导致整个水凝胶网络瞬间瓦解,就像城堡的“结构件”被精准地切断了 。
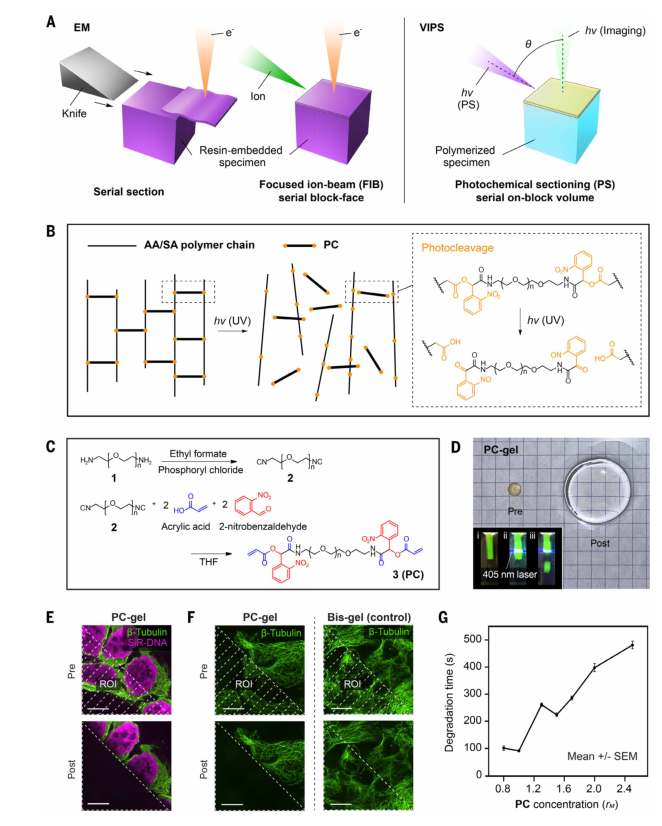
当凝胶瓦解后,包裹在其中的生物分子和荧光标记物就会扩散出去,样本在被照射的区域就“消失”了 。
2.2 “无影刀”:光化学切片(PS)
VIPS的第二步,就是利用这种“光可降解”的特性,实现非接触式、空间精确的切片,也就是光化学切片(PS) 。 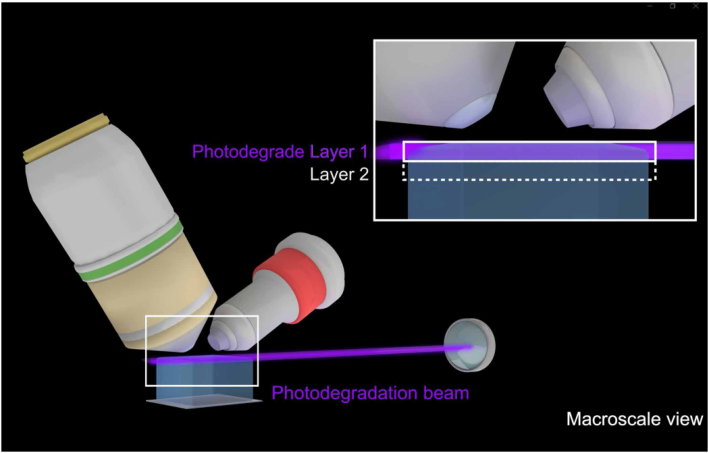
在传统的电子显微镜(EM)中,我们用机械刀片或离子束(FIB-SEM)来切除一层样本 。而在VIPS中,研究人员则使用一束光片(Light-Sheet)作为他们的“无影刀” 。
他们将样本浸泡在水凝胶中 ,使用一束精确聚焦的光片(例如405nm激光光片)从侧面照射样本的顶层 。这束光片只在它经过的平面上触发凝胶的分解 。在实验中,这束光在短短约20分钟内,就能完成对4到5倍膨胀样本的平面切除 。
这种光化学切片的最大优势在于其非接触性 。它不会像机械切片那样产生形变、撕裂或丢失 。而且,光片可以精确地控制“切除深度”,保证了每一层切片的平整度和一致性 。
2.3 “片上成像”与迭代循环
光片切除了一层后,露出的是一个全新的、平整的“块面” 。此时,高分辨率显微镜(VIPS通常采用格子光片显微镜, LLSM )登场,对这层新鲜暴露的表面进行“片上体积成像”(On-block volumetric imaging)。LLSM拥有高速度和低光漂白的特性,非常适合处理这种大样本、高分辨率的成像任务 。
然后,这个过程开始迭代 。
LLSM 成像到物镜的最大工作深度 。
光化学切片(PS)将这层已经成像的体积去除 。
露出下一层块面,再次进行LLSM 成像 。
如此循环往复,一层一层地深入,直到对整个样本完成成像 。通过这种“边切边看,看完就扔”的策略,VIPS完美绕开了高分辨率显微镜工作距离短的物理限制 。

它有效地将一个“无法窥探的深水巨型生物”,转化为了一个“可以无限连续剥洋葱的自动化过程” 。
3. 数据背后的创新与颠覆性分析:
VIPS的技术突破,最终体现在它所能处理的样本规模和数据产出上,展现出前所未有的深度和广度 。
3.1 跨越物理障碍的厘米级成像
VIPS最直接的成就,就是突破了物理尺寸的限制 。
在早期的实验中,研究人员就证明了VIPS结合双光子(2P)技术,能对一块小鼠脑组织实现约3.8毫米深度的连续成像 。要知道,这已经远远超出了他们所用物镜约2.6毫米的最大工作距离 。

当技术升级为更快速的LLSM和光片PS组合后,VIPS更是展现了惊人的可扩展性。他们成功完成了对一个完整的小鼠嗅球(OB)的纳米级成像 。这个嗅球经过2倍膨胀后,体积达到了约 。
在整个成像过程中,VIPS采用了9个回合的LLSM成像与光化学切片交替进行 。整个获取过程历时10天,产生了17,280个体素切片,原始数据量高达0.5P字节(Petabytes, PB) 。
这是一个了不起的成就,因为它证明了VIPS能够将纳米级分辨率的成像能力,从以往的“局部小片”提升到“器官整体”的宏大尺度 。
3.2 单轴突分辨率的定量分析
有了完整的、高精度的三维数据,科学家们就可以进行更深入、更可靠的定量分析,实现“前所未有”的生物学洞察 。
研究团队利用专为PB级数据设计的高性能计算流水线PetaKit5D和PetaVIPS ,成功地重构了小鼠嗅球中所有有髓鞘和无髓鞘的轴突 。最小直径约150纳米的单个轴突都可以被追踪和重构 ,这达到了单轴突分辨率的精细程度 。
更重要的是,VIPS使比较研究成为可能。研究人员对一个正常的野生型(WT)小鼠嗅球和一个神经退行性疾病模型(NPC1) 小鼠嗅球进行了完整成像和对比 。
分析结果显示了惊人的差异,特别是疾病发展模式:
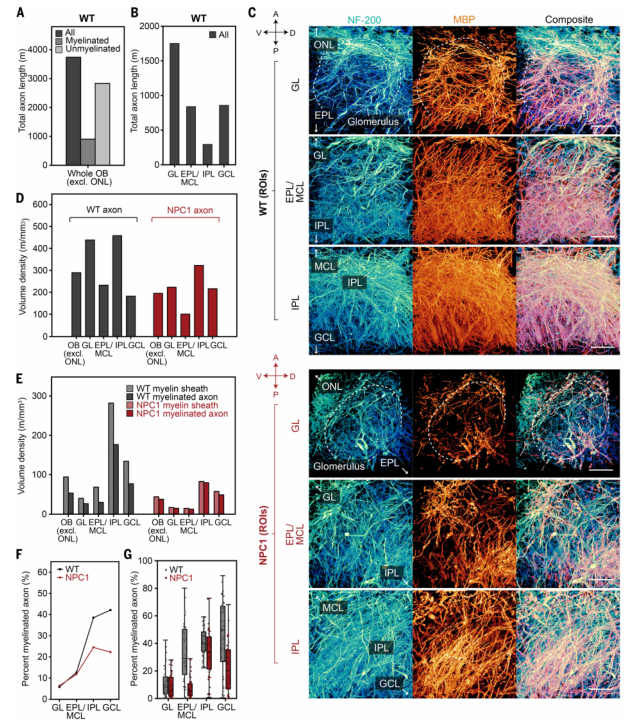
1. 轴突密度的异质性变化:
在NPC1小鼠嗅球中,轴突的体积密度在整体上是降低的 。
但是,不同解剖层表现出极大的异质性 。例如,外丛状层/僧帽细胞层(EPL/MCL) 的轴突密度下降最严重,降幅高达56.6% 。
令人意外的是,颗粒细胞层(GCL) 的轴突密度反而增加了18.6% 。这被认为是神经元大量损失后,GCL中可能发生的代偿性轴突发芽(Axonal Sprouting) 。这种局部细节的涨落,在传统的局部采样中是无法被捕获的 。
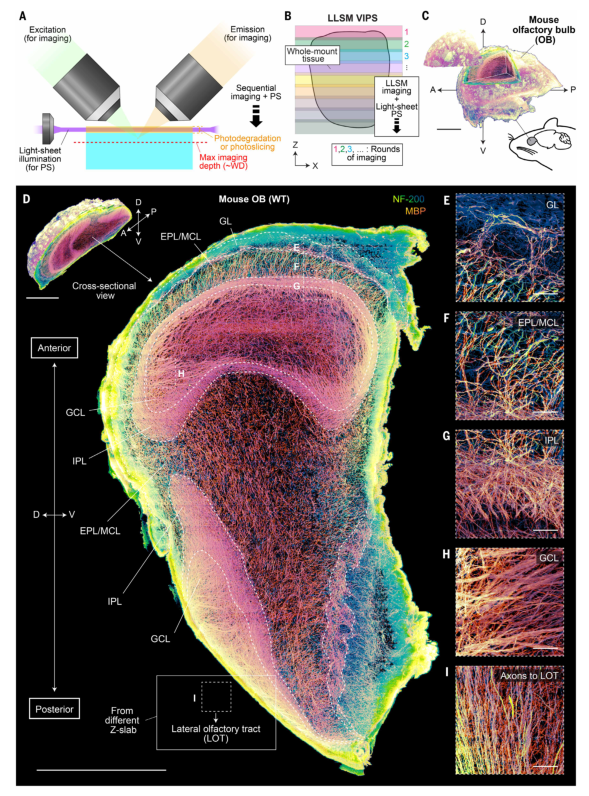
2. 髓鞘形成的差异性:
髓鞘的密度在NPC1嗅球中也整体下降 ,证实了早期的髓鞘形成障碍(Dysmyelination)持续存在 。
更有趣的是,有髓鞘轴突占总轴突的百分比在嗅球的深层(如内丛状层IPL和GCL)下降幅度最大,分别减少了36.2% 和46.9% 。这表明在这些深层,有髓鞘的轴突可能比无髓鞘的轴突遭受了更严重的损失 。
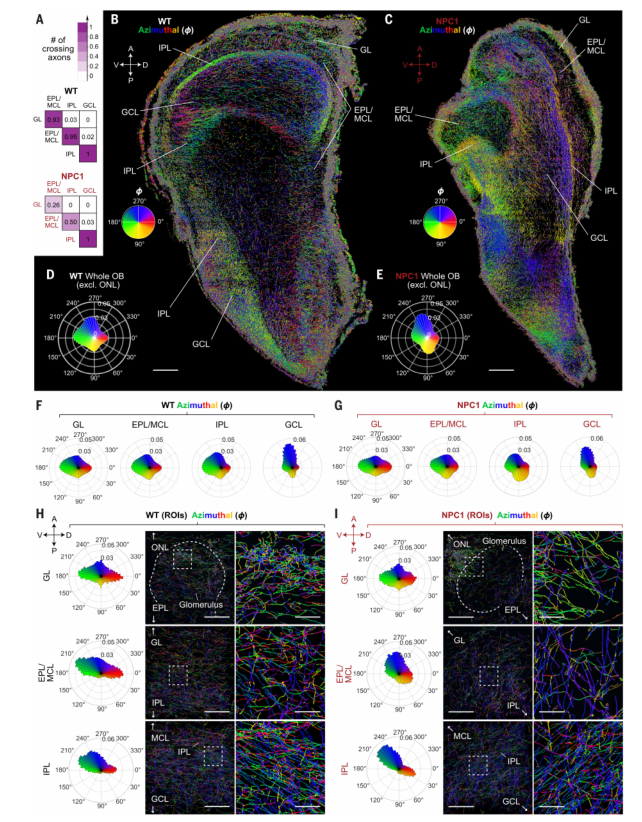
3. 退行性模式和方向选择性:
对轴突的走向和连接性(Tractography)分析揭示了神经退行的内向性模式 。在NPC1嗅球中,从内层(IPL-GCL)向外层(GL-EPL/MCL)穿越的轴突数量逐渐减少 ,暗示退行性变化始于嗅球的外层并向内推进 。
此外,疾病的退行性过程甚至对轴突的方向具有选择性 。在NPC1小鼠的IPL中,沿着腹侧-背侧轴投射的轴突表现出最显著的减少 。
这些惊人的定量结果,是VIPS提供的“全样本连续性”和“纳米级分辨率”缺一不可的产物 。它把生物学研究从**“猜测和稀疏采样”推向了“完整定量测量”**的新时代 。
4. 应用展望、局限性与未来路线图
VIPS技术的问世,无疑为神经科学和组织学研究带来了巨大的工具箱升级 。它能轻松整合到现有的显微镜平台中,实现连续、自动化的数据采集 。
4.1 潜在应用场景
这项技术的直接应用包括:
绘制全脑连接组: VIPS与LLSM结合,为光学方法绘制突触级别的完整哺乳动物大脑连接组(Connectomes)奠定了基础 。未来的目标是通过全膜或蛋白质标记,在纳米尺度上重构整个大脑的神经回路 。
疾病的整体研究: 通过对整个器官进行定量比较,科学家可以更准确地识别神经退行性疾病、发育异常或衰老等疾病在空间上和结构上的细微变化和模式 。
生物学的立体定向研究: VIPS能揭示以前无法检测到的解剖异质性、梯度和生物学模式 。
4.2 客观的局限性与挑战
任何前沿技术都有其局限性,VIPS也不例外 。研究人员坦诚地指出了当前面临的几个挑战:
荧光标记的深度和特异性: 即使在仅约2倍的膨胀倍率下,荧光标记的密度和特异性仍然存在限制 。例如,在对嗅球的轴突计数中,他们通过VIPS获得的无髓鞘轴突数量,仅为先前电镜研究(EM)结果的约14% 。在大样本中实现均匀、致密的标记仍然是一个核心难点 。
数据处理的巨大挑战: 单个样本的数据量轻松超过PB级 。这带来了数据存储、传输、计算和分析的巨大成本 。
非刚性配准的难题: 在子体积边界处观察到的非线性形变(Nonlinear Warping)问题 ,意味着需要开发出能够处理PB到EB(Exabytes)级别数据的、可扩展的非刚性图像配准算法 。
4.3 未来路线图:AI是PB级数据的钥匙
未来解决这些挑战的关键,在于人工智能(AI) 。
面对如此庞大的3D数据集,人类单独进行分析和手动注释是不现实的 。研究人员明确指出,AI系统将是替代手动注释、并从海量数据中提取定量洞察的关键 。
幸运的是,随着荧光标记化学、AI/GPU加速的非刚性求解器、分割技术以及计算成本的不断进步,这些差距正在被迅速缩小 。VIPS,与高性能计算和AI的结合,正在将我们带入一个 “全景式” 理解生物学的新纪元 。