【Anal. Chem.】新型近红外荧光探针,只加一个Biotin,大幅度增加癌细胞的靶向能力
近日,湖南大学的研究团队开发出一种名为QL-VB的新型近红外荧光探针,可以精准靶向癌细胞并实现成像。这一突破性进展为癌症的早期诊断和精准治疗提供了新的工具和方向。
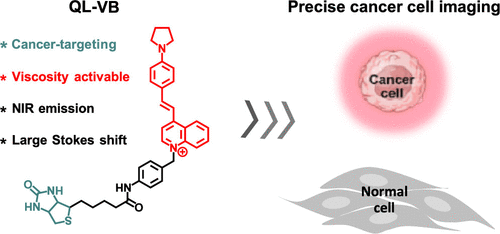
探针设计的巧妙之处
分子结构设计
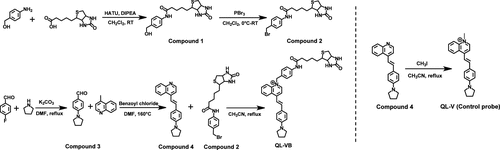
图1. QL-VB的合成路径
QL-VB探针的分子结构设计非常巧妙,主要由三个关键部分组成:
电子受体: 4-甲基喹啉季铵基团
- 这一基团不仅作为电子受体,还能帮助探针靶向线粒体
电子供体: 吡咯烷基团
- 具有强电子供给能力
靶向基团: 生物素
- 可以与癌细胞表面过表达的受体结合,实现靶向功能
电子受体和供体通过双键连接,形成分子转子结构。这种结构使得探针对环境粘度变化非常敏感。
工作原理
在低粘度环境中,分子可以自由旋转,荧光被猝灭。而在高粘度环境(如癌细胞线粒体)中,分子旋转受限,荧光显著增强。这种"开关"特性使得QL-VB可以在癌细胞中被特异性激活。
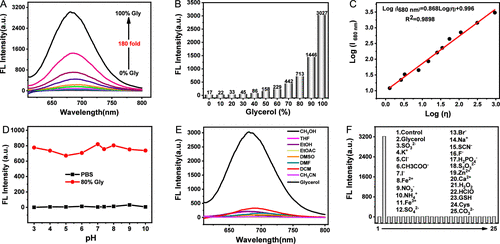 图2. QL-VB的成像原理
图2. QL-VB的成像原理
探针的优异性能
QL-VB探针展现出多项优异的光学和生物学特性:
- 高灵敏度: 对粘度变化极为敏感,可在0.89-998 cP范围内线性响应
- 近红外发射: 发射波长为680nm,有利于深层组织成像
- 大斯托克斯位移: 高达100nm,有效减少光谱重叠
- 优良的光化学性质:
- 光稳定性好,可长时间连续激发
- 不受pH值(3.0-9.0范围内)和极性影响
- 良好的生物相容性:
- 水溶性好,即使在100μM高浓度下仍能很好溶解
- 细胞毒性低,20μM浓度下细胞存活率仍达
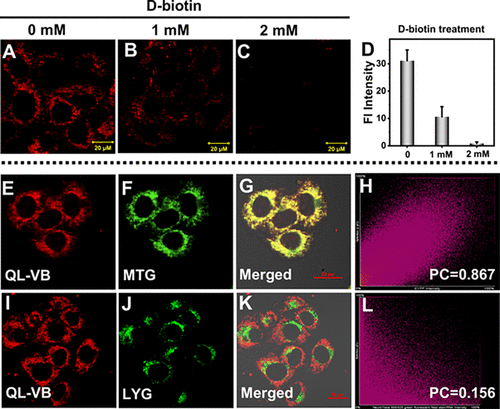 图3. QL-VB的性能测试
图3. QL-VB的性能测试
在细胞和活体中的应用
癌细胞与正常细胞的区分
研究人员在多种癌细胞和正常细胞中进行了对比实验: 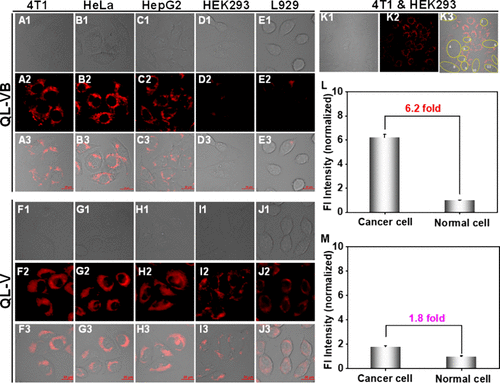
图4. QL-VB对不同细胞的成像
- 在HeLa、4T1和HepG2等癌细胞中,QL-VB呈现出强烈的荧光信号
- 而在HEK 293和L929等正常细胞中,几乎观察不到荧光
- QL-VB在癌细胞/正常细胞的信噪比高达6.2,远优于对照探针(1.8)
线粒体粘度变化的动态监测
QL-VB还能够监测癌细胞线粒体粘度的动态变化:
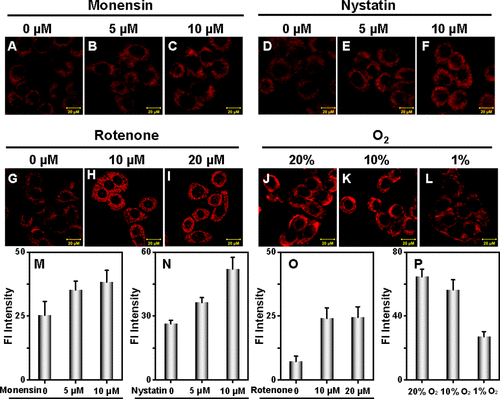 图5. QL-VB的粘度成像测试
图5. QL-VB的粘度成像测试
- 药物刺激: 用莫能菌素和制霉菌素处理后,荧光信号随药物浓度增加而增强
- 能量代谢抑制: 用鱼藤酮抑制呼吸链后,荧光信号显著增强
- 缺氧条件: 在低氧环境下,荧光信号随氧浓度降低而减弱
这些结果表明,QL-VB可用于研究线粒体功能和代谢异常。
活体肿瘤成像
在荷瘤小鼠模型中,QL-VB同样展现出优异的性能:
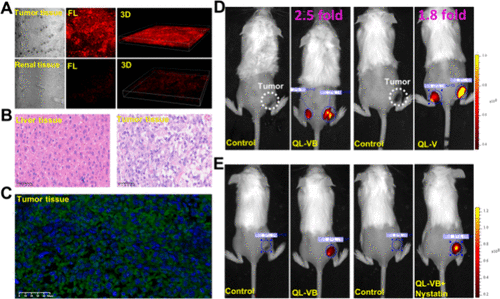 图6. QL-VB的肿瘤成像
图6. QL-VB的肿瘤成像
- 肿瘤组织中的荧光信号明显强于正常组织
- 肿瘤/正常组织的信噪比达到2.5,优于对照探针(1.8)
- 可快速检测肿瘤组织(30分钟内)
- 能够监测活体内肿瘤粘度的变化
研究意义与展望
这项研究的意义主要体现在以下几个方面:
- 为癌症早期诊断提供新工具: QL-VB探针可以在细胞和组织水平精确区分癌和正常样本
- 有助于癌症手术导航: 近红外发射特性使其有望用于术中实时成像
- 推动基础研究: 为研究癌细胞线粒体功能和代谢提供了新方法
- 药物开发潜力: 可用于筛选影响细胞粘度的潜在抗癌药物
参考文献
Qian, M.; Ye, Y.; Ren, T.-B.; Xiong, B.; Yuan, L.; Zhang, X.-B. Cancer-Targeting and Viscosity-Activatable Near-Infrared Fluorescent Probe for Precise Cancer Cell Imaging. Anal. Chem. 2024, acs.analchem.4c01551.