NSC通俗阅读,带你探索更多来自《自然》《科学》《细胞》等顶刊中的奇妙研究世界🧪🧠🌍
【Nature】饿到忘了疼?《自然》发现大脑“疼痛总开关”,揭示饥饿、恐惧如何成为天然镇痛剂
我们每天都可能会遇到各种疼痛,比如不小心切到手指的急性疼痛,或是运动后肌肉酸痛的炎症性疼痛,还有一些人长期忍受着慢性疼痛的折磨。有趣的是,我们有时会发现,在某些特殊情况下,疼痛感似乎会“消失”。比如,在饥肠辘辘时,好像就不那么在意身上的小伤小痛了。这背后究竟隐藏着怎样的科学奥秘呢?
最近发表在顶级期刊《自然》上的一项研究,为我们揭示了大脑中一个精密的“疼痛调控中心”,它解释了为什么饥饿、口渴甚至恐惧等强烈的生存需求,能够有效“关闭”我们对持续性疼痛的感知。这项研究不仅让我们对疼痛有了全新的认识,也为开发新型镇痛疗法带来了希望。
我们的大脑里,藏着一个“疼痛开关”
想象一下,我们的大脑就像一个极其复杂的指挥中心,负责处理从身体各处传来的海量信息,其中就包括“疼痛”这个重要的警报信号。当我们的身体受到伤害时,比如手指被割伤,痛觉信号会沿着神经系统这条“高速公路”迅速上传至大脑,告诉我们“这里出问题了,需要关注!”
长久以来,科学家们一直在努力寻找大脑中精确处理这些痛觉信号,尤其是那些在身体伤口愈合后仍然“纠缠不休”的慢性疼痛信号的“中央处理器”。以往的研究已经定位了一些处理瞬间、急性疼痛的神经元,但对于那种持续的、令人备受折磨的“背景式”疼痛,我们的大脑是如何感知和调控的,仍然是一个谜。
这项新研究将目光锁定在了一个名为外侧臂旁核 (lPBN) 的脑区。这个区域位于脑干深处,像一个重要的交通枢纽,接收来自身体的各种感觉信号(包括疼痛),同时也是整合多种情绪和行为状态(如饥饿、恐惧)的关键节点。研究人员猜测,正是在这个枢纽里,疼痛信号可能被其他更紧急的“生存信号”所压制。
找到关键“按钮”:表达Y1R的神经元
为了在这个复杂的枢纽中找到精确调控疼痛的“开关”,研究团队使用了一种名为“空间转录组学”的尖端技术。这项技术可以让他们不仅能识别出大脑组织中每一个细胞的分子身份(即哪些基因是活跃的),还能知道这些细胞在空间上的精确位置,就像为大脑绘制了一张高清的“分子地图”。
通过这张地图,他们发现了一群非常特殊的神经元。这些神经元并不像之前发现的某些疼痛相关神经元那样聚集在一起,而是广泛地分布在臂旁核的各个亚区,并且分子类型也多种多样。然而,它们拥有一个共同的“身份标签”——它们的细胞膜上都表达一种叫做**“神经肽Y受体Y1”(简称Y1R)**的特殊蛋白。
这个Y1R就像一个“信号接收器”或“对接端口”。当一种名为**神经肽Y(NPY)**的信号分子出现时,它就会与Y1R结合,从而改变这些神经元的活动状态。研究人员将这些表达Y1R的神经元命名为 “Y1R神经元”。
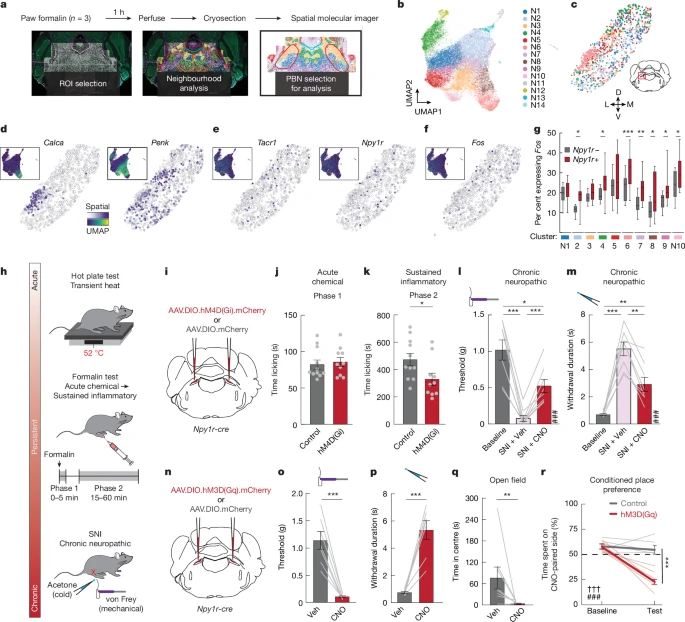
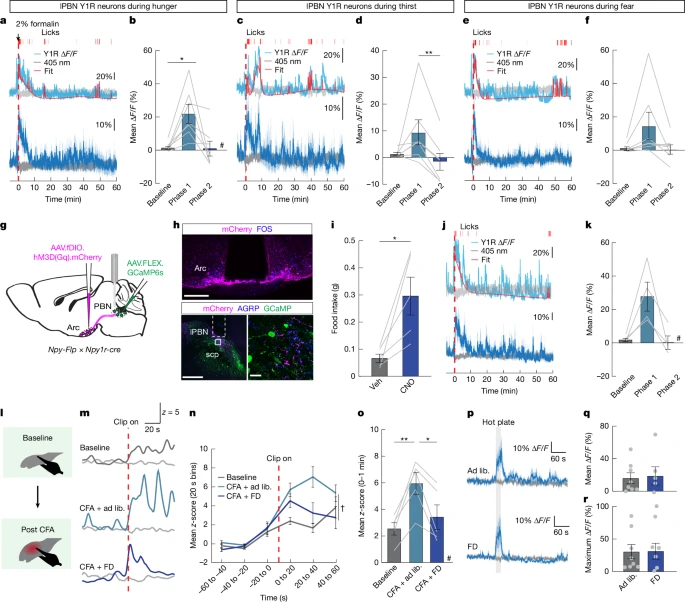
更有趣的是,当研究人员给实验小鼠注射能引发持续性疼痛的物质(如福尔马林)后,他们发现这些Y1R神经元的活跃度显著增加了,并且活跃程度与小鼠表现出的疼痛行为(如舔舐爪子)密切相关。这强烈暗示,Y1R神经元的持续活跃,可能就是大脑感知“持续性疼痛”的关键信号。
验证“开关”功能:打开就痛,关闭则止
为了验证这个猜想,科学家们进行了一系列精巧的实验,可以说是对这群Y1R神经元进行了“遥控操作”。
实验一:“关闭”开关,疼痛感减弱
研究人员利用化学遗传学技术,给小鼠的Y1R神经元装上了一个特殊的“人造受体”。当给小鼠注射一种无害的化学物质(CNO)时,这个受体就会被激活,从而抑制Y1R神经元的活动,相当于按下了“关闭”按钮。
结果非常惊人:
对于持续性的炎症疼痛(福尔马林注射的后期反应)和慢性神经痛(由神经损伤引起),当Y1R神经元被抑制后,小鼠的疼痛行为(如对触碰和冷刺激的敏感度)都显著减轻了 1。
然而,这种抑制对于急性的、短暂的疼痛(如福尔马林注射的瞬间反应或热刺激)并没有影响 2。
这个结果说明,Y1R神经元这个“开关”主要控制的是“持续性”的疼痛状态,而非瞬间的疼痛警报。这就像关掉了房间里嗡嗡作响的背景噪音,但并没有影响你听到突然响起的门铃声。
实验二:“打开”开关,无伤也痛
反过来,如果人为地“打开”这个开关会怎样呢?研究团队给另一组小鼠的Y1R神经元装上了另一种“人造受体”,注射CNO后会激活而非抑制这些神经元。
结果同样引人注目:
当Y1R神经元被激活时,即使小鼠身体没有任何损伤,它们也表现出了典型的疼痛症状,比如对轻微的机械触碰和冷刺激变得异常敏感(即痛觉超敏)3。
小鼠还表现出焦虑、奔跑、跳跃等行为,并且会强烈回避那个与神经元激活相关联的环境,这表明激活Y1R神经元不仅会产生类似疼痛的感觉,还会带来强烈的不愉快情绪 4。
这两个实验有力地证明了,臂旁核中的Y1R神经元是编码和传递持续性疼痛状态的核心节点。它们就像一个“疼痛状态指示灯”,灯亮着,大脑就认为身体正处于持续的痛苦之中。
饥饿与恐惧:身体自带的“超级镇痛剂”
现在,我们回到了最初的问题:为什么饥饿时我们对疼痛的感知会降低?研究团队认为,答案就藏在那个能够与Y1R“对接”的信号分子——**神经肽Y(NPY)**上。
NPY是一种非常重要的神经递质,它在大脑中扮演着多重角色,最著名的就是促进食欲。当我们感到饥饿时,大脑中的特定区域就会释放大量的NPY。研究人员推测,这些NPY可能不仅仅作用于食欲中枢,还可能“顺便”作用于臂旁核的Y1R神经元,从而起到镇痛的作用。
生存需求优先于疼痛感知
为了验证这一点,他们进行了一系列行为学实验,模拟了动物在野外面临的各种生存挑战:
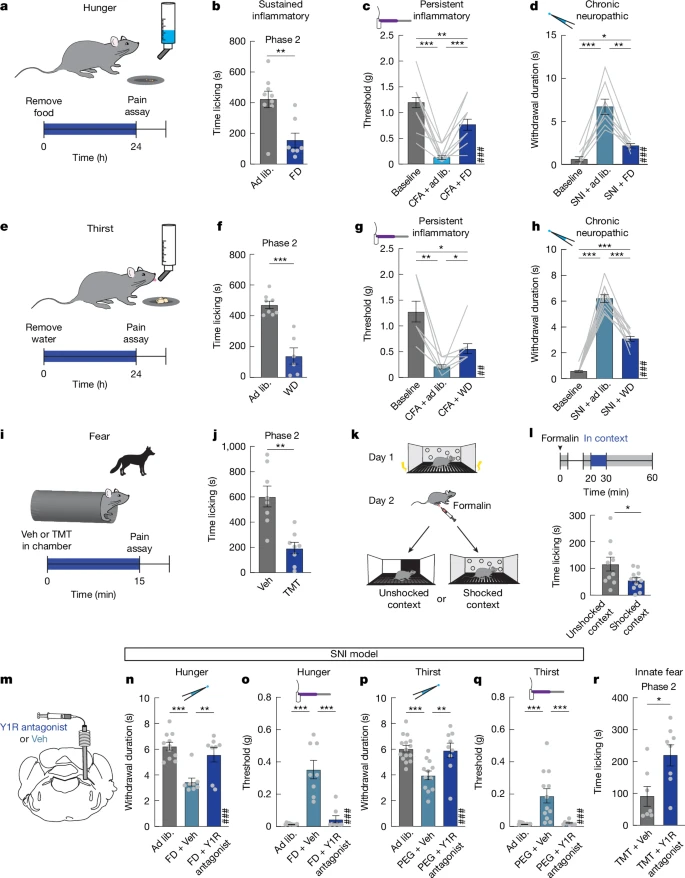
饥饿:将小鼠禁食24小时。
口渴:将小鼠禁水24小时,或注射一种能引发强烈口渴感的物质(PEG)。
恐惧:在环境中释放捕食者的气味(TMT),或将小鼠置于曾受过电击的可怕环境中。
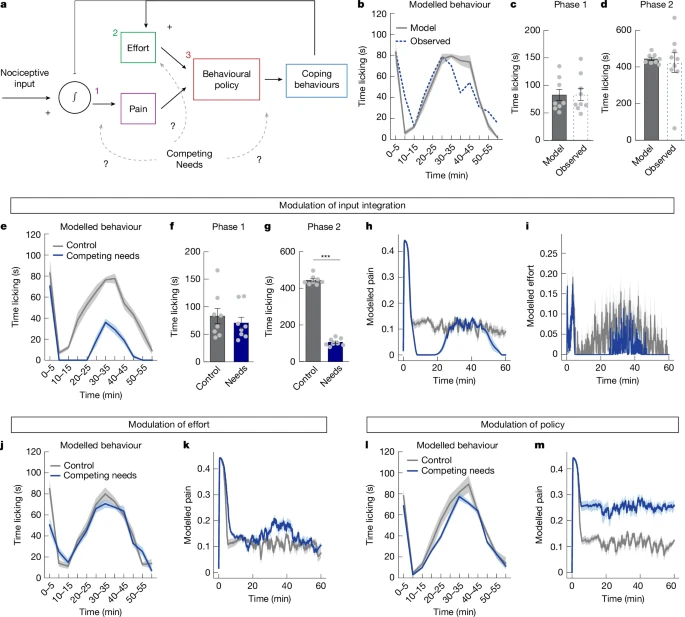
结果发现,无论是饥饿、口渴还是恐惧,这些强烈的“生存需求”都能够显著抑制小鼠在持续性炎症疼痛和慢性神经痛模型中的疼痛行为 555555555。这就像大脑在说:“现在有更重要的事情要处理(找食物、找水、躲避天敌),身上的这点小痛先放一放!”
重要的是,这些生存需求同样只抑制“持续性”的疼痛,对急性疼痛反应没有影响 6。这进一步证明了大脑中存在一种精密的机制,能够在不牺牲对新危险的快速反应能力的前提下,选择性地忽略那些“旧的”、持续的疼痛信号。
NPY-Y1R信号通路是关键
那么,这个镇痛效果真的是通过NPY和Y1R这条通路实现的吗?研究人员通过直接在小鼠的臂旁核中注射一种Y1R的阻断剂(一种能抢先占据“对接端口”,阻止NPY与之结合的药物)来回答这个问题。
结果发现,当Y1R被阻断后,饥饿、口渴和恐惧带来的镇痛效果全都消失了 7。这就像切断了NPY这个“镇痛信使”和Y1R这个“接收器”之间的联系,使得大脑无法再执行“忽略疼痛”的指令。
这个实验完美地形成了一个闭环,证明了在面临更紧急的生存需求时,大脑会释放NPY,NPY作用于臂旁核中的Y1R神经元,从而抑制这些神经元的活动,最终达到“关闭”持续性疼痛感知的效果。
深入观察:神经元活动如何被“静音”
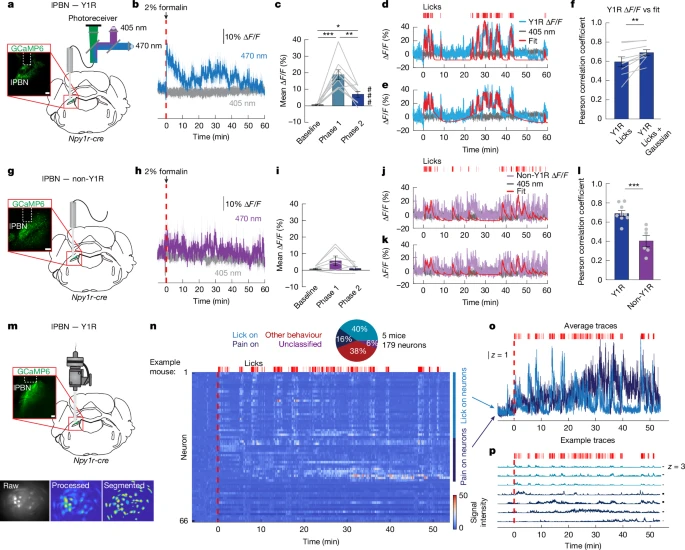
为了亲眼看到这个“镇痛”过程是如何在神经元层面发生的,研究人员使用了纤维光度法技术。他们将一种能对钙离子浓度(神经元活跃度的指标)产生荧光反应的“传感器蛋白”导入到Y1R神经元中,并通过一根植入大脑的光纤来实时监测这些神经元的“喜怒哀乐”。
他们发现:
在正常情况下,福尔马林注射会引起Y1R神经元活动持续、显著的升高 8。
然而,当小鼠处于饥饿、口渴或恐惧的状态下时,福尔马林注射后Y1R神经元的活动几乎没有升高,就像被“静音”了一样 9。
这个结果直观地展示了生存需求是如何在源头上“掐断”持续性疼痛信号的。大脑并没有让我们“忍受”疼痛,而是直接调低了编码疼痛的神经元的音量,让我们从根本上就不再那么“感觉”到疼痛了。
从“跑龙套”到“主角”:重新认识持续性疼痛
这项研究最深刻的意义之一,是它帮助我们区分了两种不同性质的疼痛信号。
快速的、与行为相关的信号:这部分信号与具体的应对行为(如舔舐伤口)紧密相关,来得快去得也快。
缓慢的、持续的“背景”信号:这部分信号反映了一种持久的“疼痛状态”,即使在没有进行具体应对行为时也持续存在。
通过对单个Y1R神经元活动的精细分析,研究发现Y1R神经元群体中存在明确的分工。大约40%的Y1R神经元属于“行为反应型”,只在小鼠舔舐伤口时才活跃;而另外约16%的神经元则属于**“疼痛状态编码型”,它们在受伤后会进入一种持续的、高水平的活跃状态**,而这种状态与具体的行为无关 10。
正是这群“疼痛状态编码型”的Y1R神经元,构成了我们对持续性疼痛的神经基础。而饥饿、恐惧等生存信号所抑制的,也正是这部分缓慢、持续的“背景”信号。
对我们的启示:通往未来新型镇痛疗法之路
这项研究的发现,不仅仅是满足了我们的好奇心,更为解决困扰全球数亿人的慢性疼痛问题,开辟了全新的思路。
精准的治疗靶点:臂旁核的Y1R神经元,特别是那个缓慢编码疼痛状态的亚群,成为了一个极具潜力的新型镇痛药物靶点。未来的药物开发或许可以专注于设计能够特异性抑制这群神经元活动的分子,从而在不影响急性疼痛预警功能的前提下,有效缓解慢性疼痛。
理解“情境镇痛”:这项研究科学地解释了许多我们生活中的现象,比如“转移注意力可以止痛”。无论是沉浸在一部精彩的电影中,还是在进行一项极具挑战性的工作,这些高度投入的状态可能也在调动类似NPY这样的内源性镇痛系统,通过抑制Y1R神经元来减轻我们对疼痛的感知。
身心健康的联系:研究强调了生理状态(如饥饿)和情绪状态(如恐惧)对疼痛感知的巨大影响。这也提醒我们,在治疗慢性疼痛时,不能仅仅局限于处理身体的损伤,更要关注患者的整体身心状态。改善营养、调节情绪、减轻压力,或许都能成为辅助治疗疼痛的有效手段。
总而言之,我们的大脑远比我们想象的要复杂和智能。它内置了一套精密的“优先级排序系统”,能够在关键时刻,为了更重要的生存目标,暂时屏蔽掉那些持续的、恼人的疼痛信号。解开这个“疼痛开关”的秘密,无疑是人类在战胜疼痛的漫长道路上,迈出的又一坚实步伐。未来,我们有理由相信,科学家们将能基于这些发现,开发出更安全、更有效的镇痛疗法,让无数被疼痛困扰的人们重获高质量的生活。
📕文章信息: Goldstein, N., Maes, A., Allen, H.N. et al. A parabrachial hub for need-state control of enduring pain. Nature (2025). https://doi.org/10.1038/s41586-025-09602-x