NSC通俗阅读,带你探索更多来自《自然》《科学》《细胞》等顶刊中的奇妙研究世界🧪🧠🌍
【Cell】熬夜“伤肝”,究竟“伤”在哪?科学家用“彩虹时间”相机,亲眼看到了细胞死亡的全过程

一、你的每一次熬夜,细胞都在经历一场“灾难大片”
我们都听过无数遍“熬夜伤身”,但这种“伤害”究竟是什么样的?它看不见,摸不着,似乎只是一种模糊的健康警告。直到今天,我们可能才有了“亲眼目睹”这场细胞级灾难的机会。
想象一下,当你深夜不眠,刷着手机时,你身体里的每一个细胞可能正在经历一场风暴。有的细胞因为能量供应不上而“罢工”,有的则在氧化应激的“枪林弹雨”中挣扎,甚至走向死亡。这个过程复杂而混乱,细胞核、线粒体、内质网……这些我们中学课本里学过的细胞器,它们之间是如何相互作用,又是如何一步步走向崩溃的?
过去,科学家想看清这一切,就如同想在人山人海的春运火车站里,同时追踪好几个不同目的地的旅客一样困难。传统的荧光显微镜技术,就像给旅客穿上不同颜色的衣服,比如去北京的穿红色,去上海的穿绿色。但颜色就那么几种,想同时追踪七八个甚至更多目标,颜色就不够用了,很容易“看串了行”。这极大地限制了我们对复杂生命过程的理解。
然而,来自西湖大学张鑫教授团队的一项突破性研究,彻底改变了游戏规则。他们在顶级期刊《细胞》(Cell)上发表了一篇名为《时间分辨荧光蛋白拓展荧光显微镜的时间与光谱维度》的论文 ,为我们带来了一套全新的“生命摄像系统”。这套系统不仅能分辨“颜色”,还能分辨“时间”,让我们得以用前所未有的清晰度,去观察细胞内部繁忙而有序,或是在压力下混乱崩溃的世界。
这项技术的核心,是一种被他们称为**“时间分辨荧光蛋白”(tr-FPs)**的神奇工具 。
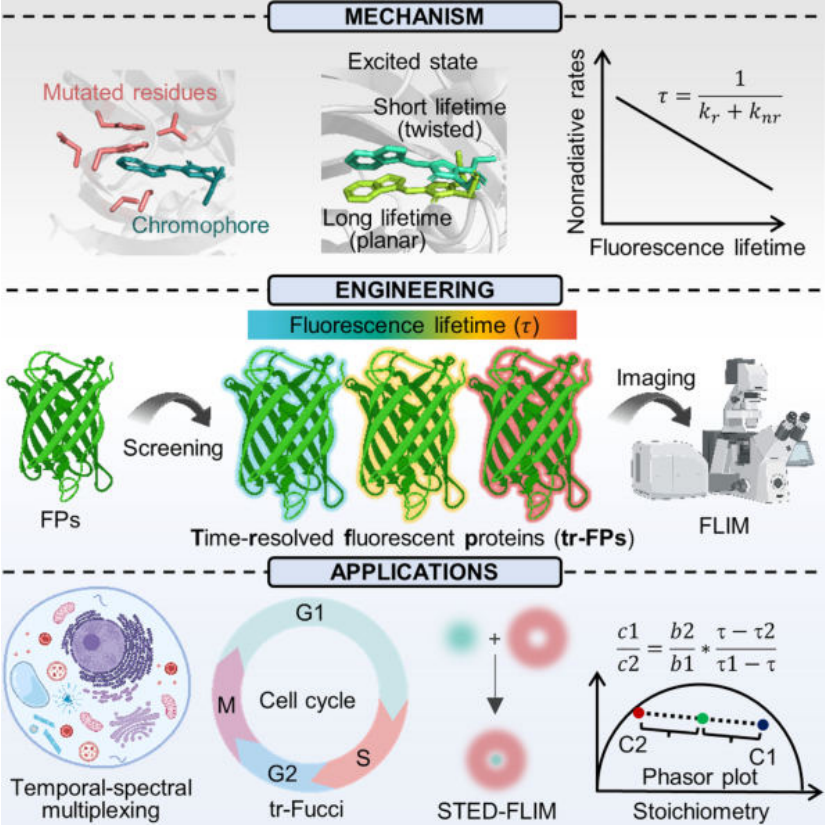
二、给生命打上“时间邮戳”:不仅仅是五颜六色
要理解这项技术的革命性,我们得先聊聊它的前辈——荧光蛋白。自从发现绿色荧光蛋白(GFP)的科学家获得诺贝尔奖以来,用不同颜色的荧光蛋白标记细胞内的特定分子,就成了生物学研究的常规操作。这就像是在黑暗的细胞宇宙中,点亮一颗颗不同颜色的星星,让科学家能够追踪蛋白质的行踪。
然而,正如前面提到的,可见光的颜色是有限的,光谱重叠的问题让科学家们很快就遇到了瓶颈 。我们想同时观察细胞凋亡过程中,细胞核的变化、线粒体的损伤、内质网的应激、高尔基体的解体、溶酶体的反应……仅仅用几种颜色是远远不够的。
张鑫团队的科学家们跳出了“颜色”的思维定势,引入了一个全新的维度——荧光寿命 。
什么是荧光寿命?我们可以打个比方。想象你在夜晚看到许多盏灯,它们不仅颜色不同(红、绿、蓝),而且每一盏灯闪烁后,从亮到灭的持续时间也不同。有的灯“啪”一下就灭了,只亮了1纳秒;有的灯则会慢慢变暗,持续亮了5纳秒。
这个“持续时间”,就是荧光寿命(Fluorescence Lifetime!) 。它是一个荧光分子被激发后,在激发态停留的平均时间,是一个内禀的、稳定的物理特性 。
有了这个概念,一切就变得豁然开朗。我们不仅可以给细胞里的不同蛋白质贴上“红色”“绿色”的颜色标签,还可以给它们贴上“亮1纳秒”“亮3纳秒”“亮5纳秒”的时间标签 。这样一来,即便两个蛋白质都是绿色的,只要它们的荧光寿命不同,我们就能在显微镜下把它们清晰地区分开来。
“颜色”(光谱)和“持续时间”(寿命),这两个维度一结合,就像给原本平面的照片加上了3D效果,信息的丰富度呈指数级增长。科学家们将这种新的成像方式称为**“时间-光谱”联用显微技术** 。
三、巧夺天工的“分子手术”:如何随心所欲地调控“时间”?
有了这个绝妙的想法,下一个问题就是:如何才能创造出这样一群荧光寿命各不相同,且能覆盖整个可见光谱的荧光蛋白呢?
这就要提到这项研究最核心、最巧妙的工程策略了。荧光蛋白的发光,依赖于其内部一个被称为“生色团”的核心分子结构 。这个生色团就像灯泡里的灯丝。研究团队发现,生色团在被激发后会发生非常快速的旋转运动,这种运动会以非辐射(不发光)的形式消耗掉一部分能量,从而影响荧光寿命的长短 。
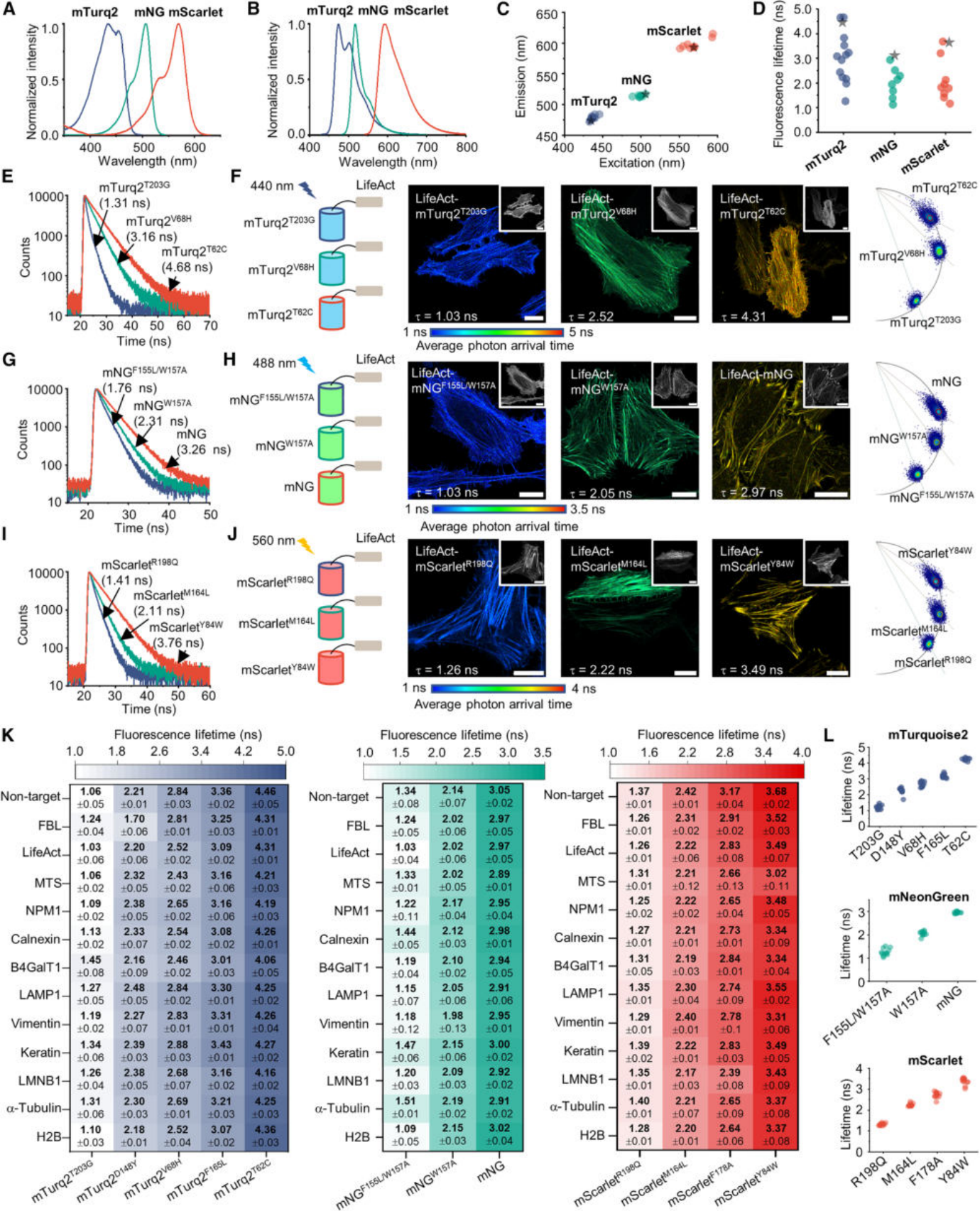
他们的核心策略是:通过改变生色团周围的氨基酸“微环境”,来控制它的旋转。
这就像是给一个陀螺(生色团)旋转的地面设置不同的障碍物。如果周围空间很拥挤,障碍物很多(特定的氨基酸),陀螺就转不起来,能量更多地以光的形式释放,荧光寿命就长。反之,如果把周围的障碍物挪开,让空间变得宽敞,陀螺就能自由旋转,更多能量通过非辐射途径耗散掉,荧光寿命就变短了 。
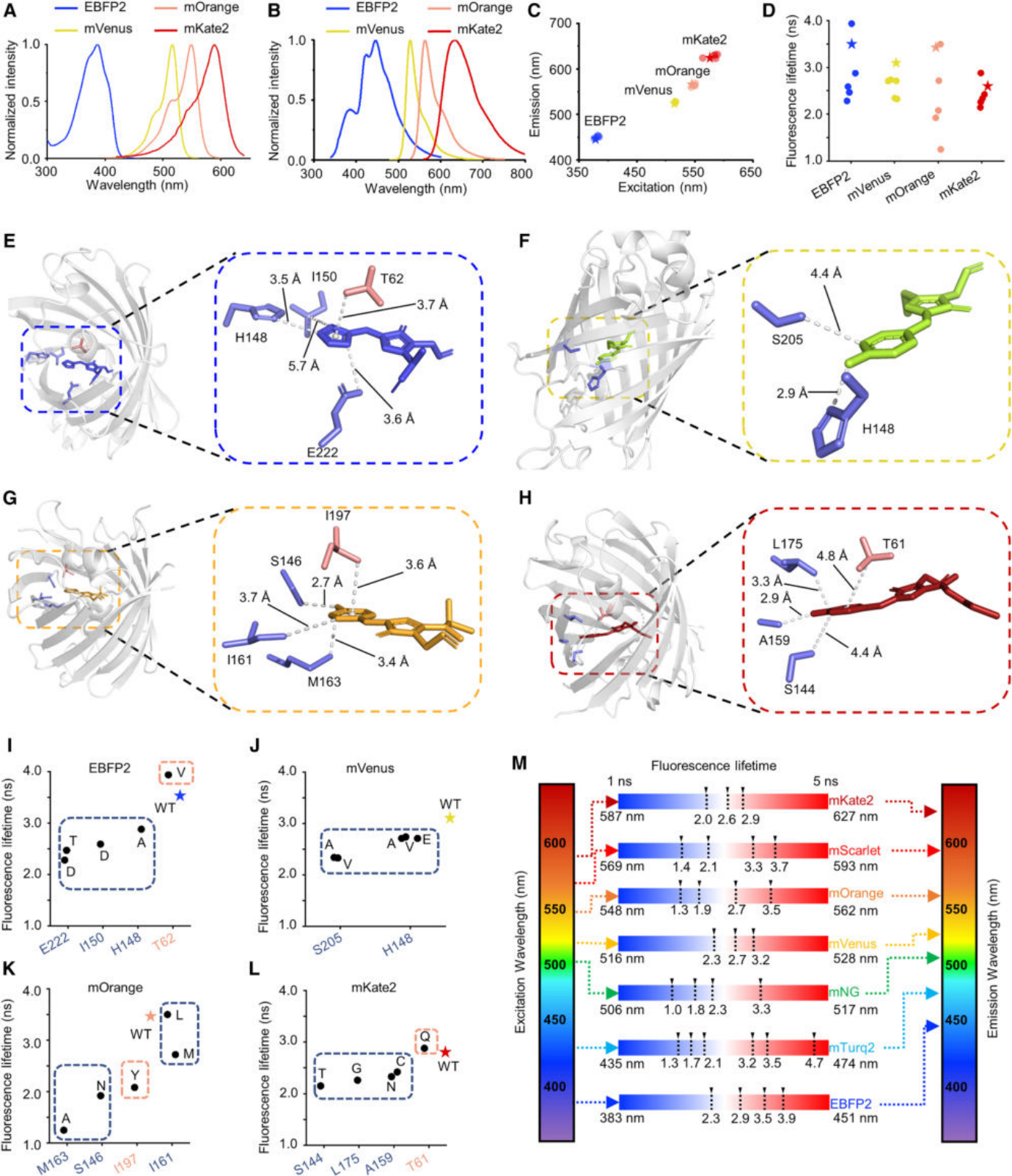
通过对距离生色团6埃(1埃 = 0.1纳米)范围内的氨基酸进行饱和突变筛选 13,研究团队就像进行着一场场精密的“分子手术”,最终成功地创造出了一整套“时间分辨荧光蛋白彩虹工具箱” 。这个工具箱里包含了从蓝色到红色,覆盖整个可见光谱的28个成员,它们的荧光寿命可以精确地在1到5纳秒之间调控,而且这种寿命特性非常稳定,无论把它们送到细胞的哪个角落,表现都基本一致 。
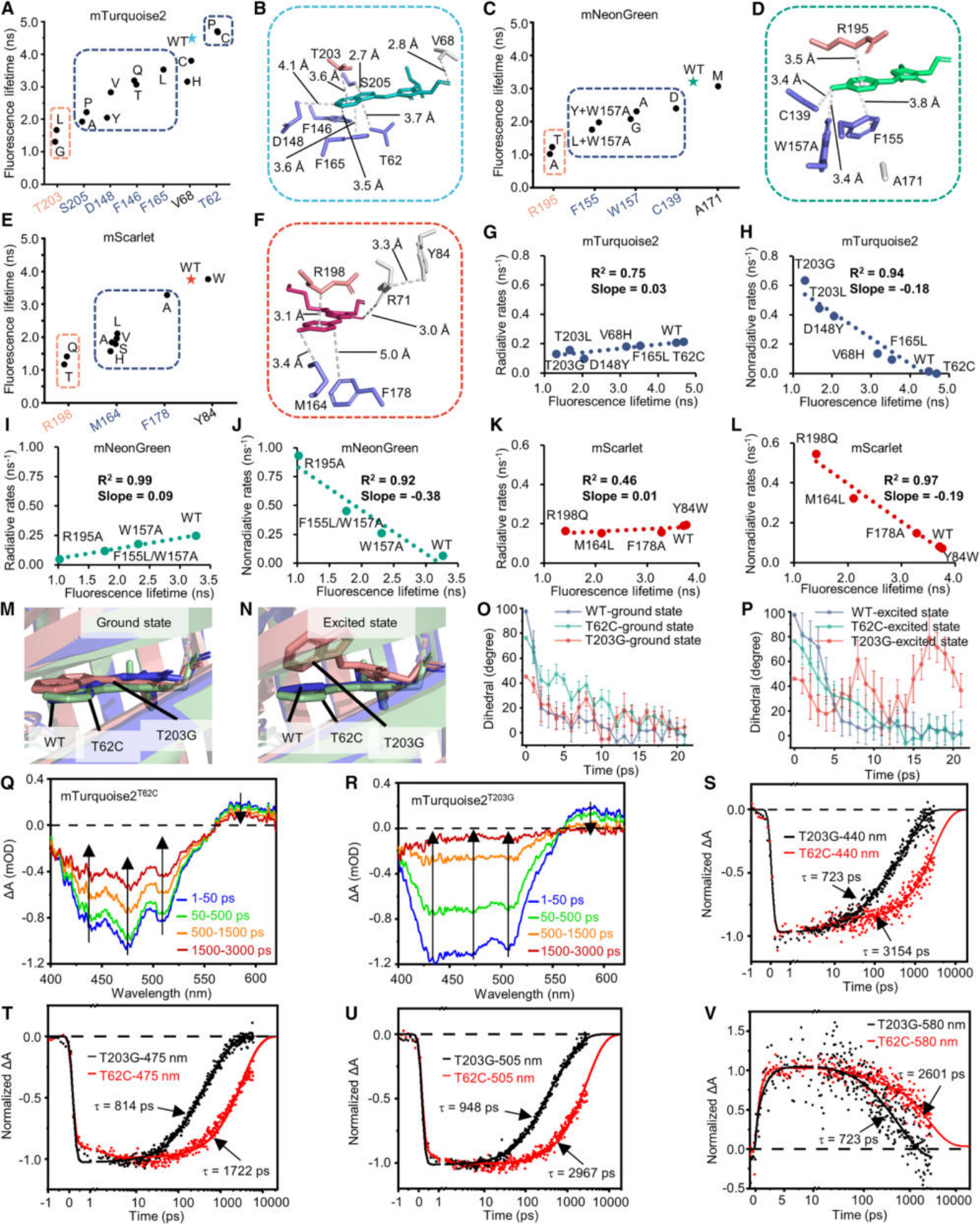
这就像是拥有了一套包含各种颜色、各种亮度衰减速度的“生命颜料”,为描绘复杂的生命画卷提供了前所未有的可能。
四、现场直播细胞“生死劫”:我们看到了什么?
拥有了这套强大的“彩虹时间”相机,科学家们首先就将镜头对准了文章开头提到的那个终极问题——细胞是如何死亡的?他们选择了两种经典的细胞死亡模式进行观察:铁死亡(ferroptosis)和氧化应激(oxidative stress) 。
这两种死亡方式,都与我们日常生活息息相关。比如,一些神经退行性疾病、缺血性损伤与铁死亡有关;而我们常说的熬夜、压力、环境污染等导致的身体损伤,很大程度上就是通过氧化应激实现的。
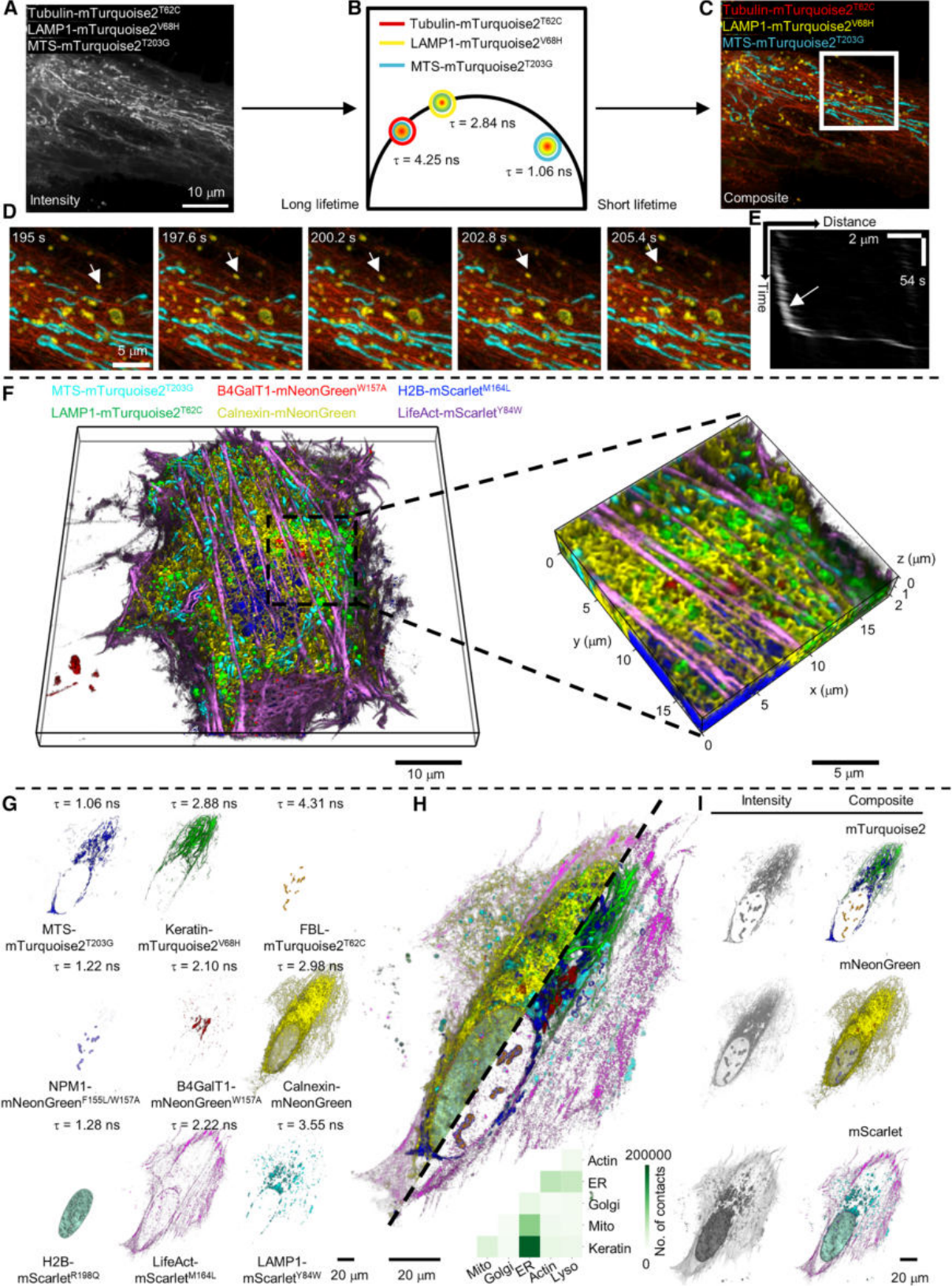
在过去,我们只能在某个时间点,像拍照片一样,看到细胞死亡后的“遗照”。而现在,研究团队在同一个活细胞内,同时标记了9个不同的细胞器和结构蛋白,进行了一场长达数小时的4D(三维空间+时间)延时摄影 。
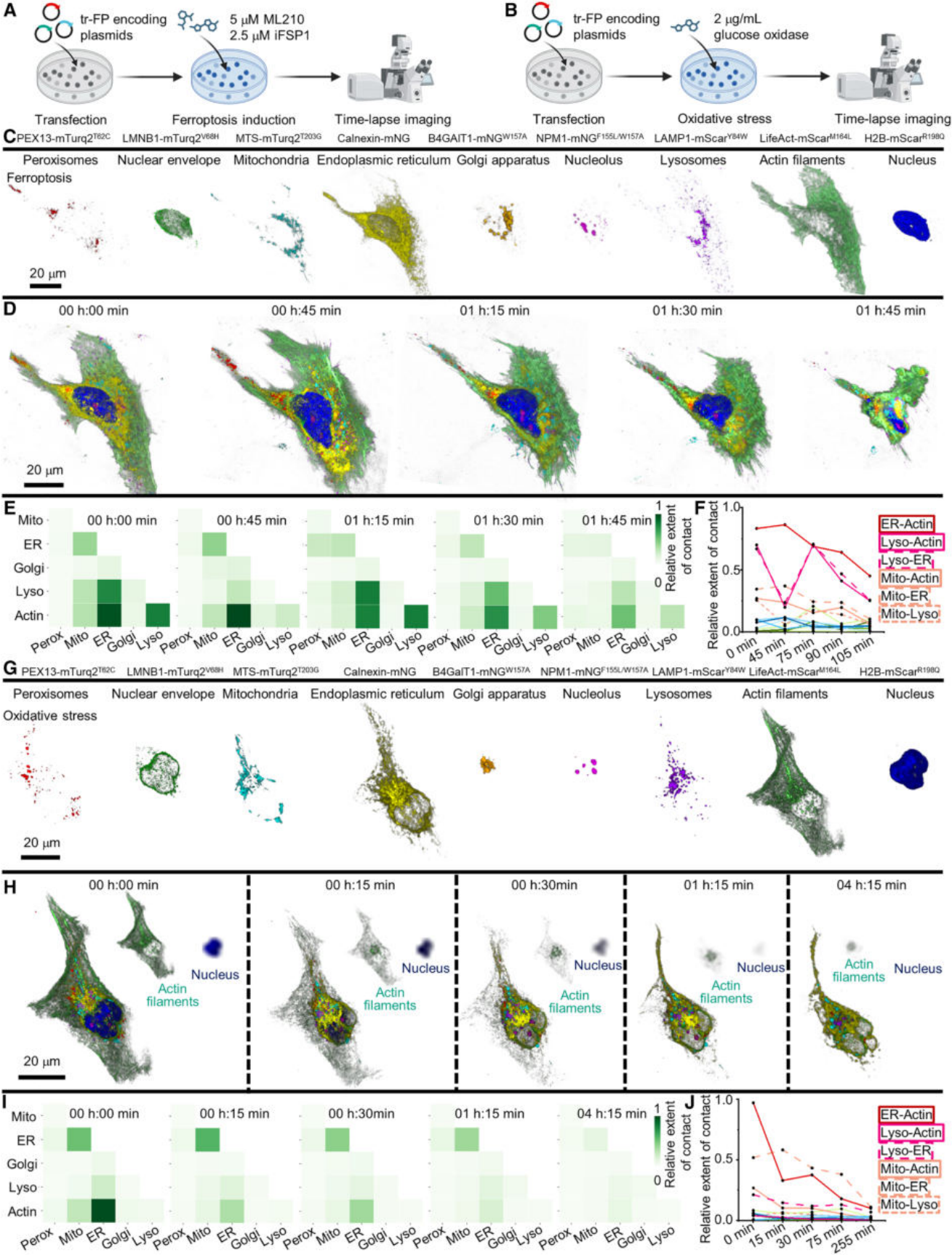
直播开始了,震撼的场面上演:
在铁死亡中:细胞最先出现的反应是体积的迅速收缩 。随后,作为细胞内“能量工厂”和“生产车间”的内质网,开始急剧地收缩、断裂并形成大量空泡,仿佛一座正在崩塌的工厂 。紧接着,线粒体也从正常的条状碎裂成颗粒状 。尤其引人注目的是,高尔基体也发生了惊人的崩溃,这暗示着细胞内的“物流中心”可能也极易受到铁死亡的攻击 。整个过程,就像一场由内而外、以膜系统破坏为核心的精准爆破。
在氧化应激中:细胞展现了截然不同的“死法” 。最显著的变化发生在细胞骨架(如同房屋的钢筋)和细胞核(指挥中心),它们在短短15分钟内就开始迅速降解 。这表明,氧化应激产生的“自由基”是无差别的攻击手,直接破坏了细胞最核心的结构和遗传物质 。
通过这种多目标、长时间的动态观察,科学家们首次如此清晰地分辨出不同死亡路径下,细胞内部各部件响应的先后顺序和独特模式。这些直观的视觉证据,为理解相关疾病的机制和开发新的治疗药物,提供了宝贵的线索。
五、从“看热闹”到“精细活”:tr-FPs 的更多“神操作”
这套“彩虹时间”工具箱的威力远不止于此。它还解锁了许多过去难以想象的“精细活”。
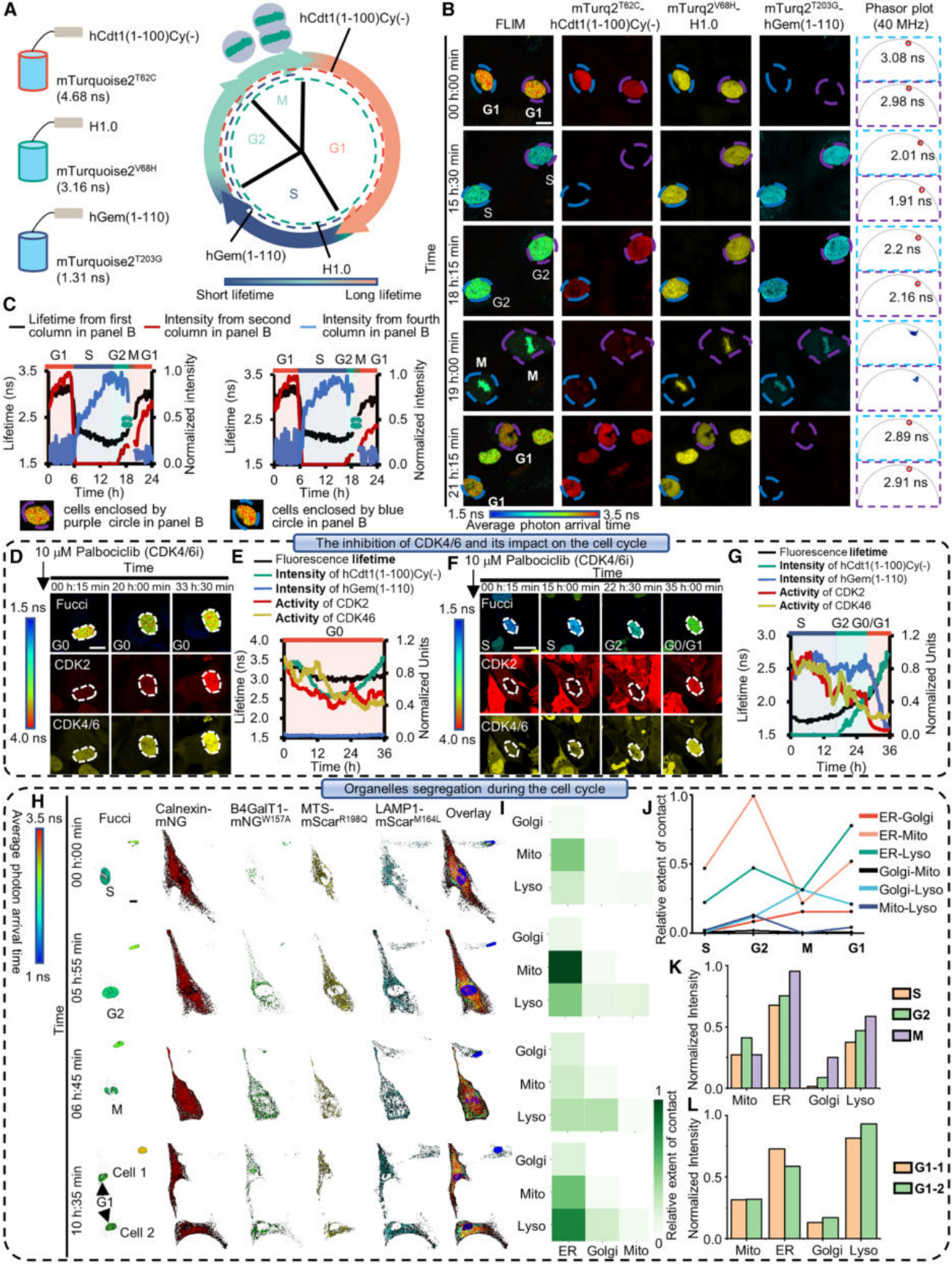
1. 单色光搞定细胞周期监控,还能“一心二用”
细胞周期,即细胞从一次分裂完成到下一次分裂结束所经历的过程,是生命最基本的核心节律。传统的细胞周期指示剂(如Fucci系统)需要两种不同颜色的荧光蛋白(比如红和绿)来分别标记不同时期,这直接占用了两个宝贵的光谱通道 。
而利用tr-FPs,研究团队开发出了全新的tr-Fucci系统 。他们巧妙地设计了多个荧光寿命不同的青色荧光蛋白,用它们来标记细胞周期的不同阶段。这样一来,只需要一个青色通道,通过分析荧光寿命的变化,就能精准地判断细胞处于G1、S、G2还是M期 。
这有什么好处呢?它解放了其他颜色通道!科学家们可以在监控细胞周期的同时,用绿色和红色的探针去观察其他生命活动,比如细胞周期蛋白依赖性激酶(CDK)的活性 。他们发现,CDK2和CDK4/6这两种关键的调控蛋白,在细胞周期中的活跃模式有着微妙而重要的区别 。这种将核心生命节律与其他动态事件关联起来分析的能力,是前所未有的。
2. 超高分辨率下的“四色同堂”
普通光学显微镜受到衍射极限的限制,分辨率只能达到约200纳米,这让我们无法看清许多精细的细胞结构。STED超高分辨率显微镜技术打破了这一限制,让我们能看到更小的世界。
现在,tr-FPs与STED技术强强联合,催生了STED-FLIM 。研究团队开发了适用于STED的tr-FP版本,成功地在同一个细胞中,用一个光谱通道,同时以超高分辨率分辨出了两种不同的结构——线粒体和微管 。更进一步,他们结合其他探针,实现了四种不同蛋白质的超高分辨率同时成像 。这就像是用一台超高清摄像机,在纳米尺度上,同时拍摄一部由四个主角出演的“细胞大片”。
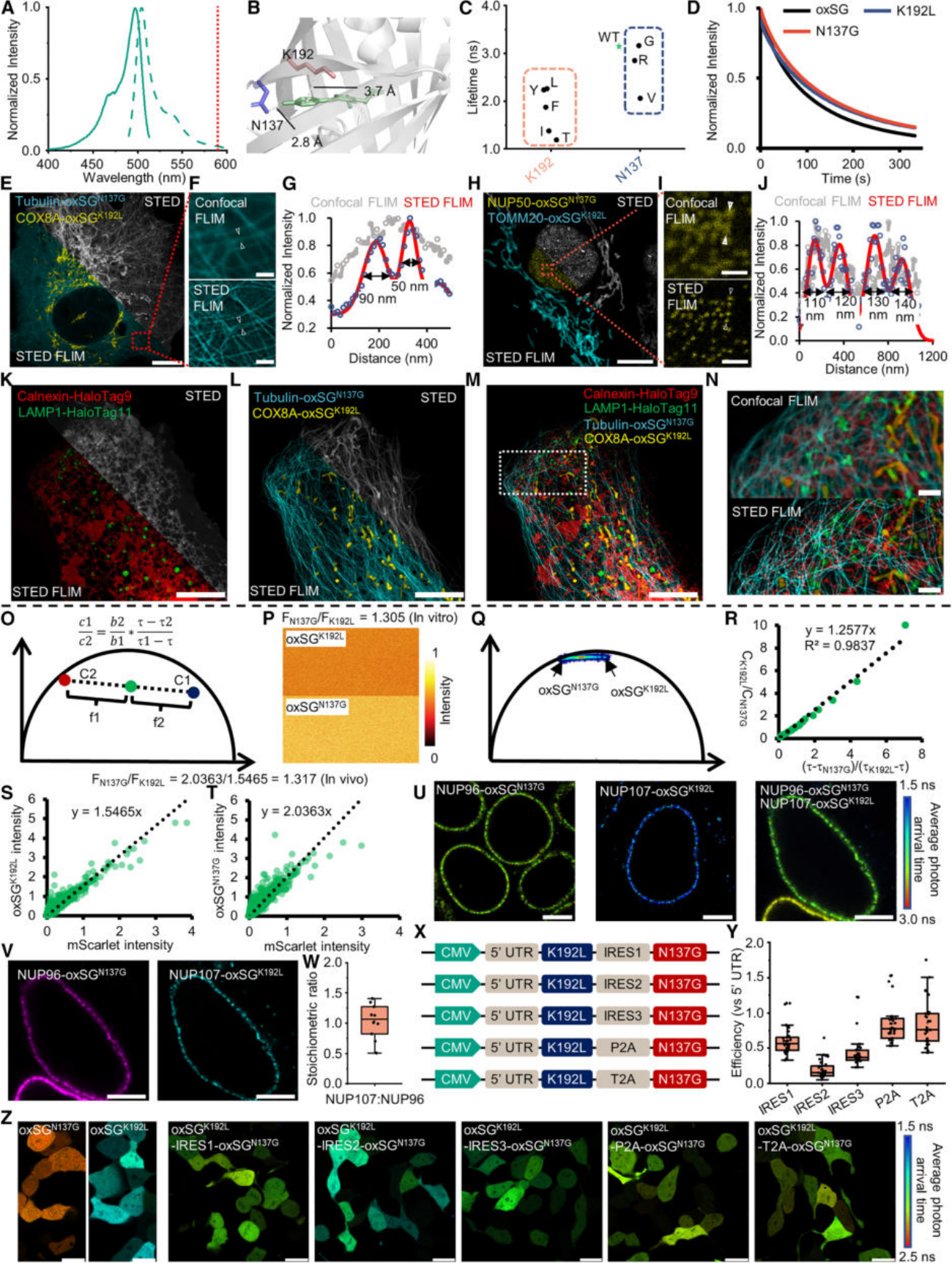
3. 给细胞里的“零件”做人口普查
一个复杂的机器,比如一台汽车发动机,其高效运转不仅需要各种零件,还需要这些零件之间保持精确的数量比例。细胞也是如此,细胞核孔复合物(NPC)是细胞核的“大门”,由多种核孔蛋白(NUP)构成,它们之间的精确比例至关重要。
过去,想在活细胞里精确“清点”这些蛋白质的数量比例,非常困难。而tr-FPs提供了一种绝妙的解决方案。利用荧光寿命可以进行线性拆分的特性,研究团队建立了一个数学模型,能够通过测量混合荧光信号的平均寿命,精确反推出两种不同寿命的荧光蛋白标记的蛋白质的化学计量比(stoichiometric ratio) 。
他们用这种方法,成功测定了细胞核孔蛋白NUP96和NUP107的比例约为1.1,与之前的研究结果高度吻合 。这项技术,为在单细胞水平上精确量化蛋白质机器的组成,打开了一扇新的大门。
六、结语:开启一个“看得更清、看得更多”的生命科学新纪元
从最初只能分辨寥寥几种颜色,到如今拥有一个“光谱+时间”双重维度的“彩虹时间”工具箱,张鑫团队的这项工作,不仅仅是一次技术的升级,更是一场观察生命范式的革命 。
它让我们能够同时追踪的生命事件数量翻倍甚至更多 37,让我们能将细胞最核心的节律与各种功能事件精准地关联起来 38,让我们能在纳米尺度上分辨前所未见的多彩世界 39,甚至还能对细胞内的分子进行“定量普查” 。
对于我们普通人而言,这意味着科学家们有了更强大的武器,去探索癌症、神经退行性疾病、衰老等复杂疾病的深层机制。今天我们能亲眼“直播”细胞的死亡过程,明天或许就能更精准地找到干预和拯救它们的办法。
这项源于基础研究的突破,也必将对未来的生物医药、新药研发、以及像飞秒科技这样的高端科学仪器产业产生深远的影响。一个能够“看得更多、看得更清”的时代已经来临,生命最深处的奥秘,正以前所未有的清晰度,展现在我们眼前。
📕文章信息: Tan et al., Time-resolved fluorescent proteins expand fluorescent microscopy in temporal and spectral domains, Cell (2025), https://doi.org/10.1016/j.cell.2025.08.035