【Biomaterials】近红外II发射的声动力荧光探针,诱导细胞凋亡以治愈癌症
总结
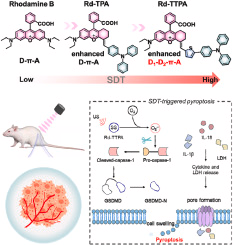
本研究设计了一种新型的NIR-II发射、可以诱导细胞焦亡的超声动力学治疗(SDT)增强剂Rd-TTPA,用于治疗肿瘤,并通过NIR-II荧光成像指导。
摘要
研究人员通过合成和特性研究,设计了一种新型的小分子细胞焦亡调节剂Rd-TTPA,该分子具有强的NIR-II荧光特性,能够在超声激发下产生大量的超氧根离子(O2),从而诱导肿瘤细胞发生细胞焦亡。Rd-TTPA采用了增强型受体-供体(A-π-D1-D2)结构,该结构有助于其在SDT中的高效ROS产生和NIR-II荧光成像能力。实验结果表明,Rd-TTPA在体内外都能有效地产生ROS,并且能够特异性地靶向肿瘤细胞的线粒体,从而在超声激发下诱导细胞焦亡。此外,Rd-TTPA在低氧条件下也能有效地诱导细胞焦亡,这为治疗氧气缺乏的肿瘤提供了新的策略。在小鼠模型中,Rd-TTPA显示出了优异的NIR-II荧光成像能力和抗肿瘤效果,能够有效抑制肿瘤生长,且不会对小鼠造成显著的毒性。研究还揭示了Rd-TTPA诱导的细胞焦亡通路,即通过激活细胞焦亡相关的Caspase-1/GSDMD通路,进而促进了细胞膜孔的形成和炎症因子的释放。
观点
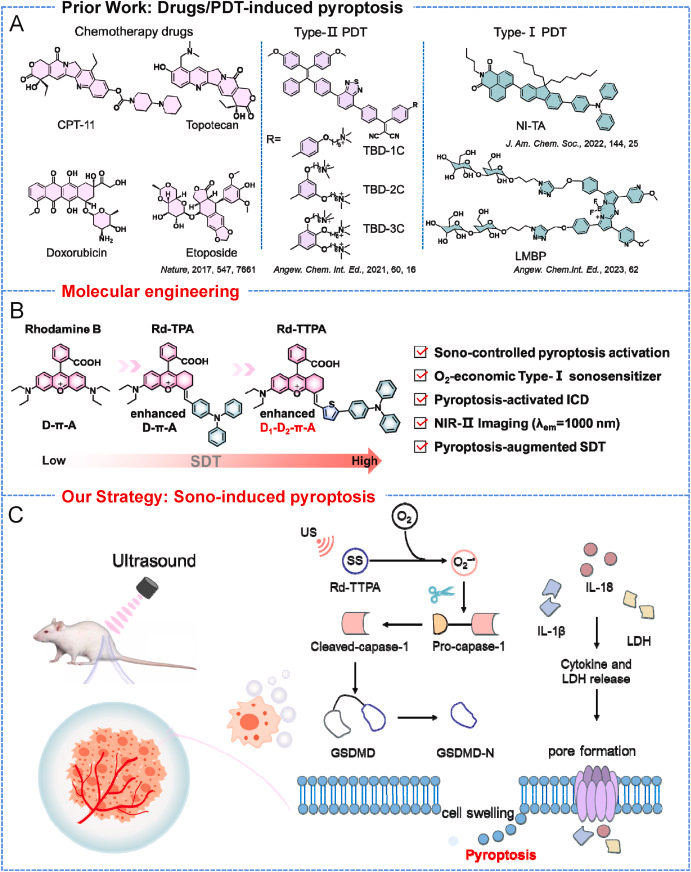
Rd-TTPA的设计基于增强型受体-供体(A-π-D1-D2)结构,这种结构有助于提高其在SDT中的ROS产生效率和NIR-II荧光成像能力。
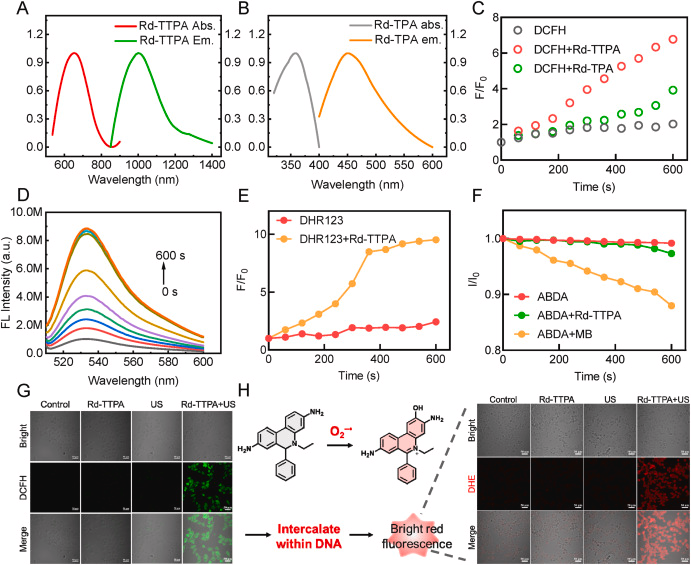
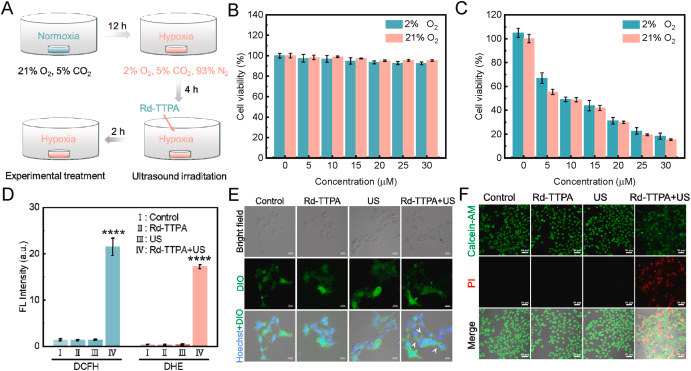
在体外实验中,Rd-TTPA能够在超声激发下产生大量的O2,这一特性使其能够作为一种有效的SDT增强剂。

Rd-TTPA能够特异性地靶向肿瘤细胞的线粒体,这对于诱导细胞焦亡具有重要意义。
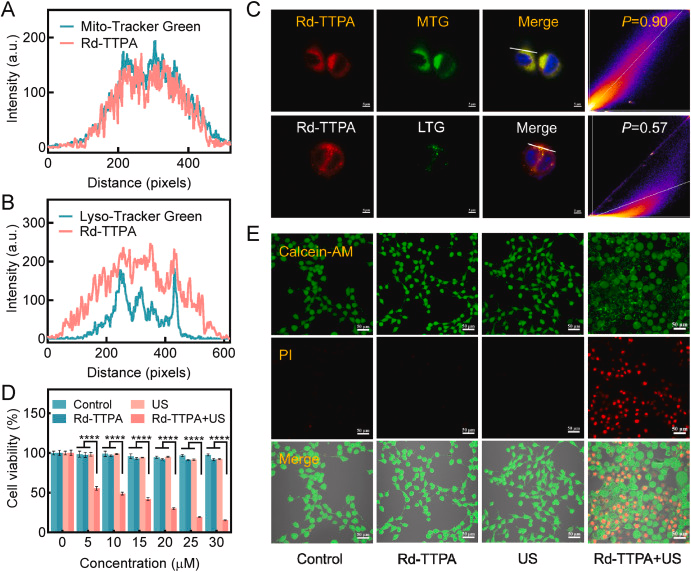
Rd-TTPA在低氧条件下仍能有效诱导细胞焦亡,这为治疗难以引入氧气的深部肿瘤提供了可能。
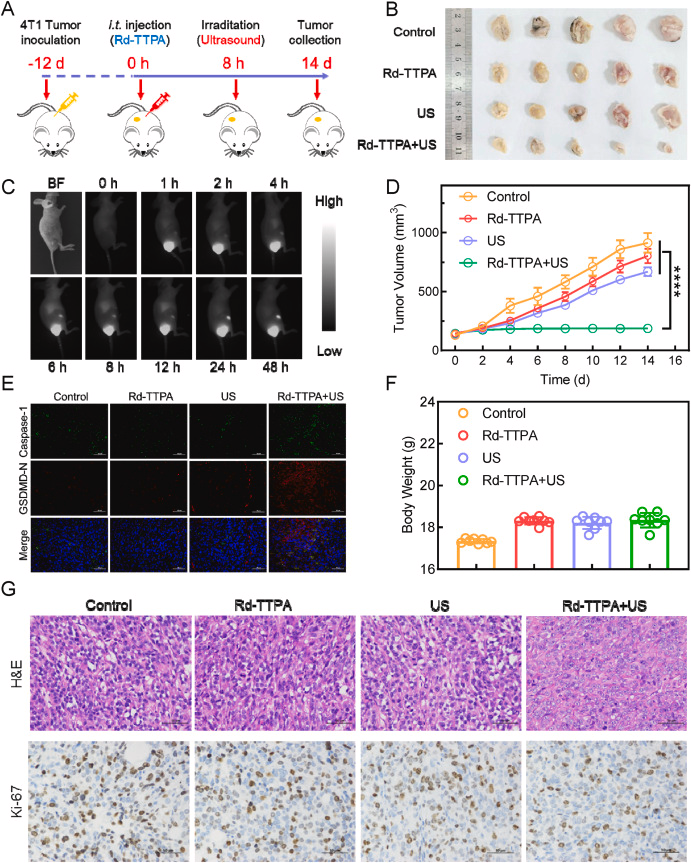
通过NIR-II荧光成像,Rd-TTPA能够在体内长时间滞留于肿瘤部位,这为SDT提供了精准的成像指导。在小鼠模型中,Rd-TTPA基于SDT的治疗方案显示出了显著的抗肿瘤效果,且不会对小鼠造成明显的毒性。
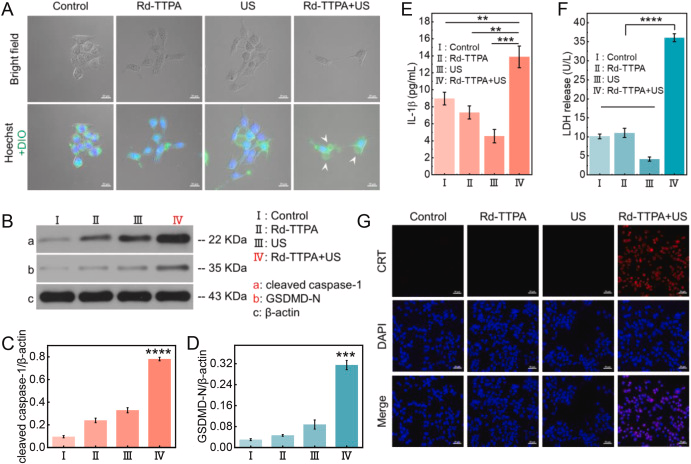
Rd-TTPA诱导的细胞焦亡是通过Caspase-1/GSDMD通路实现的,这一发现为细胞焦亡相关的治疗机制提供了新的见解。
参考文献
Wang, X.; Chi, W.; Wu, J.; Zou, J.; Yoo, J.; Hong, S.; Zhang, F.; Mao, Z.; Kim, J. S. A NIR-II Emissive Sonosensitized Biotuner for Pyroptosis-Enhanced Sonodynamic Therapy of Hypoxic Tumors. Biomaterials 2025, 315, 122969. https://doi.org/10.1016/j.biomaterials.2024.122969.