【Adv.Mater.】促进溶酶体逃逸,增强肿瘤浸润,提升治疗效果,新型纳米马达同时激活CDT和PTT,大幅度促进铁死亡
总结
本研究成功设计了一种近红外光激活的铁离子自供应纳米马达,用于增强肿瘤浸润和治疗,该纳米马达在近红外(NIR)照射下能够产生自热力作用,增强其在肿瘤微环境中的扩散能力,促进溶酶体逃逸并深入肿瘤组织,同时在酸性肿瘤微环境中释放羟基自由基(•OH)的前体H2O2和Fe离子,激活CDT和光热治疗PTT,实现肿瘤细胞的铁死亡。
摘要
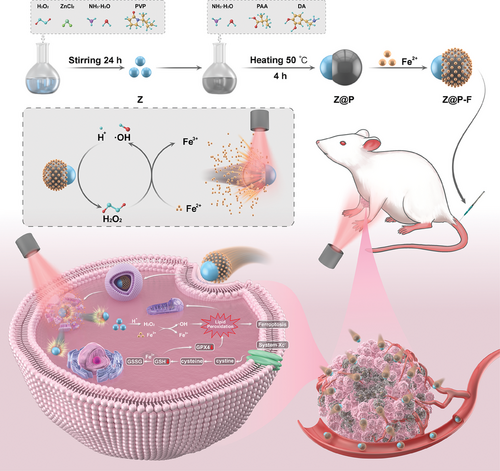
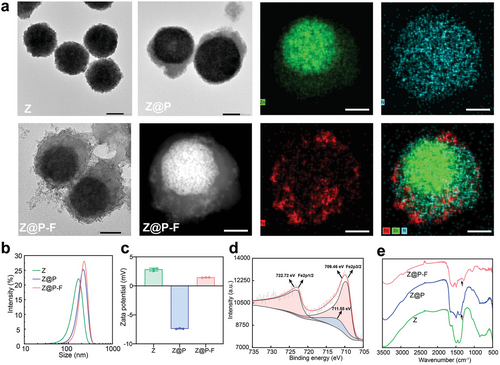
在这项研究中,研究者们设计并制备了一种NIR光激活的自热力驱动的纳米马达,用于增强肿瘤穿透和治疗。该纳米马达是用过氧化锌(ZnO2)对聚多巴胺(PDA)进行不对称修饰,然后通过PDA中的多酚基团螯合亚铁离子(Fe2+)而产生的。在NIR光照射下,Z@P-F纳米马达能够产生温度梯度,从而通过自热力作用增强其在肿瘤微环境中的扩散能力,有助于溶酶体逃逸并促进深入肿瘤组织。同时,在酸性肿瘤微环境中,Z@P-F能够缓慢释放H2O2和Fe离子,通过激活CDT和PTT,有效地促进了肿瘤细胞的铁死亡。实验结果表明,该纳米马达在体内外都展现出了显著的肿瘤杀伤效果,并且具有良好的生物相容性和安全性。
细节
NIR光激活的自热力作用
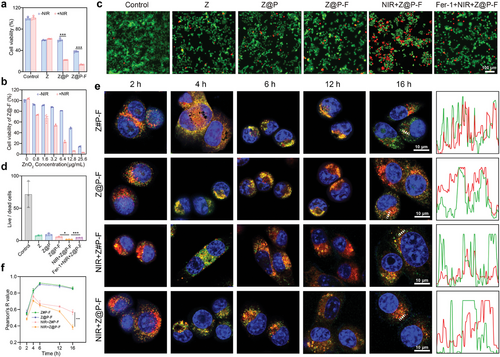
Z@P-F纳米马达在NIR光照射下能够产生温度梯度,通过自热力作用增强其在肿瘤微环境中的扩散能力,促进其在肿瘤组织中的深入浸润。 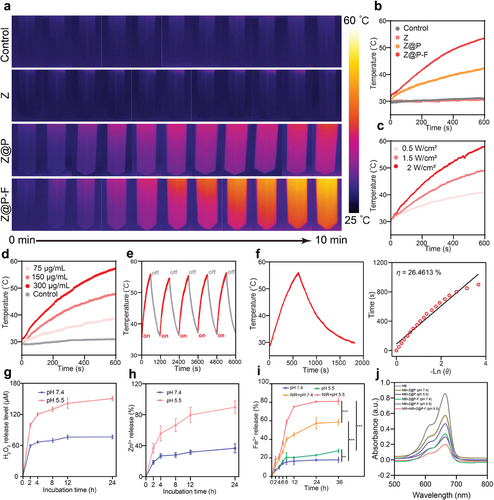
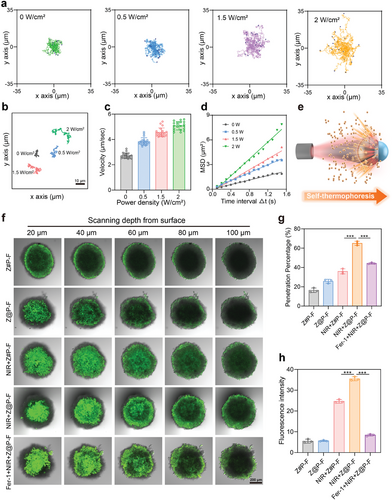
肿瘤微环境响应性
Z@P-F在酸性肿瘤微环境中能够缓慢释放H2O2和Fe离子,为CDT提供了必要的前体物质,同时与PTT相结合,实现了对肿瘤细胞的有效杀伤。
铁死亡的激活
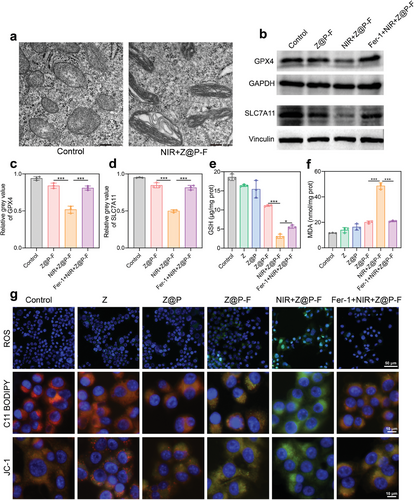
通过释放的H2O2和Fe离子激活的CDT,Z@P-F纳米马达能够诱导肿瘤细胞的铁死亡,这是一种基于铁离子依赖性的程序性细胞死亡方式。
多模态治疗策略
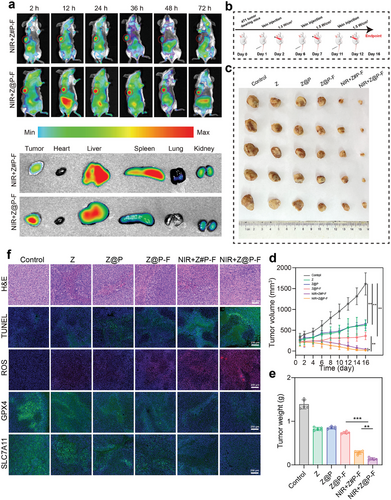
实验表明,Z@P-F纳米马达在体内外都具有良好的生物相容性和安全性,对正常组织的潜在损伤较小。但Z@P-F纳米马达的设计结合了CDT和PTT的优势,提供了一种多模态治疗策略,有望在临床肿瘤治疗中发挥重要作用。
参考文献
Hu, Z.; Tan, H.; Ye, Y.; Xu, W.; Gao, J.; Liu, L.; Zhang, L.; Jiang, J.; Tian, H.; Peng, F.; Tu, Y. NIR‐Actuated Ferroptosis Nanomotor for Enhanced Tumor Penetration and Therapy. Advanced Materials 2024, 2412227. https://doi.org/10.1002/adma.202412227.