【Nat. Mater.】突破肿瘤微环境中的隐形屏障,纳米药物递送效率提升8倍!
在纳米医学领域,纳米粒子作为药物和基因的载体展现出巨大潜力,已有多种产品获批用于临床治疗。然而,如何使纳米粒子在实体肿瘤中高效积累仍是一个重大挑战。最近,《Nat. Mater.》杂志上发表的一项研究由Drew Weissman, Wei Guo & Michael J. Mitchell 领导的研究团队,揭开了肿瘤细胞衍生的小细胞外囊泡(sEVs)对纳米粒子传递的阻碍作用,为纳米粒子在肿瘤治疗中的应用提供了新的见解。 
研究背景:
纳米粒子在肿瘤治疗中的主要挑战之一是如何提高其在肿瘤组织中的积累。尽管已有多种策略通过优化纳米粒子的大小、形状、表面化学和硬度来提高其在肿瘤中的积累,但效果仍有限。研究团队将目光投向了肿瘤微环境中的sEVs,这些小囊泡由肿瘤细胞分泌,可能对纳米粒子的传递构成障碍。 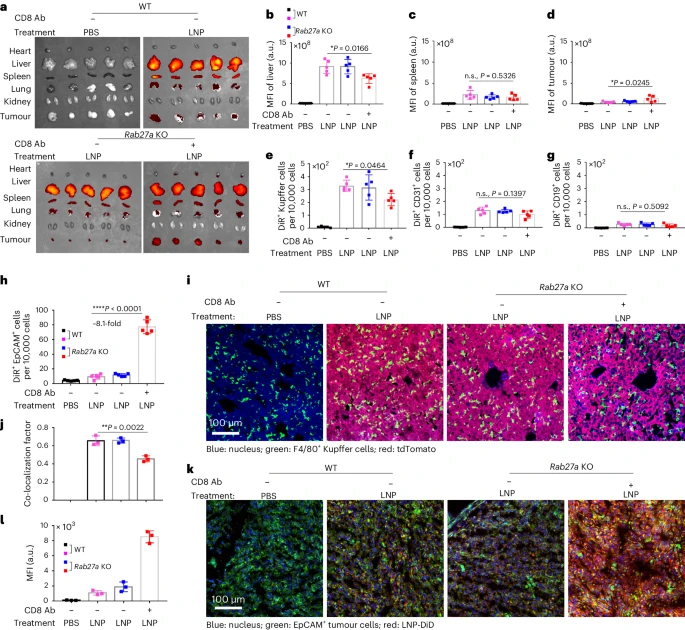
发现
研究团队发现,肿瘤细胞分泌的大量sEVs能在肿瘤微环境中与进入肿瘤组织的纳米粒子结合,并将它们运送至肝脏的Kupffer细胞中进行降解。这一发现表明,sEVs实际上构成了肿瘤对纳米粒子药物传递的一种。通过敲除控制sEVs分泌的Rab27a基因,研究人员成功降低了sEVs水平,并显著提高了纳米粒子在肿瘤组织中的积累。
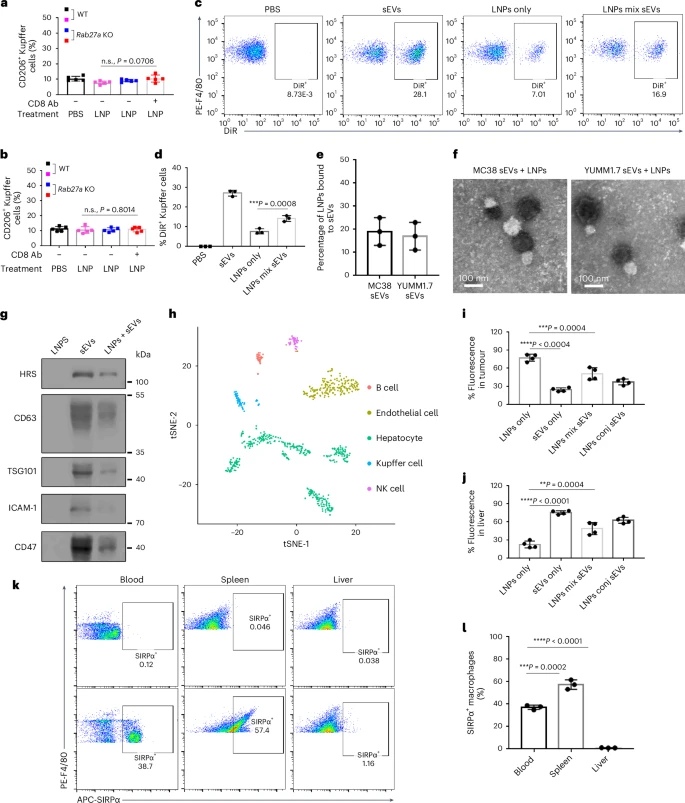
而当研究人员将编码肿瘤抑制和促炎蛋白的信使RNA(mRNA)与Rab27a小干扰RNA共封装于脂质纳米粒子中时,治疗效果得到了显著提升。这一发现不仅证实了sEVs在肿瘤纳米粒子传递中的关键作用,也为开发新的肿瘤治疗策略提供了可能。 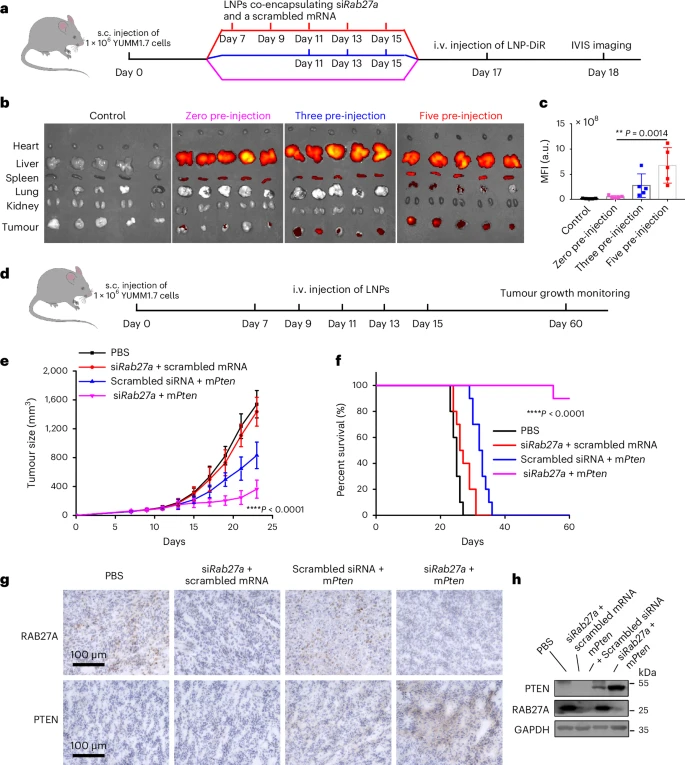
该研究的深远意义在于,发现了外泌体在纳米药物运输中扮演的角色,并提出了一种解决办法以提升药物运输的效率。
参考文献
Gong, N., Zhong, W., Alameh, MG. et al. Tumour-derived small extracellular vesicles act as a barrier to therapeutic nanoparticle delivery. Nat. Mater. (2024). https://doi.org/10.1038/s41563-024-01961-6