Learning what keeps nanomedicines in tumours:AI驱动的纳米药物蓄积预测新突破
在纳米医学领域,一个长期存在的挑战是如何准确预测纳米药物在肿瘤中的蓄积效率。近期,Lammers等研究人员在这一领域取得了重大进展,他们开发的机器学习模型为个性化纳米药物治疗开辟了新的可能性。本文将深入探讨这项研究的意义、局限性以及未来的发展方向。
研究亮点:机器学习模型预测纳米药物蓄积
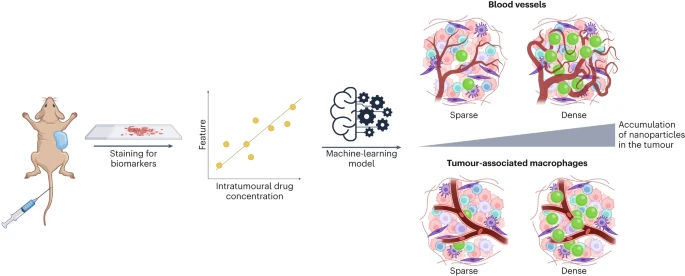
Lammers团队的研究聚焦于识别影响纳米药物在肿瘤中蓄积的关键特征。他们开发的机器学习模型能够分析23种预先选定的肿瘤特征,预测纳米药物的积累效率。这一突破性成果为实现个性化纳米药物治疗策略提供了重要基础。
模型局限性与未来优化方向
尽管该研究取得了显著成果,但专家们指出了几个值得关注的局限性和潜在的改进方向:
细胞类型特异性:当前模型未考虑特定细胞类型对不同纳米药物的吸收情况。例如,化疗药物理想情况下应主要递送至肿瘤细胞,而免疫激活剂则应递送至免疫细胞。
高分辨率组织病理学图像:使用更高分辨率、带有特定细胞类型标记的组织病理学图像进行模型训练,可能会提高预测准确性,并揭示新的细胞类型特异性纳米粒子积累生物标志物。
非侵入性生物标志物:目前的模型需要实际肿瘤组织来测量血管密度和浸润巨噬细胞,这并非总是可行。开发基于影像学或血液样本的替代非侵入性生物标志物将提高该策略的转化相关性。
自监督学习:未来的机器学习模型可以采用自监督学习方式,利用患者肿瘤微环境的蛋白组学、转录组学甚至多重空间数据,以及肝肾功能生物标志物和临床元数据(如性别、年龄、种族和民族),更精确地预测纳米药物在患者体内的积累效率。
展望:迈向精准纳米医学
这项研究为纳米药物的个性化应用开辟了新的可能性。通过持续优化预测模型,我们有望在不久的将来实现以下目标:
- 更精确地预测纳米药物在特定患者肿瘤中的蓄积效率。
- 识别新的纳米药物积累生物标志物。
- 开发非侵入性的预测方法,提高临床应用的可行性。
- 整合多维度数据,实现更全面、准确的预测。
结语
Lammers等人的研究为纳米医学领域带来了新的希望。随着人工智能技术的不断进步和跨学科合作的深入,我们有理由相信,精准、个性化的纳米药物治疗将在不久的将来成为现实,为癌症患者带来更有效、更安全的治疗选择。