【Angew.Chem.】310 倍荧光爆发!NIR-II 探针让胆管手术精准度翻倍
✨文章标题:Protein-Triggered Reassembly of Quinocyanine Nanosheets for Intraoperative NIR-II Cholangiography ✉️作者:Prof. Dr. Yisheng Xu, Prof. Dr. Zhiqian Guo 等 🔗链接:https://doi.org/10.1002/anie.202522772
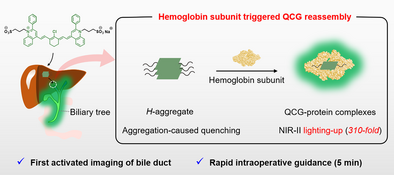
在肝胆外科手术室里,医生面临着一个棘手的难题:胆管就像缠绕在肝脏上的细水管,直径不足 3 毫米,却要在复杂的组织间隙中精准识别。传统手术中,哪怕毫米级的误伤,都可能导致胆汁泄漏、肝损伤等严重并发症。而临床常用的ICG 荧光探针,就像 “长亮的手电筒”,在照亮胆管的同时,也让肝脏背景发亮,医生很难快速区分目标与干扰。
如今,华东理工大学团队的一项研究彻底改变了这一现状。他们开发出一种名为喹菁绿(QCG) 的 NIR-II 探针,凭借 “蛋白触发重组” 的神奇机制,实现了310 倍的荧光爆发,让胆管在手术中清晰 “发光”,胆囊与肝脏的信号比达到25 倍,远超传统探针的 1.8 倍。这项发表在《德国应用化学》的成果,为精准外科手术打开了新大门。
一、手术导航的 “痛点”:为什么传统探针不好用?
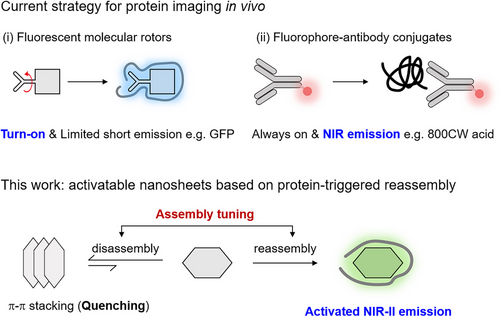
要理解 QCG 的突破性,首先得明白术中荧光成像的核心需求。外科手术中的荧光导航,本质是给医生装一双 “透视眼”,让目标组织(比如胆管)在术中实时显影,避免误伤。但这双 “透视眼” 要好用,必须满足两个关键条件:一是 “看得清”(高对比度),二是**“不迷路”(高特异性)**。
传统的荧光探针却很难兼顾这两点。目前临床唯一获批的胆管成像探针 ICG,属于 “常开型” 探针 —— 从注射进体内开始就持续发光。虽然它能结合胆汁蛋白增强信号,但肝脏组织也会吸收并发出荧光,形成强烈的背景干扰。就像在白天开手电筒,光线被环境光掩盖,很难看清目标。数据显示,ICG 的胆囊 - 肝脏信号比仅1.8 倍,医生在手术中需要反复辨认,不仅延长了手术时间,还存在误判风险。
更关键的是,人体组织中的很多生物靶点(比如胆管相关的蛋白)都是 “化学惰性” 的 —— 它们结构稳定,很难被传统探针 “激活”。之前的两种主流解决方案都有明显短板:分子转子探针虽然能 “遇靶发光”,但发射波长太短,容易被手术灯光干扰;荧光团 - 抗体偶联物能在近红外区工作,却依然是 “常开” 模式,背景荧光问题无法解决。
手术中对精准导航的需求越来越迫切,尤其是在腹腔镜胆囊切除术、肝移植等复杂手术中,医生急需一种 “平时不亮,遇胆管才亮” 的智能探针。QCG 的出现,正好命中了这个行业痛点。
二、核心突破:QCG 探针的 “开关魔法”
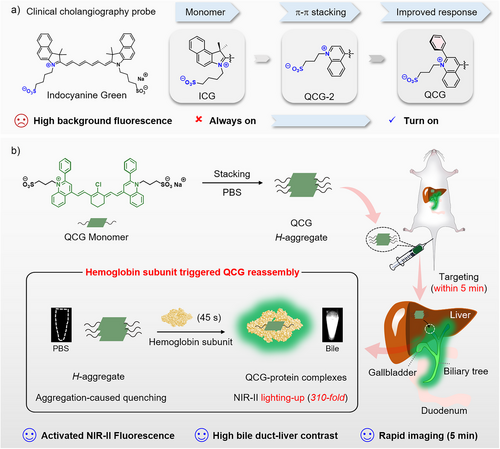
QCG 之所以能实现 310 倍的荧光爆发,关键在于它的 “蛋白触发重组” 机制 —— 这是一种全新的探针设计思路,把传统认为的 “短板” 变成了 “优势”。
首先得解释一个关键概念:NIR-II 荧光成像。我们可以把它类比成 “手术中的夜视仪”,其发射波长在 900-1700 纳米之间,能穿透更深的人体组织,而且不会被手术灯光干扰,成像清晰度远超可见光和近红外 I 区(700-900 纳米)。但 NIR-II 探针的设计难度很大,既要保证发光强度,又要实现 “按需激活”。
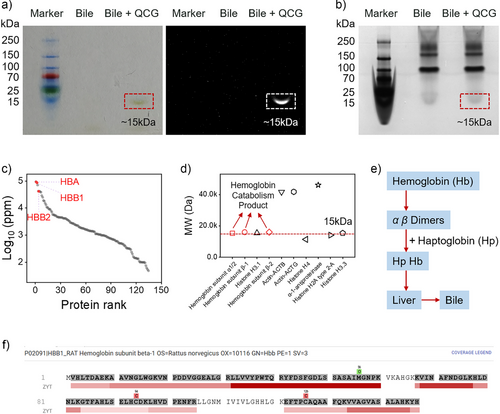
QCG 的设计团队采用了 “三步走” 的分子工程策略。第一步,打造 “平面化” 的染料分子。他们以临床常用的 ICG 为基础,改造出喹啉衍生的七甲川菁染料,这种分子结构具有极强的平面性和刚性,就像一片片规整的 “小薄片”。第二步,让 “小薄片”自发组装。在水溶液中,这些平面分子会通过π-π 堆积作用(可以理解为 “分子间的磁力”),自动聚集形成纳米片。此时,染料的荧光会被完全淬灭,就像按下了 “关灯” 键,避免了在非目标组织中发光产生背景干扰。第三步,设计 “特异性开关”。当这些纳米片进入胆汁后,胆汁中的血红蛋白亚基会成为 “钥匙”,触发纳米片解体并重组 —— 染料分子与血红蛋白亚基结合,形成均匀的球形复合物,荧光被瞬间激活,相当于按下了 “开灯” 键。
这个过程就像一场精密的 “分子舞蹈”:平时染料分子抱团 “休眠”,一旦遇到胆汁中的特定蛋白,就立刻解散重组并 “发光报信”。而这把 “钥匙”—— 血红蛋白亚基,是肝脏分解血红蛋白后的产物,会随胆汁排出,成为胆管特有的 “身份标识”,这也保证了 QCG 的特异性。
与传统方法相比,QCG 的创新点十分突出。分子转子探针受限于结构,发光波长只能到 450-700 纳米,容易被手术灯干扰;荧光团 - 抗体偶联物能在近红外区工作,但 “常开” 模式导致背景信号高。而 QCG 既实现了 NIR-II 区的深穿透成像,又通过 “组装 - 重组” 机制解决了特异性激活问题,相当于给探针装了 “智能导航 + 自动开关”。
三、数据说话:QCG 到底比传统探针强多少?
实验室里的创新,最终要靠数据验证。研究团队通过一系列对比实验,用硬核数据证明了 QCG 的颠覆性优势,每一组数据都直指临床痛点。
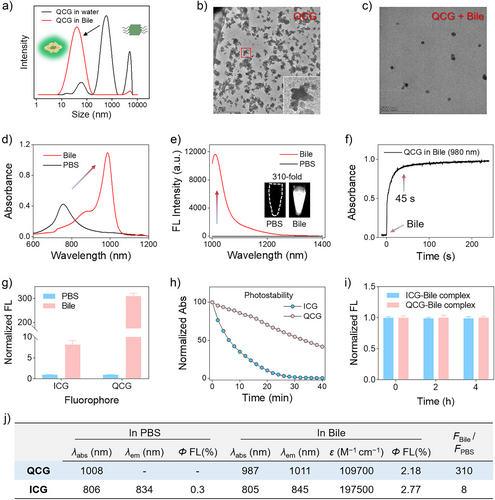
首先是核心的荧光增强效果。在 PBS 溶液中,QCG 形成纳米片后几乎不发光;而进入胆汁后,与血红蛋白亚基结合重组,在 1011 纳米处的荧光强度飙升310 倍。作为对比,传统 ICG 在胆汁中仅能实现 8 倍荧光增强。310 倍的差距意味着什么?相当于把手机屏幕亮度从 1 格调到 310 格,在复杂的手术环境中,医生能一眼看清胆管的位置和形态。
其次是成像对比度。这是手术导航最关键的指标之一。在小鼠模型中,注射 QCG 后 30 分钟,胆囊与肝脏的信号比达到24.8,接近 25 倍;而 ICG 的这一比值仅为 1.8。这意味着,使用 QCG 时,胆囊的荧光信号是肝脏背景的 25 倍,就像在黑夜中看到一盏明亮的灯;而 ICG 则像是在黄昏中看一盏台灯,边界模糊难辨。这种高对比度,能让医生在分离组织时精准避开胆管,大幅降低手术风险。
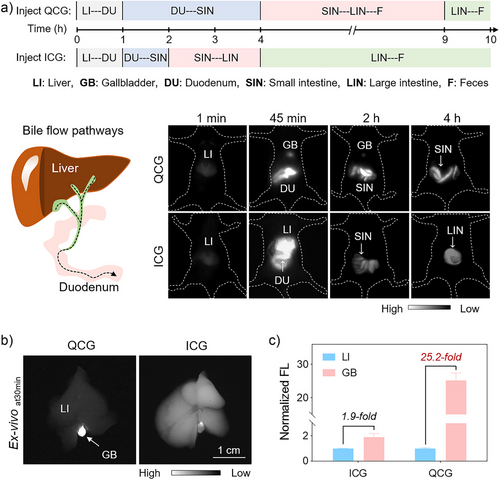
空间分辨率同样表现出色。通过高斯拟合计算,QCG 的成像分辨率达到487 微米,而 ICG 仅为 808 微米。分辨率越高,意味着能看清更细小的胆管分支。人体的肝内胆管直径最小可达 1 毫米,QCG 能清晰勾勒出这些细小分支的走向,这对于肝移植、肝切除等复杂手术至关重要。
还有两个关键的临床指标:响应速度和稳定性。QCG 与胆汁接触后,45 秒内就能完成重组并激活荧光,注射到体内后5 分钟内就能清晰显示胆管树,满足手术中快速导航的需求。而 ICG 需要更长时间代谢,且背景信号消退慢。在光稳定性测试中,QCG 在持续照射下的半衰期约为34 分钟,是 ICG(6 分钟)的 5 倍多。手术过程可能长达数小时,探针的高稳定性能保证全程成像清晰,不会出现中途 “熄灯” 的情况。
生物相容性和代谢安全性也通过了严格验证。细胞毒性实验显示,即使 QCG 浓度高达 80μM,对细胞的毒性依然极小。在小鼠体内,QCG 通过肝脏摄取后,随胆汁排出,24 小时后除了大肠有微弱信号外,其他器官均无残留,不会在体内蓄积,符合临床应用的安全要求。
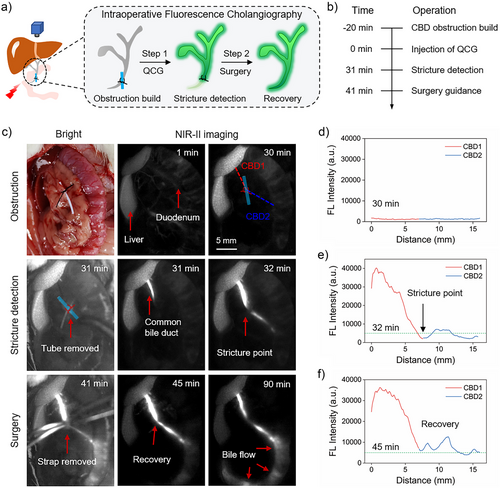
除了基础性能,QCG 还在多个临床场景中展现出实用价值。在胆管梗阻模型中,完全梗阻时胆管无荧光信号,移除梗阻物后,荧光迅速恢复,医生能实时判断胆管是否通畅;在胆管狭窄模型中,QCG 能精准定位狭窄部位,帮助医生制定手术方案;甚至能检测到术中急性胆漏,避免术后并发症。这些场景都是临床中常见的难题,QCG 的出现为解决这些问题提供了新工具。
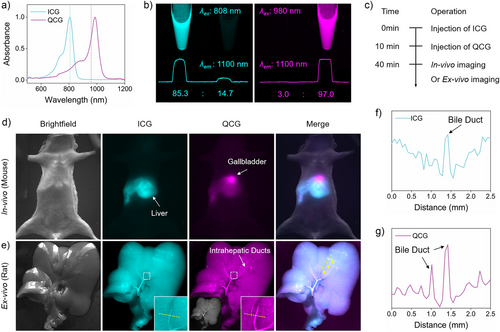
更令人惊喜的是,QCG 还能与 ICG 搭配实现双色成像。ICG 在 808 纳米激发下主要显示肝脏和血管,QCG 在 980 纳米激发下专门显示胆管,两者激发波长相差 150 纳米,几乎没有信号串扰。在大鼠模型中,双色成像能同时清晰勾勒出肝脏实质、血管和胆管的形态,就像给医生提供了一张 “三维解剖地图”,让手术规划更精准。
四、应用展望:不止于胆管手术的未来
QCG 的突破,不仅解决了胆管手术导航的痛点,更为激活型 NIR-II 探针的设计提供了通用思路。但客观来看,这项技术目前还处于动物实验阶段,要走向临床还需要克服一些挑战。比如,需要在更大的动物模型中验证长期安全性和有效性,还要优化探针的制备工艺,降低生产成本,同时建立标准化的临床使用流程。
不过,其潜在的应用场景已经十分广阔。除了胆管手术,基于 “蛋白触发重组” 策略,可以设计针对其他惰性蛋白靶点的探针,用于肿瘤手术导航、血管成像、神经外科手术等多个领域。比如,针对肿瘤特异性表达的蛋白设计探针,就能实现肿瘤组织的精准显影,帮助医生彻底切除肿瘤并保留正常组织;在神经外科手术中,精准显示神经纤维的走向,能避免损伤重要神经。
在肝胆外科领域,QCG 未来可能成为腹腔镜胆囊切除术、肝移植、肝叶切除等手术的常规导航工具。对于胆管狭窄、胆漏等并发症的诊断,QCG 也能提供实时、无创的检测手段,减少患者的检查痛苦和医疗费用。此外,双色成像技术还能用于研究肝胆疾病的病理机制,为药物研发提供新的可视化工具。
从行业发展来看,QCG 的设计思路打破了传统激活型探针的结构限制。之前的激活型探针多依赖共价键断裂等化学反应,而 “蛋白触发重组” 依赖非共价相互作用,更温和、更具特异性,也更容易适配不同的蛋白靶点。这种通用策略,可能会催生出一系列针对不同疾病的 NIR-II 探针,推动精准外科手术的全面发展。
结语
一场成功的外科手术,既需要医生的精湛技艺,也离不开先进工具的辅助。QCG 探针的出现,就像给肝胆外科医生配备了一把 “精准导航的手术刀”,310 倍的荧光爆发、25 倍的成像对比度,让曾经难以分辨的胆管清晰显影,为手术安全增添了重要保障。
更重要的是,这项研究提出的 “蛋白触发重组” 策略,为解决化学惰性蛋白靶点的激活成像问题提供了新方案。从实验室的分子设计到动物模型的成功验证,QCG 的每一步突破都朝着临床应用迈进。未来,随着技术的不断优化和临床验证的推进,我们有理由相信,这种智能探针将走进更多手术室,让精准外科手术惠及更多患者,也为近红外荧光成像技术开辟更广阔的发展空间。