【Angew.Chem.】仅需一次治疗,治愈率达 37.5%!这种 595 Da 的小分子光敏剂,竟能让致死性转移癌“消声匿迹”
✨文章标题:Seamlessly Overcoming Biological Barriers with a Small Photosensitizer to Treat Metastatic Tumors with Photodynamic Therapy ✉️作者:Luis G. Arnaut, Lígia C. Gomes-da-Silva 等 🔗链接:https://doi.org/10.1002/anie.202509121
[!summary] 精简版
直击痛点: 传统光敏剂体积大、难以渗透进致密的肿瘤组织,且难以诱导足够的免疫反应来抑制肿瘤转移。而癌症致死的主因正是占总数 90% 的转移性癌症。
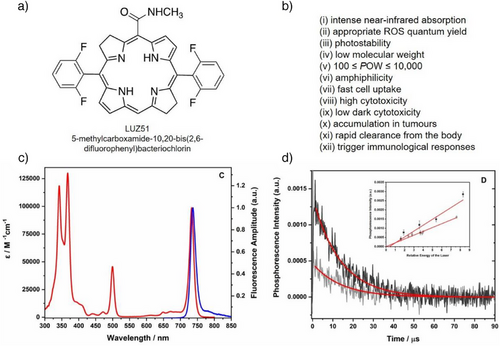
创新武器 LUZ51: 这是一种分子量仅为 595 Da 的小型细菌叶绿素衍生物。它拥有近红外强吸收、高光稳定性以及极佳的“两亲性”(既亲水又亲油)。
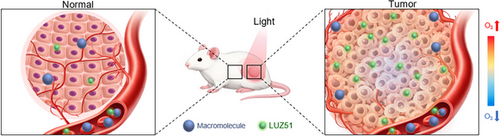
“穿墙”机制: 凭借小身材和独特结构,LUZ51 无需复杂载体,仅靠 被动扩散 就能在几分钟内迅速穿过生物屏障,进入癌细胞内部。
惊人疗效:
在极低光照剂量下,对多种癌细胞展现出 纳摩尔级别(5-15 nM) 的杀伤力。
在小鼠实验中,它成功治愈了 57% 的 CT26 结肠癌模型。
更具突破性的是,对于极难对付的、已发生转移的 4T1 原位乳腺癌,仅需一次治疗即可实现 37.5% 的治愈率,并显著抑制肺转移。
安全性极高: 血液半衰期仅 82 分钟,代谢极快,不会引起传统光动力疗法常见的皮肤光毒性副作用。
系统免疫激活: 它不仅是局部的“精准爆破”,还能诱导 免疫原性细胞死亡(ICD),激活 T 细胞产生长期的免疫记忆,让身体学会自己抵抗癌症复发。
在人类与癌症的长达一个世纪的“拉锯战”中,我们最恐惧的敌人往往不是最初发现的那个肿块,而是那些悄无声息、像种子一样播撒到全身的“逃兵”——转移性肿瘤。统计数据冰冷且残酷:在成年癌症患者中,约 90% 的死亡并非死于原发瘤,而是死于这些如影随形的转移病灶。
长期以来,临床医生面对转移癌,往往只能寄希望于化疗或免疫疗法这种“全城搜捕”式的系统方案,而光动力疗法(PDT)则一直被视为一种“定点爆破”的局部疗法。然而,近期发表在化学顶级期刊《德国应用化学》(Angewandte Chemie International Edition)上的一项突破性研究彻底打破了这一成见。
来自科英布拉大学的研究团队设计出一种名为 LUZ51 的新型小分子光敏剂。它不仅能在极低剂量下实现局部肿瘤的“物理消除”,更能通过激活人体自身的免疫系统,对那些远端转移的癌细胞发动一场“全面反击”。最令人震撼的是,在极难对付的、已经发生转移的 4T1 原位乳腺癌模型中,仅需单次 PDT 治疗,就实现了 37.5% 的完全治愈率。
“穿墙术”:595 Da 带来的降维打击
要理解 LUZ51 为什么如此厉害,我们得先聊聊目前癌症药物面临的“中年危机”——分子肥胖(Molecular Obesity)。
许多新型药物为了追求多功能和特异性,结构变得越来越复杂,分子量也随之飙升。但在充满敌意的肿瘤微环境(TME)中,这些“大块头”步履维艰。肿瘤内部那致密的细胞外基质、异常升高的组织间压力,就像一道道厚重的围墙,将药物挡在门外。
研究人员做出了一个违背“常规智慧”的决定:化繁为简。
他们设计出的 LUZ51 是一种小型细菌叶绿素衍生物,分子量仅为 595 Da。这个数字在光敏剂界堪称“精瘦”。与临床常用的其他光敏剂相比,它就像是一个身轻如燕的特种兵,能够利用一种简单的“被动扩散”机制,几乎不受阻拦地穿过生物屏障。
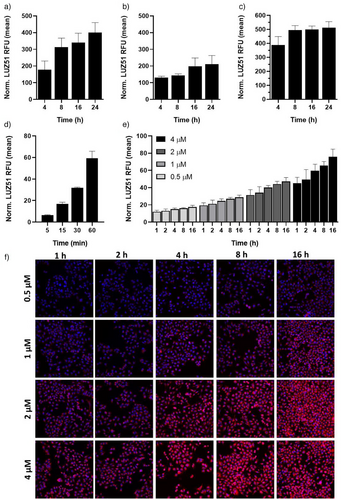
研究团队通过精密的同位素追踪和动力学实验证实,LUZ51 在进入人体后,短短 5 分钟内就能与癌细胞建立关联,1 小时内就能在细胞内部达到极高的浓度。
这种“穿墙术”的核心秘诀在于 LUZ51 达到了一个近乎完美的“两亲性甜点”。它既能溶于水随血液循环,又能轻松溶入细胞膜的脂质双分子层。这意味着它不需要复杂的纳米包装,不需要等待漫长的内吞过程,直接就能“闪现”进敌军内部,占据内质网和高尔基体等核心战略位置。
深层爆破:近红外光下的纳摩尔级绝杀
光动力疗法(PDT)的原理其实很像一场“光学陷阱”:光敏剂进入细胞后保持沉睡,只有当特定波长的光线照射时,它才会迅速吸收能量,将周围的氧气转化成破坏力极强的活性氧(ROS),从而从内部炸毁癌细胞。
但传统 PDT 有两个致命弱点:一是光穿不透组织,二是光敏剂“火力”不足。
LUZ51 通过以下三项核心物理属性完美解决了这些问题 :
极强的近红外吸收: 它的吸收峰位于 733 nm,处于组织透明度最高的“生物光学窗口”。这意味着治疗光线可以像穿透玻璃一样,深入组织内部杀灭大型肿瘤。其消光系数高达 ,是传统光敏剂 Photofrin 的近 80 倍。
恐怖的杀伤效率: 在 1 的极低光照剂量下(相当于普通手电筒照一会儿),LUZ51 对多种癌细胞的半数有效浓度()竟然达到了 5-15 nM。这是什么概念?相当于在游泳池里滴几滴药水,就能通过光照清空池子里的癌细胞。
极高的安全性: LUZ51 具有高达 25,000 的“光治疗指数”。在没有光照的情况下,它几乎没有任何毒性,即使浓度达到 也非常安全。
更为惊人的是它的代谢速度。传统光敏剂常让患者在治疗后数周内不能见光,否则会发生严重的皮肤灼伤。而 LUZ51 的血液半衰期仅为 82 分钟,24 小时后皮肤中的残留量极低,小鼠甚至可以直接在模拟阳光下奔跑而毫发无伤。
数据解析:在“噩梦级”模型中的逆天表现
为了验证 LUZ51 的实战能力,研究团队选取了两种极具代表性的动物模型。
1. CT26 结肠癌模型:从治愈到免疫记忆
首先是常规的 CT26 结肠癌。实验显示,当光敏剂剂量仅为 0.10 mg/kg 时,结合 40 的光照,57% 的小鼠肿瘤彻底消失,并实现了长期无瘤生存。
但这还不是最精彩的部分。研究人员在这些治愈后 45 天的小鼠身上,重新植入了同种癌细胞(这一过程称为“二次挑战”)。结果发现,43% 的治愈小鼠成功排斥了新肿瘤的生长。这表明 LUZ51 引发的不仅仅是局部物理爆破,它还教会了小鼠的免疫系统如何识别并攻击这种癌症,形成了宝贵的 免疫记忆。
2. 4T1 原位乳腺癌:攻克转移癌的“滑铁卢”
真正的挑战来自 4T1 原位乳腺癌模型。在科研界,这个模型被称为“噩梦”,因为它与人类晚期三阴性乳腺癌高度相似:血管贫乏、间质压力大、极度抑制免疫,且一旦肿瘤长到 5 mm,肺部转移几乎是板上钉钉。
历史上,无论是临床常用光敏剂 Photofrin 还是新一代的 Redaporfin,在这个模型面前都折戟沉沙,治愈率几乎为零。
然而,LUZ51 交出了一份令人瞠目结舌的答卷:
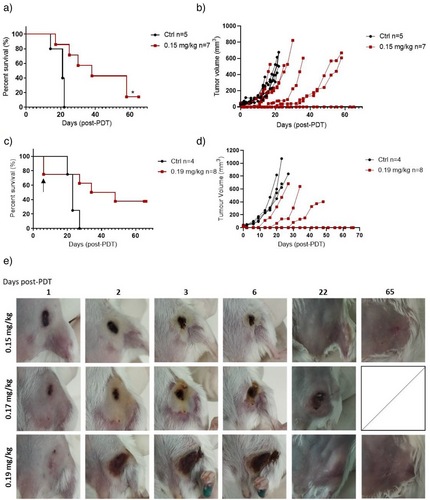
生存奇迹: 随着药物剂量提升至 0.19 mg/kg,在单次治疗后,37.5% 的小鼠达到了临床治愈标准。
抑制转移: 磁共振成像(MRI)监测显示,未受治疗的小鼠在第 21 天肺部就长满了巨大的转移结节。而 LUZ51 治疗组的小鼠,直到第 42 天才观察到微小的转移迹象,且治愈小鼠的肺部始终保持洁净。
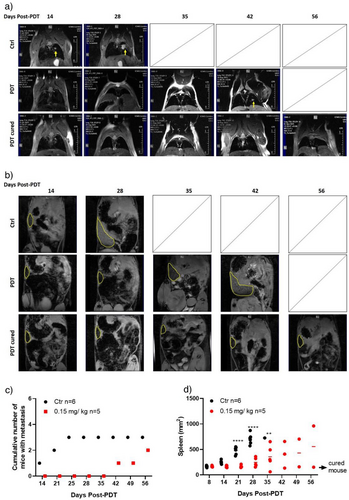
Figure 9 展示了这种对比:在未治疗组中,由于严重的肿瘤负荷,小鼠的脾脏肿大到了惊人的程度;而在 LUZ51 治疗成功的案例中,小鼠的脾脏大小和形态完全恢复了正常,肺部转移病灶消失殆尽。
机制拆解:从“物理爆破”到“系统免疫”
为什么一个局部治疗能管到全身?秘密在于 LUZ51 诱导的一种特殊死亡方式——免疫原性细胞死亡(ICD)。
在 LUZ51 的精准打击下,癌细胞在临死前会释放出一系列“求救信号”(如钙网蛋白暴露、ATP 释放等)。这些信号就像给免疫系统打了一剂强力兴奋剂,将原本处于“休眠”状态的 T 细胞唤醒,并引导它们寻找并消灭全身各处的同类癌细胞。
研究团队为了证实这一点,进行了一场巧妙的对比实验:他们在缺乏 T 细胞的“裸鼠”身上重复了治疗。结果发现,虽然光敏剂依然能通过物理爆破延长裸鼠的寿命,但没有一例实现治愈。而在拥有正常免疫系统的野生型小鼠中,治愈率则大幅上升。
这实锤了 LUZ51 的疗效:物理清除为引,免疫反击为核。
总结与展望:PDT 的新时代已经开启?
尽管这项研究在实验室中取得了辉煌的战果,但作为一个严谨的科技自媒体,我们也必须客观地看待其局限性与未来。
当前的挑战与局限:
光穿透深度: 虽然近红外光能够穿透数厘米的组织,但对于人体深部器官(如肝脏中心或深部腹腔)的肿瘤,依然需要借助内窥镜或光纤插针技术来输送光能。
人体转化: 实验室小鼠的肿瘤环境与真实的人类患者仍有差异。尽管 LUZ51 在安全性指标上表现优异,但其在复杂人体环境下的药代动力学仍需更大规模的临床前及临床试验验证。
未来的社会影响: LUZ51 的出现可能从根本上重塑我们对光动力疗法的认知。它不再仅仅是皮肤病或浅表癌的配角,而是具备了作为一线抗癌利器的潜力,特别是对于那些传统化疗难以渗透的致密肿瘤和已经发生转移的晚期癌症。
我们可以预见,在不久的将来,PDT 可能不再被视为一种“局部方案”,而是与免疫检查点抑制剂(PD-1 等)强强联手的“黄金搭档”。通过 LUZ51 的“精准爆破”释放肿瘤抗原,再配合免疫药物撤掉癌细胞的防御伪装,人类或许真的能让那些曾经判了死刑的转移癌患者重获新生。
在这个追求“更复杂、更昂贵”医疗技术的时代,LUZ51 用它的简练、高效告诉我们:有时候,解决最复杂问题的答案,就藏在最简单的设计之中。