【Angew.Chem.】 亮度飙升310%!中国科学家首创“共价锁”技术,跨越血脑屏障,1800微米深处精准“狙击”脑肿瘤
✨文章标题:Covalent Bond Locking in Semiconducting Oligomers Boosts Ultrabright NIR-II Luminescence for Deep Brain Theranostics ✉️作者:Ke Wang, Jun Qian, Shengliang Li 等 🔗链接:https://doi.org/10.1002/anie.7337664
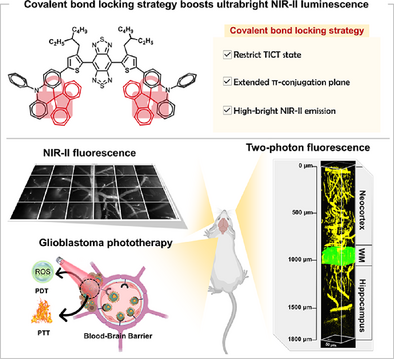
[!summary]
1. 研究背景与挑战
目前,近红外二区窗口(NIR-II, 1000-1700 nm) 荧光成像因其组织穿透深、散射低、自动荧光干扰小等优点,成为脑部疾病精准诊疗的热点。然而,现有的 NIR-II 荧光分子面临一个核心“鱼与熊掌不可兼得”的难题:亮度不足。荧光分子的亮度由量子产率(QY)和摩尔消光系数()共同决定,但两者之间往往存在相互制约的平衡,导致高性能荧光探针的设计极其困难。此外,血脑屏障(BBB) 的存在严重阻碍了药物进入大脑病灶。
2. 核心创新点:共价键锁定(CBL)策略
研究团队提出了一种共价键锁定(CBL)策略。他们通过将扭曲的二苯胺(TPA)单元通过刚性的螺环结构进行锁定,设计了新型螺环荧光分子(STB-1 和 STB-2)。
物理机制: 这种锁定结构能够有效抑制扭曲分子内电荷转移(TICT) 态的形成,减少非辐射能量损耗。
性能提升: 相比于未锁定的对照分子(TB-1 和 TB-2),STB-2 的亮度提升了 3.1 倍,纳米颗粒(NPs)状态下的量子产率达到了 4.2%,摩尔消光系数显著提高。
3. 技术突破与应用成果
多尺度脑血管成像: 借助 STB-2 NPs 的超高亮度,实现了目前报道中视野最大(2100 μm × 1680 μm) 的单光子荧光(1PF)脑血管造影。
极限深度探索: 在 1700 nm 飞秒激光激发下,实现了深度达 1800 μm 的双光子荧光(2PF)深层大脑成像,打破了传统深度限制。
协同治疗: STB-2 NPs 具有极佳的光热转换效率(63.5%)和产生超氧阴离子及羟基自由基的能力,可同时进行光热治疗(PTT)和光动力治疗(PDT)。
跨越屏障: 通过在纳米颗粒表面修饰载脂蛋白 E(ApoE),使其能够有效穿过血脑屏障,精准靶向脑胶质瘤。在小鼠实验中,该疗法成功抑制了肿瘤生长,将中位生存期延长至 30 天。
4. 结论与意义
该工作不仅为设计高亮度近红外荧光分子提供了一套通用的分子工程学方法,还构建了一个集高分辨率成像与高效治疗于一体的纳米平台,为深层脑部疾病的精准诊疗铺平了道路。
从脑部诊疗的“深水区”到革命性的技术突破
人类大脑被誉为宇宙中最复杂的器官,其内部交织着数以亿计的神经元和密集的微血管网络,形成了一个高度动态且极其复杂的微环境 。长期以来,探索大脑深处的病理变化一直是神经科学领域的“终极挑战” 。虽然临床上常用的磁共振成像(MRI)和计算机断层扫描(CT)等手段已经普及,但它们在空间分辨率和实时性上的局限,使得微观层面的病变观察依然如隔岸观火 。为了更清晰地“看透”大脑,科学家们将目光投向了近红外二区(NIR-II, 1000-1700 nm)荧光成像技术。这一波段具有组织穿透力强、散射低以及自动荧光干扰小等显著优势,被认为是深层组织可视化和精准诊疗的利器 。
然而,在实际应用中,一个巨大的瓶颈始终制约着这项技术的发展:缺乏足够亮度的荧光分子 。荧光分子的亮度由量子产率(QY)和摩尔消光系数共同决定,但传统的分子设计往往难以兼顾两者,导致成像分辨率不足,难以捕捉细微的解剖细节 。即便是有着近 70 年临床应用史的吲哚氰绿(ICG),也因为稳定性差和组织穿透力有限,难以在深层大脑成像中担当大任 。此外,血脑屏障(BBB) 这一人体自带的“防御工事”,也让绝大多数诊断和治疗药物被挡在门外,极大地增加了脑部疾病治疗的难度 。
面对这些重重阻碍,来自苏州大学、浙江大学和深圳大学等机构的联合研究团队提出了一种名为共价键锁定(CBL) 的创新策略 。这项研究不仅成功开发出了亮度大幅提升的新型荧光分子,还实现了跨越血脑屏障的深层脑肿瘤精准诊疗 。这一成果发表在化学领域的顶尖期刊《德国应用化学》上,标志着我们在攻克深层大脑诊疗难题的道路上迈出了关键一步 。
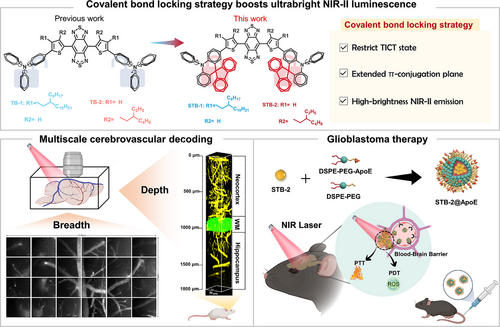
核心方法与技术细节:如何给分子加一把“硬锁”
为了理解共价键锁定策略的精妙之处,我们首先需要了解荧光分子亮度背后的“能量窃贼”——扭曲分子内电荷转移(TICT) 态 。在很多有机荧光分子中,其分子结构往往包含多个可以相对旋转的单元。当分子吸收光子进入激发态后,这些单元可能会发生剧烈的旋转,从而进入一个能量极低的非辐射状态,即 TICT 态。这就好比一个正在旋转的陀螺,如果内部结构不稳产生剧烈晃动,能量就会在摩擦和震动中白白损耗,导致发光效率大幅下降 。
研究团队的核心创新在于,他们发明了一种巧妙的“分子加固”方法,将原本容易发生旋转的单元通过刚性的螺环结构牢牢锁定 。具体来说,他们将传统的三苯胺(TPA)供体单元改进为螺环三苯胺(spiro-TPA),并通过共价键锁定策略将其融入半导体低聚物的骨架中 。这种设计就像是在分子关节点上安装了一把性能卓越的“刚性锁”,极大地限制了分子内部的自由旋转和扭曲 。
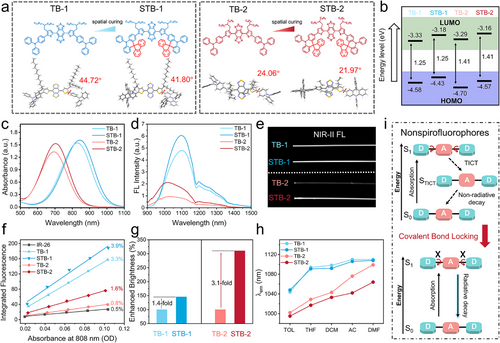
通过密度泛函理论(DFT) 计算,科学家们从量子力学层面验证了这把“锁”的威力 。结果显示,在 STB-1 和 STB-2 这两款新型分子中,锁定后的供体与噻吩单元之间的二面角显著减小,分子的共轭平面性和刚性得到了极大提升 。更重要的是,计算结果证实这种锁定结构能够显著提高激发态的旋转势垒,这意味着分子形成 TICT 态的倾向被有效抑制了 。能量不再通过分子的晃动而流失,而是更高效地转化为荧光发射,从而为超亮荧光的产生奠定了坚实的分子结构基础 。
除了解决“发光效率”问题,这把“锁”还通过优化分子能量等级,提升了分子的摩尔消光系数 。实验数据显示,STB-1 和 STB-2 在 808 纳米处的吸收能力显著强于未锁定的对照分子 TB-1 和 TB-2 。这意味着这些分子能够更贪婪地吸收激光能量,并将其转化为耀眼的荧光。通过这种“多管齐下”的分子工程手段,研究团队成功在同一分子内实现了高量子产率和高消光系数的平衡,突破了传统荧光分子设计的局限性 。
数据背后的创新与颠覆性:从 3.1 倍亮度到 1800 微米的深层奇迹
在实验室测试中,共价键锁定策略展示了令人震撼的性能提升。首先是纯度极高的荧光亮度增强:STB-1 和 STB-2 的整体亮度分别比未锁定的对照分子提高了 1.4 倍和 3.1 倍 。特别是在 STB-2 分子上,其量子产率(QY)在四氢呋喃溶液中达到了 1.6%,是对应未锁定分子 TB-2 的整整两倍 。这一数据直接证明了“分子加锁”对于抑制能量损耗的绝对有效性 。
为了让这些亮眼的分子能够在复杂的生物体内工作,研究人员利用纳米沉淀技术将其封装在两亲性聚合物中,制备成了 CBL 纳米颗粒(NPs) 。令人惊喜的是,当 STB-2 形成纳米颗粒后,由于分子间强烈的 π-π 相互作用,其性能进一步爆发:其近红外二区荧光量子产率跃升至 4.2%,摩尔消光系数也保持在极高水平 。在与目前市面上公认的高性能荧光分子的横向对比中,STB-2 NPs 的整体亮度表现位居第一梯队,展现出了极强的国际竞争力 。
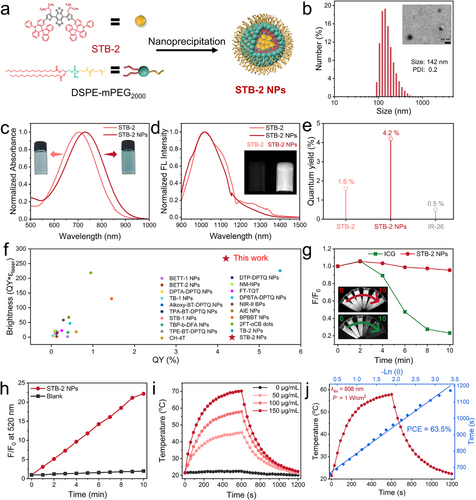
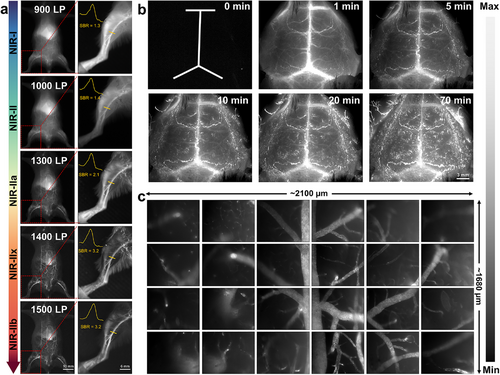
更让医学界感到振奋的是 STB-2 NPs 在活体成像中的表现。在小鼠脑血管造影实验中,凭借超高的亮度,该纳米颗粒实现了视野范围高达 2100 μm × 1680 μm 的超大范围成像 。这是目前已报道的、通过高倍荧光共聚焦显微成像获得的视野最大的脑血管图谱,清晰地展现了大脑内部细如发丝的毛细血管网络 。相比于临床常用的 ICG,STB-2 NPs 不仅清晰度更高,稳定性也更胜一筹,在连续激光照射下依然能保持稳定的信号,为长时程的监测提供了可能 。
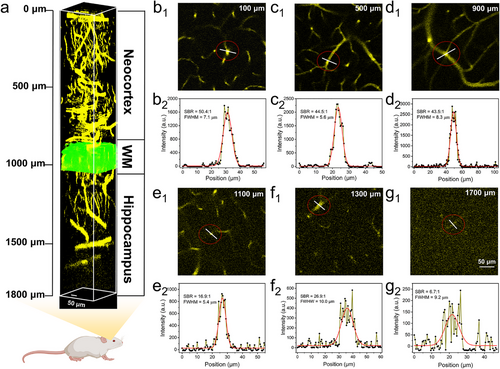
然而,真正的“重头戏”在于双光子荧光(2PF)成像 。在 1700 纳米超短脉冲激光的激发下,STB-2 NPs 展现出了极高的双光子吸收截面 。这一特性允许科学家以极高的空间分辨率深入大脑皮层下方,跨越白质,直达海马体 。通过三维重建技术,研究团队成功获取了深度达 1800 微米 的深层脑血管影像 。这一深度已经接近了光学成像在生物组织中的物理极限,为观察深层大脑的细微病变开辟了前所未有的窗口 。
除了卓越的成像能力,这种纳米颗粒还是一位全能的“特种战士”。实验显示,STB-2 NPs 具有极高的光热转换效率(63.5%),在激光照射下能迅速升温,利用热量消灭肿瘤 。同时,它还能产生包括超氧阴离子和羟基自由基在内的活性氧(ROS),通过光动力疗法(PDT)从内部瓦解癌细胞 。这种光热/光动力双模治疗(PTT/PDT) 机制,赋予了 STB-2 NPs 强大的肿瘤杀伤能力 。
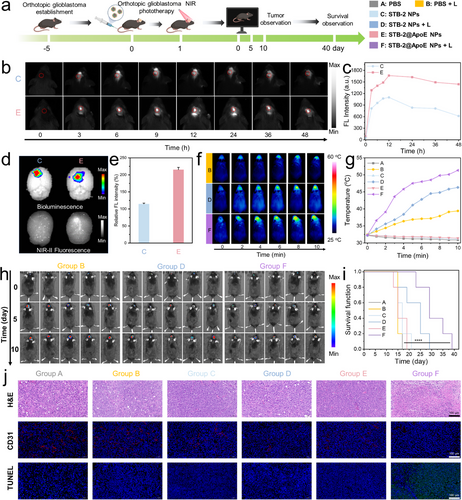
为了解决血脑屏障这一难题,研究团队在纳米颗粒表面修饰了载脂蛋白 E(ApoE) 。这种修饰使得纳米颗粒能够像拥有了“通行证”一样,高效地穿透血脑屏障并精准富集在脑胶质瘤区域 。在原位脑胶质瘤小鼠模型中,STB-2@ApoE NPs 展示了卓越的治疗效果。相比于对照组,接受联合治疗的小鼠肿瘤生长得到了极显著抑制,其中位生存期延长至 30 天,远超其他单一或未修饰的治疗组 。术后的病理分析也证实,治疗诱导了肿瘤细胞的大规模凋亡,且对心脏、肝脏等主要器官没有明显的毒副作用,表现出了良好的生物安全性和临床转化潜力 。
应用展望、局限性与未来路线图
这项关于共价键锁定(CBL)策略的研究,为近红外二区荧光诊疗领域注入了新的活力。它不仅提供了一种普适性的分子设计思路,即通过物理约束来解锁有机分子的亮度潜力,还通过多学科交叉,构建了一个从基础理论到动物实验再到临床前评估的完整链条 。未来,这种超亮的纳米探针有望在脑部手术导航中大显身手,帮助医生实时、精准地识别肿瘤边界,最大限度地保留正常脑组织 。
当然,从实验室走向临床依然面临挑战。尽管目前的研究证明了该系统具有良好的生物安全性和清除机制,但长期的人体毒理学评估仍不可或缺 。此外,虽然 1800 微米的深度已是巨大突破,但对于体积巨大的成人大脑而言,如何进一步提升成像深度或结合其他穿透力更强的物理手段,仍是科研人员需要攻克的方向。未来的路线图将重点关注如何进一步优化分子的吸收波长,以匹配更廉价、更便携的激光器系统,并探索该平台在阿尔茨海默病、脑卒中等其他重大脑部疾病中的应用可能 。
总之,这项研究通过巧妙的“共价锁”技术,不仅让我们看清了大脑深处的“秘密花园”,更通过跨越血脑屏障的精准打击,为脑部肿瘤患者点亮了新的生命之光。这不仅是化学分子设计的胜利,更是生物医学工程向生命禁区发起的又一次成功冲锋。