【Adv.Mater.】3 个月持续释放 NO 的微孔限域 3D 打印壳–芯支架:重塑糖尿病骨缺损修复微环境的新策略
文章标题:Micropore‐Confined ROS‐Responsive 3D‐Printed Shell‐Core Scaffolds for Long‐Term NO Release to Orchestrate Immunomodulation and Angiogenesis in Diabetic Bone Defect Repair
通讯作者:Yongxiang Luo
文章链接:https://doi.org/10.1002/adma.202521475
文章概要
引言
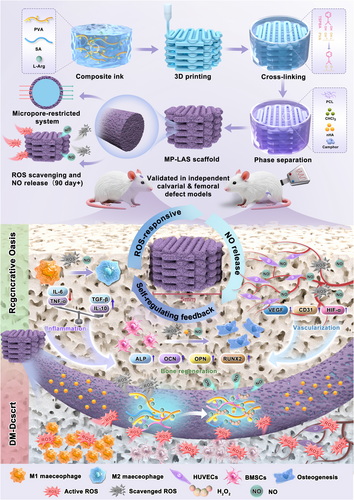
糖尿病患者的骨缺损修复长期受制于高糖环境引发的多重病理因素,包括持续性炎症、过量 ROS(活性氧)、免疫失衡以及血管–成骨耦合受损。这些因素共同造成骨再生能力显著下降,使得传统抗炎、抗氧化或生长因子递送策略难以实现长期、稳定、可控的治疗效果。NO(Nitric Oxide)因其抗炎、促血管生成及调控成骨的多重生物学功能,被视为潜在的治疗手段,但其半衰期极短、易爆发式释放,难以满足糖尿病骨修复所需的长期稳定供给。为解决这一核心难题,作者提出“微孔限域(micropore confinement)”策略,通过构建 3D 打印的 PCL 壳层与 ROS 可降解水凝胶芯层,实现对 NO 生成反应空间的物理限域,从而将传统的“爆发–耗尽式”释放模式转变为“按需、长期、可编程”的释放模式。
主要实验及结论
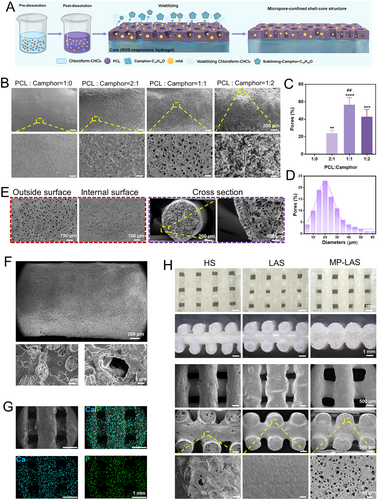
研究首先通过 3D 打印构建 PVA/SA 基水凝胶作为芯层,并利用 TSPBA 交联实现 ROS 响应性;随后在外层包覆含樟脑致孔剂的 PCL 溶液,经溶剂挥发与樟脑升华形成贯通微孔的壳层结构。优化后的 PCL:camphor = 1:1 组可获得约 57% 的表面孔隙率与 20 μm 左右的均一孔径,实现高效物质交换与稳定结构支撑。
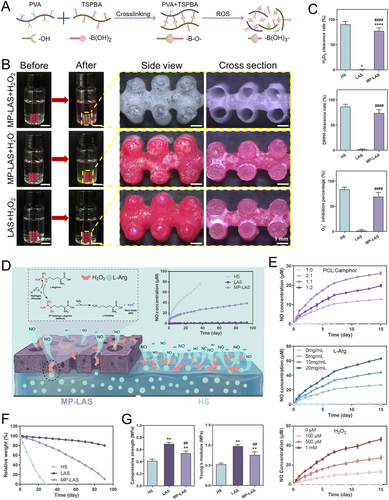
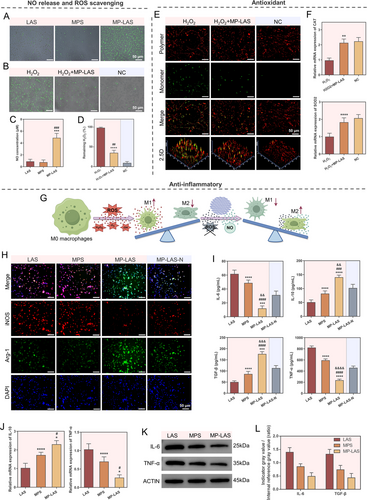
在体外实验中,MP-LAS 支架表现出显著的 ROS 清除能力(H₂O₂、DPPH、O₂•⁻ 清除率均显著高于无孔壳层组),并可在 ROS 刺激下实现长达 90 天的稳定 NO 释放,其半衰期(18 天)为普通水凝胶组的 3 倍。NO 释放速率可通过壳层孔隙度、L-Arg 含量及外界 ROS 浓度精确调控,呈现与病理 ROS 水平正相关的自适应特性。
在细胞层面,MP-LAS 支架可有效降低 ROS 水平、恢复线粒体膜电位、上调抗氧化酶(SOD2、CAT)表达,并通过持续 NO 释放促进巨噬细胞向 M2 型极化,显著降低 TNF-α、IL-6 等炎症因子,提升 IL-10、TGF-β 等抗炎因子表达,构建有利于修复的免疫微环境。
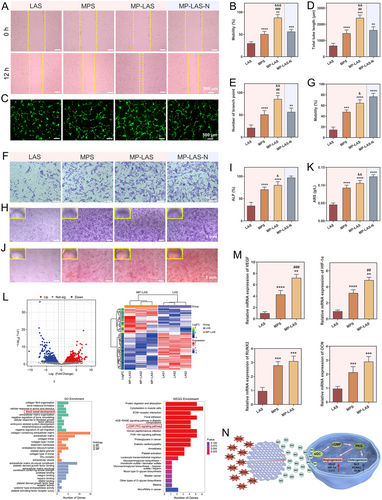
在血管生成与成骨方面,MP-LAS 支架显著提升 HUVECs 迁移、管腔形成能力,并促进 BMSCs 的迁移、ALP 活性及矿化结节形成。转录组分析显示其显著激活 sGC/cGMP/PKG 及 PI3K–Akt 等 NO 相关信号通路,验证其通过血管–成骨耦合促进骨再生的机制。
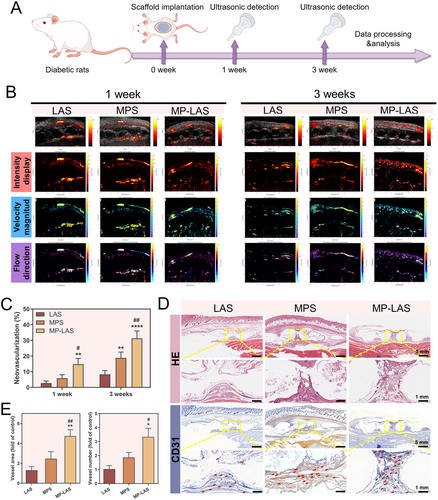
在糖尿病小鼠皮下植入模型中,MP-LAS 支架诱导的血管密度为对照组的 3–4 倍;在糖尿病颅骨与股骨缺损模型中,MP-LAS 组在 12 周时的 BV/TV、BMD、血管密度及成骨标志物表达均显著高于其他组,表现出卓越的骨修复能力,甚至超过正常模型中的 MP-LAS 组,凸显 NO 在糖尿病骨修复中的关键作用。
总结及展望
本研究提出的“微孔限域”策略成功实现了对 NO 生成反应界面的物理调控,使 NO 释放从传统的不可控爆发式转变为可预测、可调控、可自适应的长期释放模式。MP-LAS 支架通过“ROS 清除 + NO 持续生成”双重机制,重塑糖尿病骨缺损的病理微环境,协同调控免疫、血管生成与成骨过程,最终实现高效的血管化骨再生。
这一策略不仅为糖尿病骨修复提供了可临床转化的材料平台,也为其他需长期、精准、按需释放治疗分子的疾病治疗提供了通用设计思路,如气体递送、酶促反应调控、局部药物原位生成等。未来,该平台可进一步拓展至多模态治疗、智能响应系统以及更复杂病理环境下的精准再生医学应用。