【Adv.Mater.】基于超1000条数据的金纳米颗粒线粒体靶向筛选:30种材料的高通量体内亚细胞分析
文章标题:High‐Throughput In Vivo Subcellular Analysis of Gold Nanoparticles for Tumor Mitochondrial Targeting
通讯作者:Andy Tay
文章链接:https://doi.org/10.1002/adma.202517706
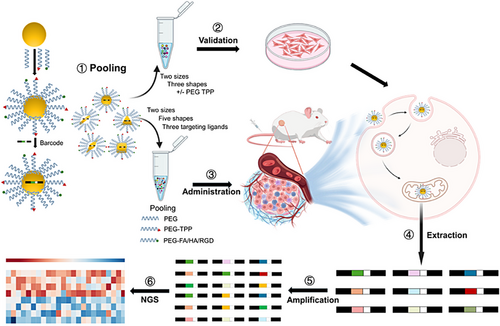
文章概要
引言
线粒体作为细胞能量中心与凋亡调控核心,是肿瘤精准治疗的重要靶点。将药物或核酸直接递送至线粒体,可有效诱导肿瘤细胞死亡并克服耐药性。然而,纳米颗粒在体内需跨越多重生物屏障,包括血液循环中的蛋白吸附、肿瘤血管渗透、细胞摄取、内体逃逸等,最终才能抵达线粒体。因此,开发能够高效穿越多层级屏障的线粒体靶向纳米材料至关重要。金纳米颗粒因其结构稳定、光热性能优异、表面易修饰等优势,被视为线粒体靶向治疗的理想平台。但目前缺乏系统性的体内亚细胞层面比较研究。为此,作者构建了一个基于 DNA 条形码的高通量体内筛选体系,可同时评估多种金纳米颗粒在器官、细胞类型及线粒体层面的分布,实现对材料库的快速筛选。
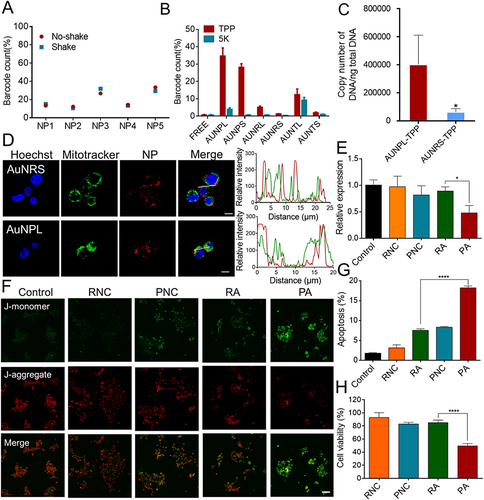
主要实验及结论
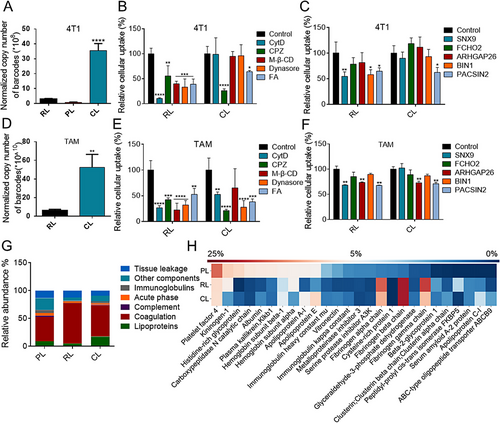
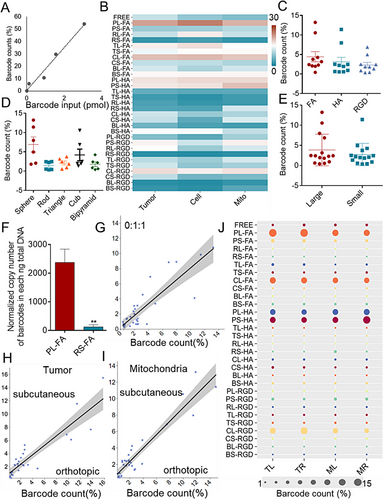
研究首先验证了 DNA 条形码系统在体外的稳定性与可靠性。六种 PEG/TPP 修饰的金纳米颗粒在不同 pH、血清环境及振荡条件下均保持条形码稳定,不影响细胞摄取与线粒体定位。随后,研究扩展至包含 30 种金纳米颗粒的材料库,涵盖五种形貌(球、棒、三角、立方、双锥)、两种尺寸(40/80 nm)及三类肿瘤靶向配体(FA、HA、RGD)。通过在皮下、原位及对侧肿瘤模型中注射混合材料库,研究者在组织、细胞亚群及线粒体层面获得超过 1000 条体内数据。结果显示:线粒体靶向能力与肿瘤累积量高度相关,单一因素(形貌、尺寸或配体)均不足以决定最终表现,而是多参数共同作用。表现最佳的两类材料为大尺寸立方体(CL‑FA)与大尺寸球形颗粒(PL‑FA)。进一步机制研究揭示二者依赖完全不同的生物学路径:CL‑FA 通过高效的网格蛋白介导内吞(CME)及特定膜曲率蛋白(如 PACSIN2、ARHGAP26)促进摄取;而 PL‑FA 虽细胞摄取较弱,但其蛋白冠富含白蛋白与载脂蛋白等“去调理素”,显著延长循环时间,提高肿瘤生物利用度。此外,条形码系统还揭示了材料在肿瘤细胞、免疫细胞、内皮细胞及 CAFs 中的差异分布,其中 CL‑FA 在肿瘤相关巨噬细胞(TAMs)中摄取最高,提示其具有免疫微环境调控潜力。
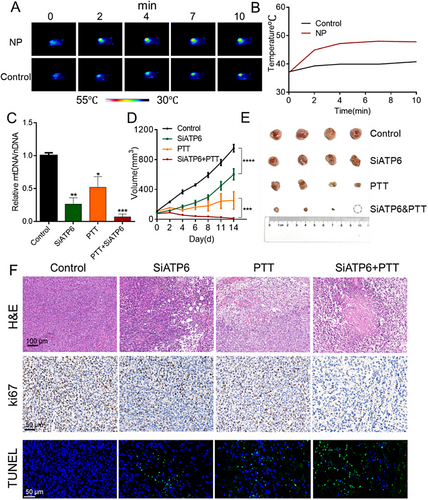
在治疗验证中,研究者选择 CL‑FA 作为候选材料,负载线粒体靶向 siATP6,并结合温和光热治疗(约 47–48°C)。结果显示,单次治疗即可实现 99% 的肿瘤抑制,伴随显著的线粒体损伤、ATP 水平下降及细胞凋亡增加。同时,TAMs 从免疫抑制型 M2 向免疫激活型 M1 转化,肿瘤免疫微环境得到重塑。组织学分析与体重监测均表明该治疗策略具有良好安全性。
总结及展望
本研究首次实现了金纳米颗粒在体内亚细胞层面的高通量筛选,建立了一个可扩展、可量化、可跨模型验证的 DNA 条形码平台。研究揭示了肿瘤累积是实现线粒体靶向的前提,且纳米颗粒的形貌、尺寸、配体及蛋白冠共同决定其体内行为。表现优异的 CL‑FA 与 PL‑FA 依赖完全不同的机制,提示未来可通过“Janus”式设计整合多种优势特性。该平台不仅可用于快速筛选线粒体靶向材料,也可用于解析纳米颗粒在不同细胞亚群中的行为,为精准纳米医学提供强有力的工具。未来工作可进一步扩大材料库规模、引入更复杂的设计,并结合机器学习挖掘多参数间的非线性规律,加速新型纳米药物的开发。