【JACS】 突破免疫检查点:单原子缺陷纳米酶实现强效抗肿瘤免疫治疗
文章标题:Defective Single-Site Nanozymes with Exposed Unsaturated Cu–N2 Sites for Antitumor Immunotherapy via Innate Immune-Checkpoint Blockade
通讯作者:Yinghui Wang_, Hongjie Zhang_, Yanli Zhao 等 文章链接:https://doi.org/10.1021/jacs.5c13802
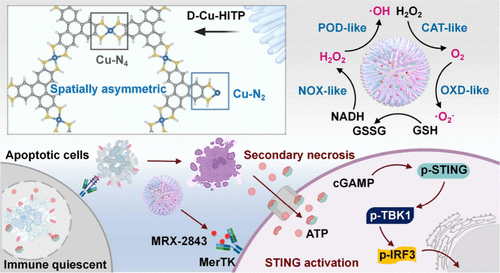
文章概要
引言
免疫治疗作为癌症治疗的重要方向,已在临床上取得突破。然而,现有疗法往往仅针对适应性免疫,导致部分患者疗效有限。肿瘤微环境(TME)中的免疫抑制网络和吞噬性肿瘤相关巨噬细胞(TAMs)阻碍了免疫激活。研究团队提出通过阻断先天免疫检查点——MerTK介导的巨噬细胞凋亡清除,同时诱导活性氧(ROS)风暴,来实现先天与适应性免疫的双重激活。
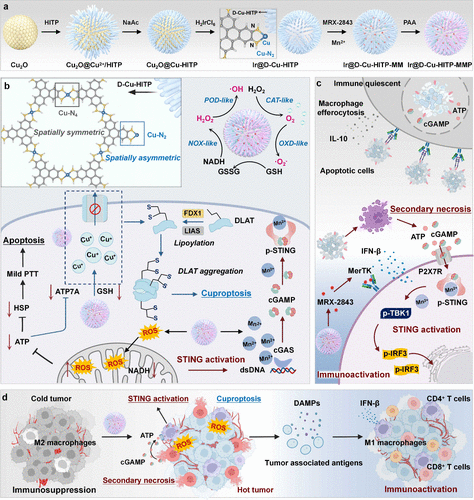
主要实验及结论
研究者设计了基于铜有机框架(Cu-HITP)的缺陷型单原子纳米酶,并在其表面构建铱空心纳米球(Ir@D-Cu-HITP)。该材料具有高度暴露的非饱和Cu–N2位点,打破对称电子分布,表现出优异的类酶催化性能。进一步加载MerTK抑制剂MRX-2843与Mn²⁺,形成复合纳米酶Ir@D-Cu-HITP-MMP。
实验结果显示:
- ROS风暴:通过多酶催化反应破坏肿瘤细胞氧化还原平衡,损伤线粒体功能,降低ATP生成,并诱导铜死亡(cuproptosis)。
- 免疫激活:ROS促进肿瘤细胞DNA泄漏,激活cGAS-STING通路;Mn²⁺进一步增强STING信号;MRX-2843阻断MerTK,抑制巨噬细胞清除凋亡细胞,延长cGAMP与ATP释放,显著提升免疫原性。
- 光热协同:材料在近红外区具有良好光热性能,结合ROS效应实现温和光热治疗,进一步增强免疫激活。
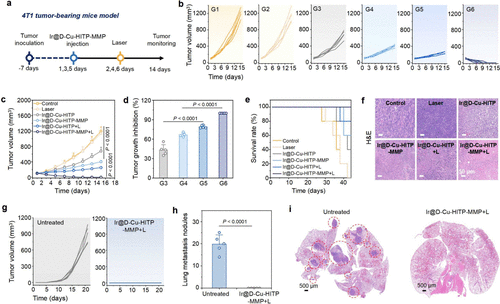
- 体内验证:在乳腺癌与结肠癌小鼠模型中,Ir@D-Cu-HITP-MMP联合光热治疗可完全抑制肿瘤生长,显著延长生存期,并有效防止复发与转移。免疫学分析显示其能促进M2型巨噬细胞向M1型转化,增强树突状细胞成熟,提升CD4⁺与CD8⁺ T细胞浸润,诱导强效抗肿瘤免疫反应。
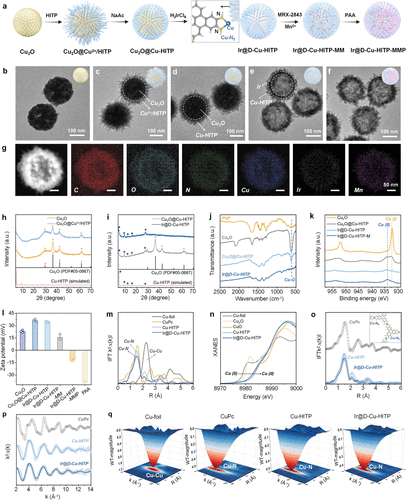
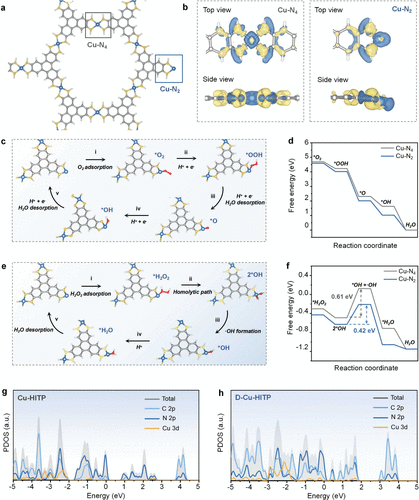
总结及展望
该研究首次通过缺陷型单原子纳米酶结合免疫检查点阻断与STING激活,实现了先天与适应性免疫的协同增强。Ir@D-Cu-HITP-MMP不仅展现出强效的抗肿瘤作用,还具备良好的生物相容性与安全性。未来,该策略有望拓展至多种肿瘤类型,推动纳米免疫治疗从实验室走向临床,为癌症治疗提供全新的思路与工具。