【Nat. Biomed. Eng.】 🧠“2400枚脑器官 + 298种药物 + 94.9%成品率”:用多糖开启人脑类器官高通量建模新纪元
在近十年的干细胞与类器官研究热潮中,人类大脑类器官(human cortical organoids,简称hCO)作为三维培养体系的重要代表,一直被寄予厚望:它能模拟胚胎皮质发育、复制神经疾病表型,甚至可用于类脑神经网络研究和药物筛选。然而,hCO技术虽然令人振奋,却依然面临一个“老大难”问题——规模化与标准化生产难以落地。这不仅限制了疾病建模和药物筛查的广度,也让批间差异成为阻碍科研可重复性的障碍。
一项发表在2025年《Nature Biomedical Engineering》上的研究解决了这一瓶颈问题。来自斯坦福大学、加州大学圣地亚哥分校与日本大阪大学的科学家们开发出一种简单却革命性的策略:在培养基中加入天然可食用多糖“黄原胶”(xanthan gum, XG),即可显著抑制器官融合,提升单位培养体积的产量,实现单人操作、低成本、全自动化兼容的类脑器官高通量生产平台。
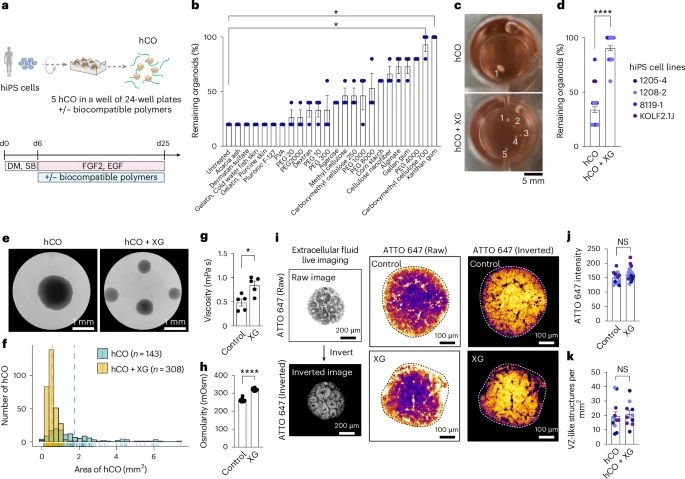
更令人惊喜的是,研究者将该平台应用于298种FDA批准药物筛选,使用超过2400枚皮质类器官,成功鉴定出会影响脑部发育的潜在致畸分子,为神经药物安全性评估开辟新途径。
这项工作不仅打破了“器官融合”这一传统瓶颈,还展示出器官工程与材料科学融合的巨大潜能,让我们一窥未来类脑药物筛选工厂的雏形。
悬浮培养最大难题:融合,融合,还是融合
目前大脑类器官的主流制备方式可归为两类:一是将细胞聚团包埋在Matrigel等基质胶中,二是将聚团直接悬浮于非附着培养皿中,不依赖基底。然而悬浮方式虽然简洁高效,但时间一长便暴露出一个致命问题:类器官在培养过程中会自发融合。
这种融合并非良性增大,而是导致细胞层次紊乱、区域化损伤,最终使器官个体差异巨大,丧失实验可重复性。
以往的解决方式包括人工挑拣(耗时耗力)、使用专用商业培养基(价格昂贵且配方不透明)或每孔只放一个器官(极低效率)。这些方法无一不牺牲了“规模化”或“标准化”。
于是,作者灵机一动:是否可以通过调整培养基的物理属性,来从根源上阻止器官融合?
答案是:可以。而且出人意料地简单。
多糖介入:一勺黄原胶,解决10年难题
研究者筛选了23种可溶性、可食用、可降解的天然高分子材料,最终锁定了——黄原胶(xanthan gum)。这是一种广泛用于食品与药品中的多糖黏合剂,在黏度提升、口感改良等方面早已应用成熟。
将0.01%~0.2%的XG添加至培养基后,实验发现:
- 融合率显著下降:以5个器官共培养为例,传统组在25天时仅剩不到2个器官未融合,XG组则保留超过4个;
- 体积更均一:使用超分辨成像对比15日龄类器官截面积,XG组标准差显著低于对照组;
- 批次稳定性提升:在4个不同的hiPSC细胞系上重复验证,均出现显著改善;
- 成本极低:每250ml培养基仅需1.25元人民币的XG成本,远低于商业替代品。
为了确认XG是通过物理机制抑制融合,作者进一步测试了培养基的黏度与渗透压变化:
- 加入XG后培养基黏度升高1.6倍,渗透压略有上升;
- 通过荧光染料ATTO 647检测发现,XG并不影响培养基深入器官内部的能力;
- 单颗器官单独培养时,XG反而轻微提高了器官体积,说明其并不抑制生长,而仅仅减少了融合。
神经特性不受影响:结构、转录组、钙信号全保留
最关键的问题仍在于:黄原胶真的不会“毒死”神经发育吗?
研究者用了最全面的一套方法给出否定答案:
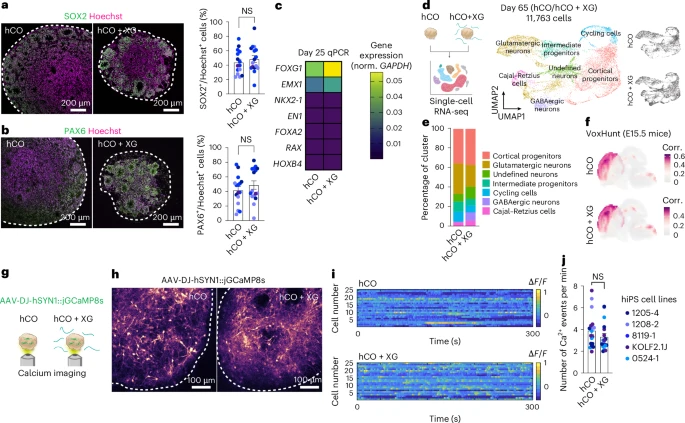
首先是组织学标志物检测:
- SOX2、PAX6(前体细胞)、CTIP2、SATB2(深层与上层神经元)、GFAP(星形胶质细胞)均在XG与对照组中表达相当;
- 轴突形态、胞体结构也未见异常;
- 关键层级结构——神经上皮样区(ventricular zone-like)在组织切片中完整保存,未见紊乱。
其次是转录组水平验证:
- 使用scRNA-seq对65日龄类器官的6720个细胞进行测序,发现XG组与对照组转录图谱高度一致;
- 主成分分析(UMAP)显示两组在神经祖细胞、胶质谱系、兴奋性神经元上无偏移;
- 多巴胺、GABA神经元标志表达比例略有差异,但在文献统计范围内;
- 总体基因表达相关性高达R² = 0.986,p < 0.001。
最后,功能性验证:
- 将编码jGCaMP8s钙感应蛋白的AAV病毒感染XG类器官,使用活细胞钙成像记录自发放电;
- 钙事件频次、强度分布均无显著差异,说明神经元活性未被抑制;
- 这一结果从功能层面验证了XG的“安全性”。
技术真正的价值:千枚级别药物筛选,单人即可完成
科学性的突破固然重要,但工程性的可拓展性更具决定意义。而这正是本研究最激动人心的地方。
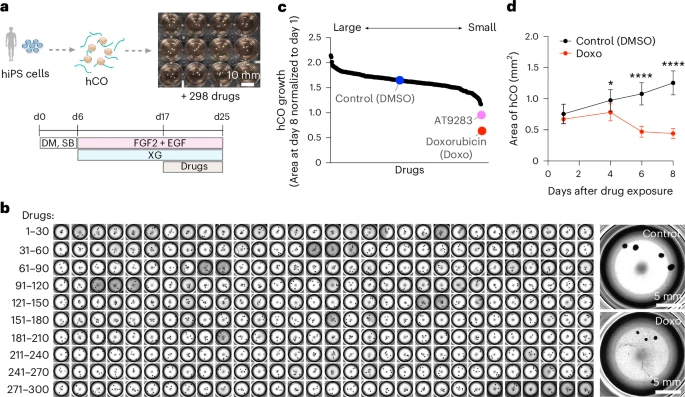
借助XG的“抗融合”特性,研究者首次实现了:
“一人八天筛选298种药物,对2400个皮质类器官进行结构与毒性评估”。
具体流程为:
- 在24孔板每孔加入5个类器官,使用XG简化维护;
- 设定药物浓度为1μM,时间窗为第17~25天(对应神经板期向神经元分化期的转换阶段);
- 使用高通量显微成像系统追踪器官体积变化;
- 将体积显著缩小的药物设定为“影响脑发育的风险因子”;
- 并以免疫组化、3D组织透明化、电生理为辅检手段。
在首轮筛选中,发现多个神经药物与抗癌药物表现出剂量依赖性毒性:
多柔比星(doxorubicin):显著减少SOX2阳性细胞,提升LDH释放,c-Caspase-3染色增强,提示诱导神经祖细胞凋亡;
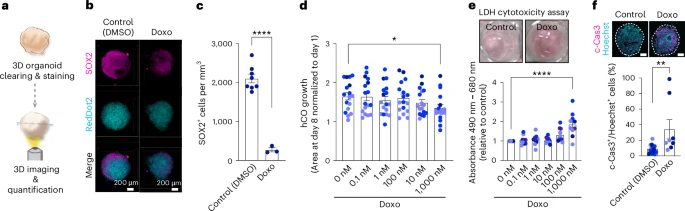
AT9283(一种JAK2/3抑制剂):剂量超过0.1μM后,类器官体积减少超40%,并伴随细胞毒性标志物升高。
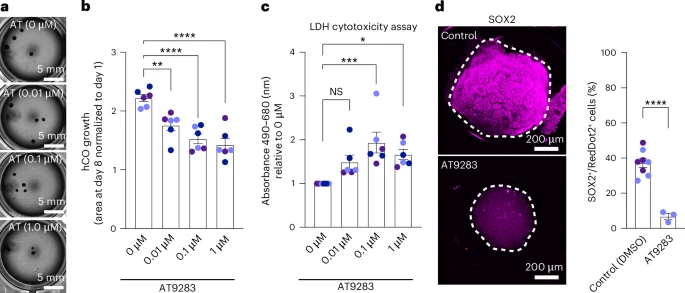
这些药物的神经毒性早有动物实验暗示,但至今缺乏人类细胞水平证据——而XG类器官平台提供了首个体外确认。
未来图景:类脑工厂、自动换液、AI判读一体化
这项技术的诞生,标志着类器官领域由“艺术家手工艺阶段”进入“工程化流水线阶段”。
它的三个直接拓展方向如下:
- 自动化兼容:得益于器官稳定性提升,该平台
继续:类脑工厂的未来已来
从科技发展角度看,该项研究打开了“可扩展人脑模型”的新大门。研究者提出了一种实用的模块化工作流,结合了几项前沿技术趋势:
自动化兼容性:由于XG显著降低器官融合风险,每个孔可同时容纳5–10个类器官,而无需人工干预。配合液体工作站(如Hamilton、Tecan)与自动换液系统,理论上可在96孔、384孔乃至板式生物反应器中执行类脑工厂操作。
成像与AI读数联动:该平台目前依赖ImageJ与人工分割进行体积检测。未来可接入AI训练模型,实现SOX2阳性区、突触密度、凋亡区域的全自动识别与评分,加速药物筛选效率并降低主观误差。
低成本拓展性:相较传统个别微井单颗器官制备,本系统在24孔板上实现“5颗合一”,原材料、人力与时间成本均显著下降,适用于大多数经费受限实验室。
跨器官移植潜力:虽然研究聚焦于皮质器官,但黄原胶抑融合效果对其他类型类器官亦可能适用(如小脑、视网膜、肾脏)。特别在异源组织融合(“组装体”技术)中,避免非目标融合将成为关键控制点。
结语:一勺黄原胶,搅动神经类器官百亿市场
从一种天然多糖出发,这项研究以出乎意料的方式,实现了类器官技术自2013年以来最大的“工程化跳跃”之一。它让复杂的类脑模型脱离精英研究室,向普通实验室、药企研发端甚至临床筛查平台开放了通道。
在ChatGPT、Copilot等大模型掀起语言类脑风暴的同时,类器官正在用湿实验室语言写出另一种“AI”——人类智能的发育轨迹。
我们可以设想这样的未来画面:
- 在一家生物医药公司中,穿戴白大褂的机器人在自动化平台上培养成千上万个hCO,测试新型抗抑郁药对神经通路的影响;
- 某家医疗器械公司,通过类器官平台筛选个体化疗方案,提前预测哪些药物会伤害认知功能;
- 临床试验前,药企可以用XG平台做高通量神经毒性评价,避免可能的致畸风险,拯救无数孕期患者及胎儿。
从“5颗器官一孔”到“2400颗脑器官一屏”,从单一融合监控到300种化合物效应追踪,这不只是黄原胶的奇妙之旅,更是一场神经科学、工程学与人工智能交织的科研革新。
参考文献
Narazaki, G., Miura, Y., Pavlov, S.D. et al. Scalable production of human cortical organoids using a biocompatible polymer. Nat. Biomed. Eng (2025). https://doi.org/10.1038/s41551-025-01427-3