【Nat. Biomed. Eng.】🚀12.5分钟采集+0.018毫升体素:12种分子一次全脑超高分辨率代谢成像新纪元
磁共振光谱成像(MRSI)在揭示人脑代谢活动方面拥有天然优势:无需对比剂、无放射性,能够非侵入性地测量神经元健康、细胞膜更新与神经递质平衡等信息。然而,临床上MRSI长久以来受制于收集时长过长、覆盖范围受限、空间分辨率低和信噪比不足四大瓶颈。单次高分辨率全脑扫描往往耗时半小时甚至数十小时,无法融入常规体检或研究流程;低浓度的代谢物常被水和脂质信号淹没,数字量化和图谱重建都存在巨大挑战;而多谱峰重叠又让谷氨酸(Glu)与γ-氨基丁酸(GABA)等关键分子的区分成为不可能之事。
在2025年6月《Nature Biomedical Engineering》上,李等人带来了一项颠覆性的技术:超快J解析MRSI(Ultrafast J-resolved MRSI),融合了FID(自由感应衰减)与双回波时间SE(自旋回波)采集策略,并巧妙引入物理引导的机器学习重建模型,使得全脑多分子代谢图谱能够在12.5分钟内获得,体素空间分辨率高达3.0×2.0×3.0毫米³(体积约0.018毫升),同时完整映射N-乙酰天冬氨酸(NAA)、肌酸(Cr)、胆碱(Cho)、肌醇(mI)、谷氨酸(Glu)、谷氨酰胺(Gln)、乳酸(Lac)和GABA等12种代谢物和神经递质。这一成果不仅刷新了临床MRSI的时间和空间极限,更为脑功能和疾病无标记、定量化代谢成像开辟了全新路径。
长久难题:为何高分辨率MRSI难以普及?
MRSI要实现全脑、高空间分辨率、高化学选择性,需要在三大维度同时发力:空间编码、谱线分离和收集速度。然而,传统方法面临天然矛盾。要获得1毫升甚至更小体素,需要在k-空间进行密集采样,延长扫描时间;为分离J耦合导致的谱峰重叠,需要进行二维J解析,进一步加重时长;而低浓度分子则迫使研究者进行多次信号平均,时间再度被拉长。与此同时,头皮下脂肪和组织水信号强度远超目标谱峰,光谱抑制技术尚不完备,分子定量更需精细算法。即便在高场3T、7T扫描仪上,单波段一维MRSI通常也要耗费10分钟以上才可勉强覆盖单个大脑切片;真正能同时实现J解析的高分辨率全脑扫描更是遥不可及。
技术突破:FID+SE双通道采集融合J解析
针对上述核心瓶颈,研究者首先在数据采集环节进行了重构。超快J解析MRSI采用FID通道进行高空间分辨率的快速编码,配合恩斯特角(Ernst angle)低翻转角激发、超短回波时间(TE)和短重复时间(TR),在极短时间内获得丰富的化学位移与空间信息。与此同时,仅对低分辨率k-空间进行两次自旋回波(TE=50毫秒和190毫秒)采集,以编码J耦合演化,从而有效分离Glu、Gln、GABA等紧密谱线。两路信号在时间上交错执行,FID数据负责提升整体信噪比与空间细节,SE数据负责多谱峰解缠,二者有机配合后,采集时间竟由传统的数小时骤降至12.5分钟,比以往J解析MRSI方法快百倍。
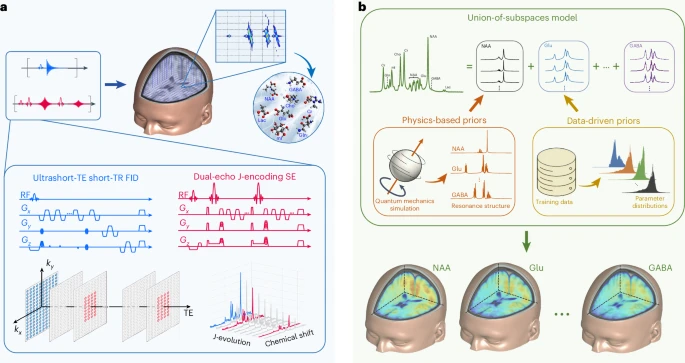
智能重建:基于子空间模型的物理引导机器学习
数据采集只是半程,如何从高度稀疏的混合FID/SE信号中重建高质量的多分子图谱?研究团队将物理先验与机器学习相融合,提出“子空间联合模型”(union-of-subspaces)。模型将每种代谢物或神经递质的谱线演化主体视作一个低维子空间,子空间基函数由量子仿真生成谱峰结构,再通过机器学习估计线宽、相位和T₂衰减。重建过程等同于从稀疏编码的FID+SE数据,利用多个子空间的联合表示逐步滤波、去噪并分离目标分子信号,最终同步获得七维时空(x,y,z,频率,J谱域)上具有量化能力的光谱体数据。该策略既减少了对大规模参数学习的需求,也确保了分子特征的物理一致性,冰与火般兼顾了准确性与泛化能力。
幻像验证:九管配置呈现分子浓度与体素分辨极限
在装有NAA、Cr、Cho、mI、Glu和GABA的标准MRSI幻像里,研究者将三种不同浓度的同一溶液并排,并设计8毫米、12毫米和16毫米三种管径测试空间分辨力。结果表明,经超快J解析MRSI重建后,所有分子在8毫米体素内均能稳定分离且定量准确。不同浓度管间信号强度比与实测浓度一致度达95%以上,体素内信号波动小于3%。相同采集时长下,对比传统3D MRSI只能获取30毫升体素的惨淡局面,超快J解析MRSI无疑赢得了“空间与化学两票全胜”。
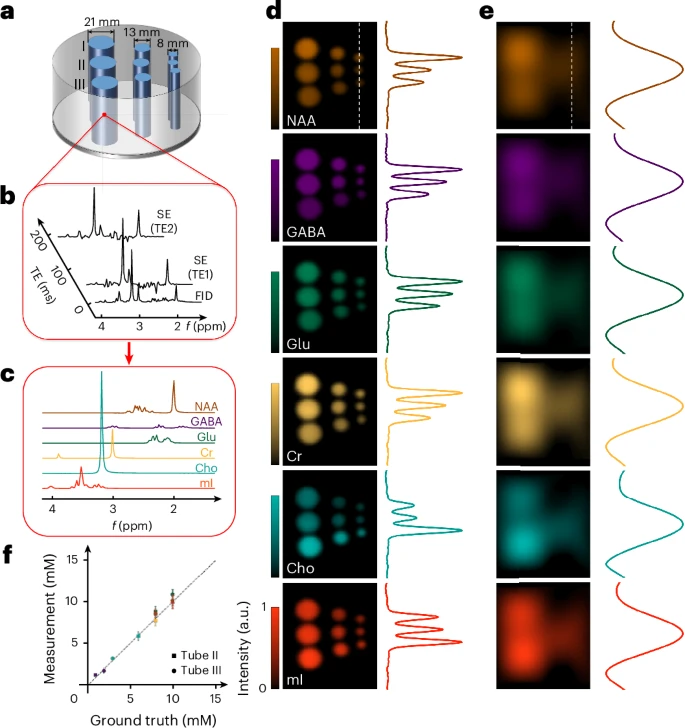
健康大脑:3.0×2.0×3.0毫米³下的代谢多态性
将该技术应用于健康受试者全脑扫描,研究者以3.0×2.0×3.0毫米³为名义分辨率,成功绘制了包括NAA、Cr、Cho、mI、Glu、Gln、Lac和GABA在内的12种分子全脑成像图谱。通过51个常用脑区ROI分析,揭示出皮质灰质与白质在NAA、Cr、Glu、Gln和GABA含量上的显著差异,以及Cho、mI在白质高于灰质的规律。基于Bland–Altman与ICC分析的测试内重测、跨日重测和跨中心重测,所有小区块CV均低于8%,ICC大多超过0.93,结果稳定复现性堪比传统功能性MRI,为临床及研究提供了可靠多次随访基础。
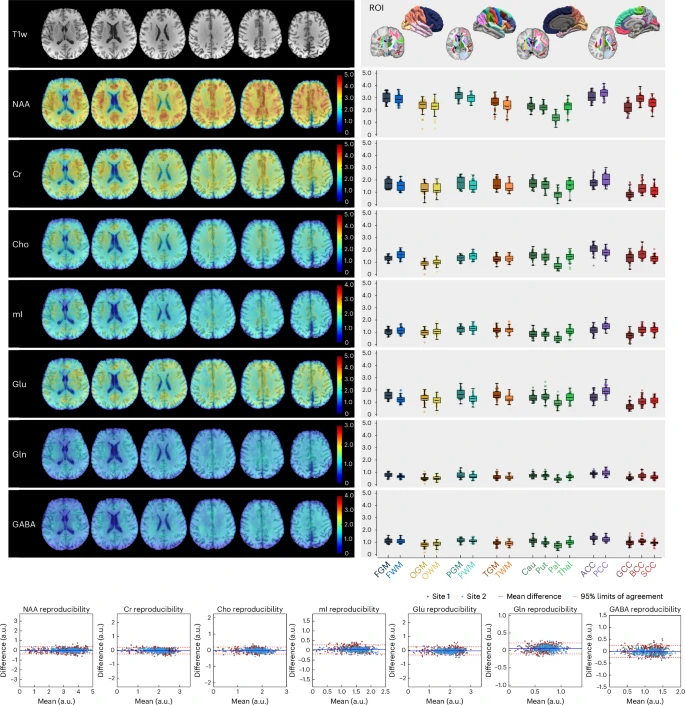
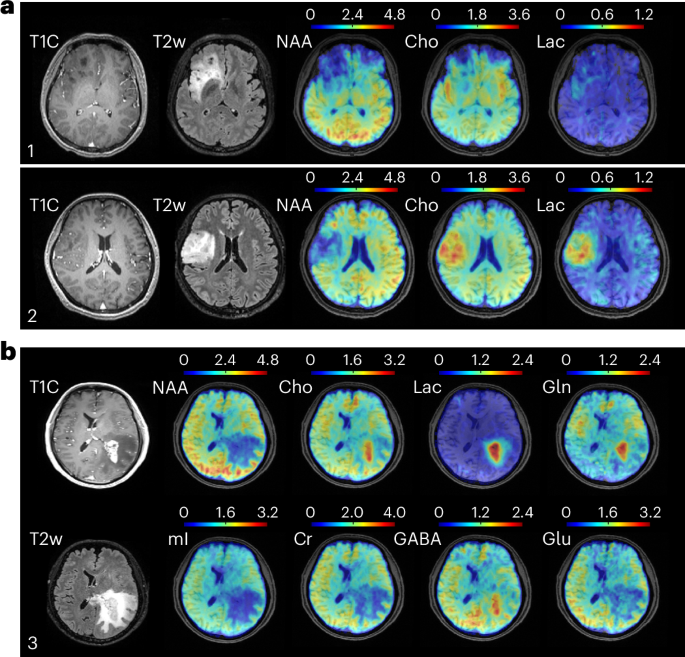
肿瘤分型:从II级到IV级的代谢指纹
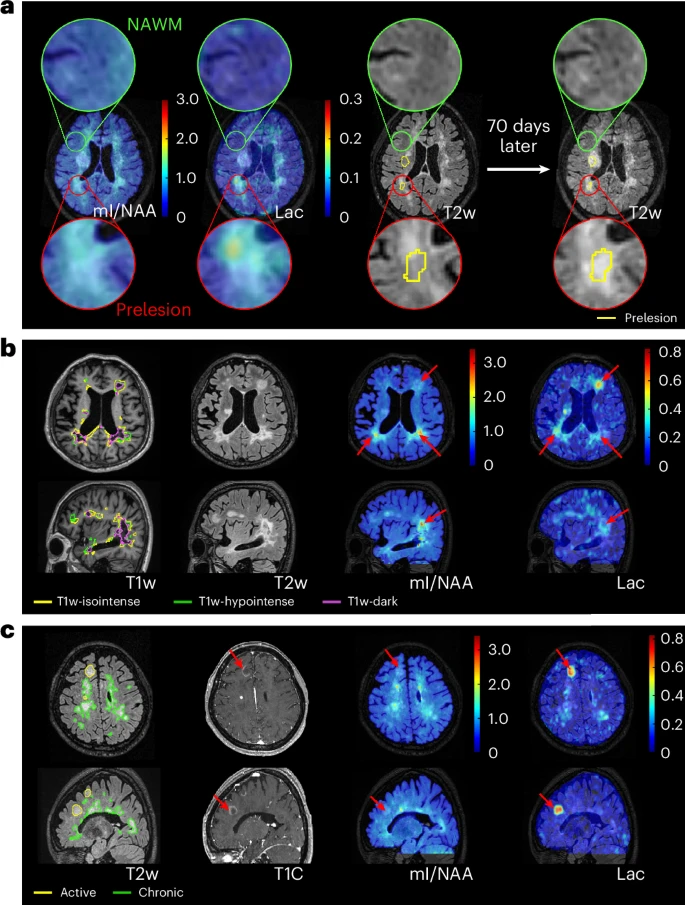
在三名脑肿瘤患者扫描中,该技术分别捕捉到II级与III级少突胶质瘤在Cho和Lac含量上的87.6%和107.5%差异,传统T1增强与T2 FLAIR结构图毫无分级线索却在分子图中一目了然。对于IV级胶质母细胞瘤,增强区Cho上升45.7%、Lac飙升1573%、Gln增加79.9%、GABA增加55.5%,而NAA、mI、Cr、Glu均明显下降,代谢异质性与侵袭区组织结构形成了完美对应。无需注射造影剂的无标记分子成像,让诊断更加直观精准。
多发性硬化:早期病灶与活动慢性分期的分子探针
研究者对一例复发缓解型MS患者进行了70天前后两次扫描,首次扫描时常规T2 FLAIR尚未见病灶,mI/NAA比值已在预病灶区升高30.3%,Lac上升120.9%,70天后影像随访确认病灶形成。进一步分析T1黑洞、T1低信号与T1等信号三类慢性病灶,mI/NAA增幅呈38.3%、51.1%、73.0%渐增,Lac在各型病灶均增加20%–29%。活动病灶相较慢性病灶Lac高出237%,mI/NAA降低27.9%,实现了对炎症与慢性脱髓鞘阶段的分子分型。本项技术首次将MS病灶的化学演变映射至微升级别,为精准免疫学干预提供了完全新维度。
技术展望:迈向功能代谢的临床新范式
超快J解析MRSI不再是限于单体素或单切片的“科研小众”,而是在12.5分钟内实现全脑高分辨率、无对比剂、无辐照、12种分子同时定量。它打通了神经科学、肿瘤学和免疫神经学的桥梁:从研究神经活动与脑区功能耦合到精准分类肿瘤分型,再到早期干预MS病灶,MRSI正从影像“看形态”走向分子“解生理”。
未来,这一技术将与动态功能MRI、PET、EEG等多模态成像深度融合,构建人体大脑代谢活动的动态全景;基于AI的自动化重建与异常检测,也将让零基础用户在社区医院即可上手。更远期,它或将成为脑机接口和代谢调控的“生理级反馈”,为大脑疾病诊疗、脑健康管理乃至人机共生开辟全新疆域。
当0.018毫升体素能够披露分子级信息,当12.5分钟扫描实现12种分子全景成像,MRSI的时代终于到来。无需等待,对话大脑,明察秋毫,超快J解析MRSI正引领代谢影像的新篇章。
参考文献
Zhao, Y., Li, Y., Jin, W. et al. Ultrafast J-resolved magnetic resonance spectroscopic imaging for high-resolution metabolic brain imaging. Nat. Biomed. Eng (2025). https://doi.org/10.1038/s41551-025-01418-4