【Nat.Nanotechnol.】新策略:利用铁基纳米药物增强造血干细胞损伤后再生
这篇发表在《自然-纳米技术》(Nature Nanotechnology)上的文章,介绍了一项关于如何利用一种已获批的纳米药物——静脉注射用氧化铁(Ferumoxytol, FMT),来促进造血干细胞(Hematopoietic Stem Cells, HSCs)在受到各种应激损伤后的再生和恢复的研究。这项研究揭示了FMT在保护健康造血干细胞的同时,还能对白血病细胞产生不同的作用,为血液系统疾病的治疗,特别是造血干细胞移植后的恢复和癌症治疗带来的希望。
1. 研究背景:造血干细胞的脆弱性与临床挑战
造血干细胞是骨髓中一类非常重要的细胞,它们是所有血细胞的“祖先”,具有自我更新和分化为各种成熟血细胞(如红细胞、白细胞、血小板)的能力。正常情况下,大多数造血干细胞处于相对静止的状态,只有少数会进入细胞周期进行分裂,以维持机体日常对血细胞的需求。
然而,在某些应激条件下,造血干细胞会大量活化并快速分裂,以补充受损或丢失的血细胞。这些应激条件包括:
1.1 体外培养
在实验室中扩增造血干细胞(体外扩增),以便用于移植等治疗。
1.2 化疗和放疗
用于治疗癌症的化疗药物和放射线在杀死癌细胞的同时,也会不可避免地损伤快速分裂的造血干细胞。
1.3 感染和衰老
严重的感染或随着年龄增长,也会对造血干细胞的功能产生不利影响。
1.4 造血干细胞移植(HSCT)
造血干细胞移植是治疗白血病等血液恶性肿瘤的重要手段。在移植前,患者通常需要接受大剂量化疗或全身放疗(预处理),以清除体内的恶性细胞和抑制免疫反应,但这也会对健康的造血干细胞造成严重损伤。移植后,新的造血干细胞需要在受损的骨髓环境中重建完整的造血系统,这是一个充满挑战的过程。
这些应激条件下造血干细胞的过度活跃分裂会产生大量的活性氧(Reactive Oxygen Species, ROS)。ROS是一类含氧的、具有高反应活性的分子,适量的ROS在细胞信号传导中起作用,但过量积累会导致氧化应激,损伤细胞内的各种大分子,包括DNA。造血干细胞中ROS的积累会损伤它们的DNA,导致其功能衰竭,自我更新能力下降,甚至细胞死亡。最终表现为造血功能障碍,无法产生足够的血细胞,即所谓的造血衰竭或全血细胞减少。
目前虽然有一些方法,如调节细胞代谢或改善微环境,可以一定程度上改善应激状态下造血干细胞的功能,但仍然需要更有效的方法来减轻造血干细胞的损伤,促进它们的再生。虽然细胞自身具有抗氧化酶来清除ROS,但在应激条件下产生的过量ROS常常超出这些酶的处理能力。因此,寻找有效的手段清除造血干细胞内的ROS,是保护其功能和促进造血恢复的关键。
2. 研究焦点:已批准纳米药物 Ferumoxytol 的独特作用
文章将研究焦点放在了静脉注射用氧化铁(Ferumoxytol, FMT)上。FMT是一种由超顺磁性氧化铁纳米颗粒组成的药物,主要用于治疗慢性肾病患者的缺铁性贫血。它已经获得了美国食品药品监督管理局(FDA)的批准用于临床。以往的一些研究表明,氧化铁纳米颗粒在不同的pH环境下可能表现出类似酶的催化活性,包括在酸性条件下类似过氧化物酶的活性(可以将H₂O₂转化为有毒的羟基自由基),以及在中性条件下类似过氧化氢酶(Catalase, CAT)的活性(可以将H₂O₂分解为水和氧气)。
这项研究提出一个问题:作为一种铁基纳米药物,FMT是否能够在复杂的体内环境中,对造血干细胞和白血病细胞产生不同的影响,并且能否作为一种有效的ROS清除剂来保护受损的造血干细胞,促进造血功能的恢复?
3. 关键发现:FMT 对造血干细胞与白血病细胞的差异作用
研究人员首先比较了FMT对健康小鼠造血干细胞(特别是长期造血干细胞,LT-HSC)和白血病细胞(急性髓系白血病,AML细胞)的影响。他们发现了一个非常重要的现象:
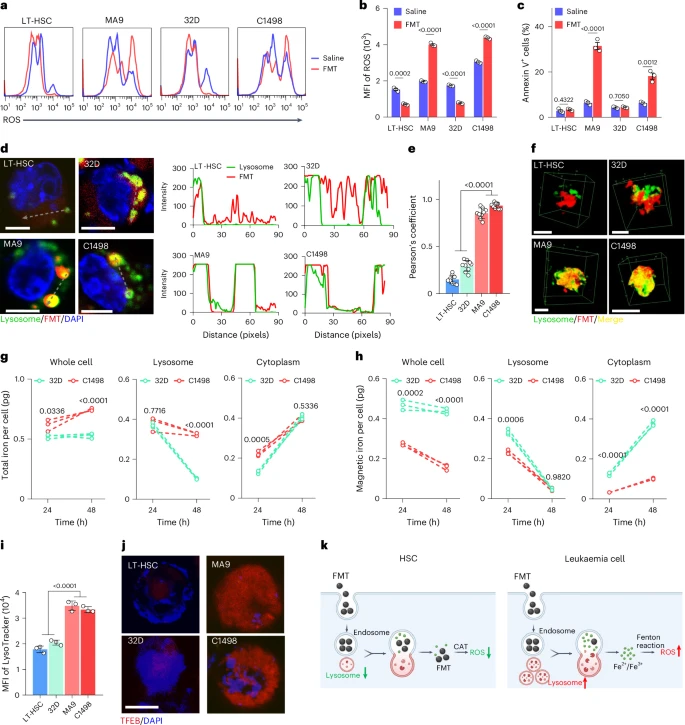
3.1 FMT 在健康造血干细胞中清除 ROS
实验结果显示,在体外用FMT处理健康小鼠造血干细胞后,细胞内的ROS水平显著降低。这表明FMT在健康造血干细胞中发挥了ROS清除剂的作用。进一步的机制研究发现,FMT的这种保护作用主要归功于其类似过氧化氢酶(CAT-like)的活性,能够有效分解细胞内过多的过氧化氢(H₂O₂),从而减轻H₂O₂引起的细胞毒性和DNA损伤。
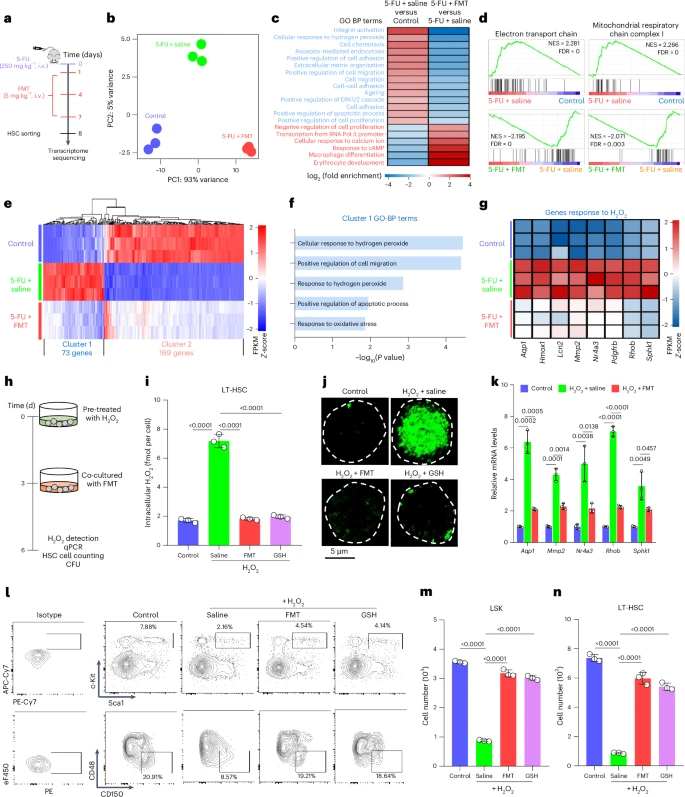
3.2 FMT 在白血病细胞中增加 ROS,诱导细胞死亡
与对健康造血干细胞的作用截然不同,FMT在白血病细胞中却显著提高了细胞内的ROS水平,并诱导了白血病细胞的凋亡(一种程序性细胞死亡)。这种差异作用使得FMT能够在不损伤健康造血干细胞的情况下,有效地杀伤白血病细胞。
3.3 差异作用的潜在机制:细胞内分布和溶酶体活性差异
为什么FMT会对这两种细胞产生如此不同的影响呢?研究人员深入探究了FMT在造血干细胞和白血病细胞内的分布和代谢过程。他们发现:
- 细胞内分布不同: 在健康造血干细胞中,大部分FMT纳米颗粒进入细胞后倾向于滞留在细胞质中,保持完整的纳米颗粒形态。在细胞质中性环境中,FMT主要表现出类似过氧化氢酶的活性,清除ROS。而在白血病细胞中,更多的FMT纳米颗粒会被内吞并运输到溶酶体中。
- 溶酶体活性差异: 白血病细胞通常比健康造血干细胞具有更高的溶酶体活性。溶酶体是细胞内负责降解物质的细胞器,其内部环境偏酸性。在白血病细胞的酸性溶酶体环境中,FMT纳米颗粒更容易发生降解,释放出游离的铁离子。
- 铁离子的 Fenton 反应: 释放的铁离子在细胞内,特别是在ROS存在的情况下,可以参与Fenton反应,催化H₂O₂产生具有强氧化性的羟基自由基,进一步增加ROS水平,从而对白血病细胞产生毒性。白血病细胞中较高的ROS水平也为Fenton反应提供了条件。
因此,FMT对造血干细胞和白血病细胞的差异作用,很可能与两种细胞类型对FMT纳米颗粒的内吞、运输到溶酶体以及在溶酶体内的降解程度不同有关,这导致FMT在健康造血干细胞的细胞质中发挥类似过氧化氢酶的ROS清除作用,而在白血病细胞的溶酶体中释放铁离子并通过Fenton反应产生ROS,诱导细胞死亡。
4. 临床应用潜力:促进造血恢复与清除白血病细胞
基于FMT对造血干细胞和白血病细胞的差异作用,研究人员进一步在动物模型中评估了FMT在促进造血恢复和治疗白血病方面的临床应用潜力。
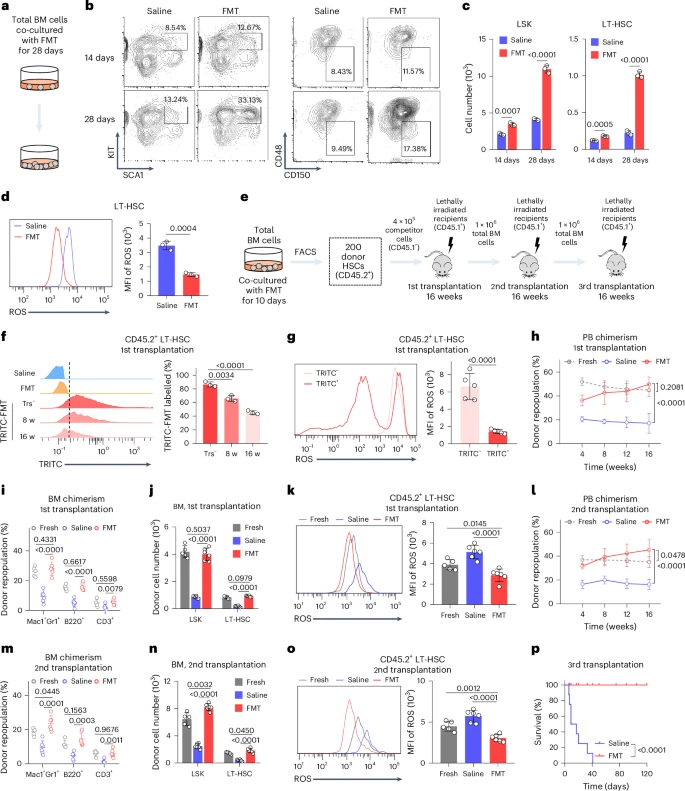
4.1 体外培养造血干细胞功能的增强
在体外将造血干细胞与FMT共同培养后,研究人员发现FMT能够显著减少长期培养过程中造血干细胞内ROS的积累和细胞凋亡,并有效维持造血干细胞的长期增殖和分化能力。通过竞争性移植实验证明,经过FMT体外处理的造血干细胞,移植到受体小鼠体内后能够更有效地重建血造血系统,提供更持久的造血功能。
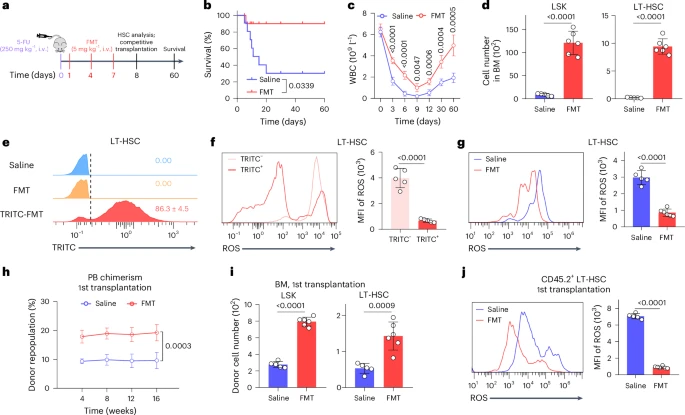
4.2 受损造血功能的体内恢复
研究人员构建了小鼠的造血损伤模型,包括使用化疗药物5-FU诱导的损伤以及致死剂量全身放疗(TBI)诱导的损伤。在这些模型中,静脉注射FMT治疗显著促进了小鼠体内受损造血干细胞的恢复,加快了外周血细胞数量的回升,增加了骨髓中造血干细胞和祖细胞的数量,并降低了造血干细胞内的ROS水平和凋亡率。这些结果表明FMT能够有效地减轻化疗和放疗对造血系统的损伤,促进造血功能的再生。
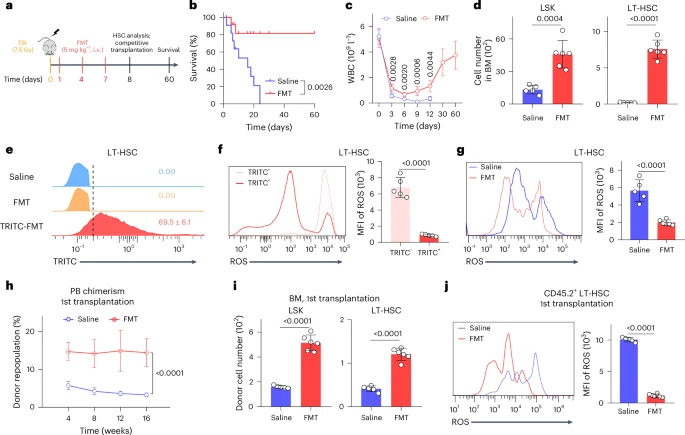
4.3 在白血病模型中清除白血病细胞并保护造血干细胞
为了模拟临床上白血病伴随造血干细胞移植的情况,研究人员使用了白血病小鼠模型,并进行了致死性全身放疗预处理后的造血干细胞移植。在这个模型中,移植后给予FMT治疗,不仅有效地清除了小鼠体内的白血病细胞,而且显著改善了移植造血干细胞的功能和长期造血重建能力。更重要的是,FMT治疗在清除白血病细胞的同时,保护了移植的造血干细胞免受损伤,显示出其独特的治疗优势。
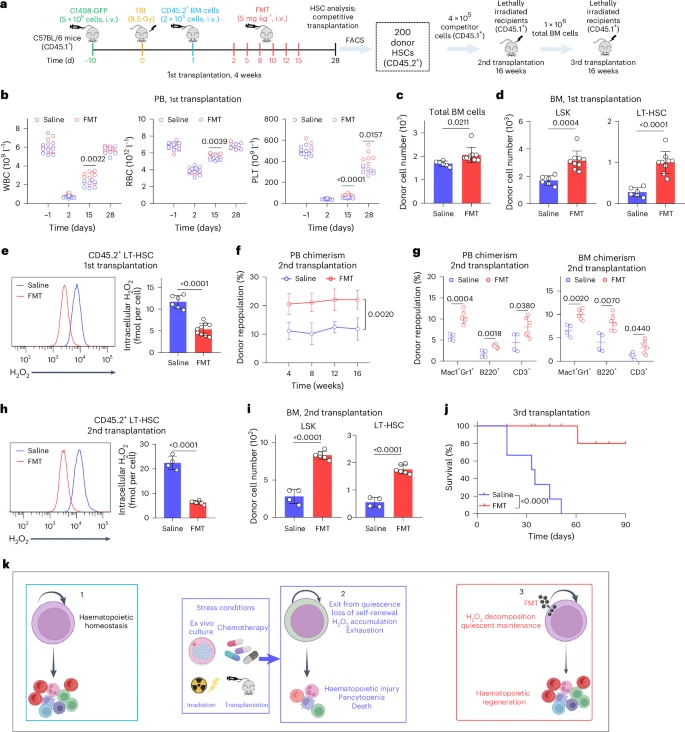
此外,研究人员还构建了一种铁离子输出蛋白(Ferroportin, FPN)表达水平较低的白血病细胞模型。FPN是细胞输出铁离子的主要通道。在这类FPN低表达的白血病细胞中,铁离子容易在细胞内积累。研究发现,FMT对这类白血病细胞具有更强的杀伤作用,进一步证实了FMT通过增加细胞内铁离子来发挥毒性作用的机制。同时,在携带这类白血病细胞的小鼠模型中,FMT治疗在有效控制白血病进展的同时,依然能够保护健康的造血干细胞。
4.4 生物安全性评估
作为一种潜在的临床应用药物,FMT的安全性至关重要。研究人员对FMT的生物分布和长期安全性进行了评估。他们发现FMT主要分布在肝脏、脾脏等器官,在骨髓中也有一定分布。长期给予FMT治疗并未引起小鼠明显的体重变化、血液生化指标异常或主要器官的病理损伤,提示FMT具有较好的生物安全性。
5. 结论与未来展望
这项研究证明,已获批的纳米药物FMT具有独特的双重作用:在健康造血干细胞中作为ROS清除剂,通过类似过氧化氢酶的活性分解H₂O₂,减轻氧化应激损伤,促进细胞再生;而在白血病细胞中,由于细胞内分布和溶酶体活性的差异,FMT更容易降解释放铁离子,通过Fenton反应产生ROS,诱导细胞死亡。
这种对健康细胞的保护作用和对癌细胞的杀伤作用相结合的特性,使得FMT在血液系统疾病的治疗中展现出巨大的潜力。研究结果表明,FMT能够有效促进受损造血干细胞的恢复,增强体外扩增造血干细胞的移植效果,并在白血病模型中实现白血病细胞的清除与造血干细胞的保护。
目前临床上还没有获批的有效的酶促抗氧化剂可以直接用于促进造血干细胞在癌症治疗或移植后的恢复。现有的许多抗氧化剂和纳米酶缺乏细胞选择性,可能在清除ROS的同时也保护了白血病细胞,带来安全隐患。这项研究强调了在设计用于清除ROS的纳米酶时,考虑肿瘤细胞和正常细胞之间差异的重要性。白血病细胞为了快速生长,其能量代谢更活跃,溶酶体活性也更高,这为FMT在白血病细胞中特异性释放铁离子并发挥毒性提供了基础。
总的来说,这项研究不仅揭示了FMT在造血干细胞损伤后再生的新功能和作用机制,也为其在临床上用于促进接受应激治疗(如化疗、放疗或造血干细胞移植预处理)的患者造血系统恢复提供了重要的理论依据和实验支持。未来,FMT有望成为改善血液系统疾病治疗效果、提高患者生存率的重要临床工具。
来源文章链接:
Wang, Q., Qian, W., Han, Y. et al. Ferumoxytol promotes haematopoietic stem cell post-injury regeneration as a reactive oxygen species scavenger. Nat. Nanotechnol. (2025). https://doi.org/10.1038/s41565-025-01907-2