🤯 【JACS】颠覆!有机分子首获“量子嗅觉”:只需,室温水溶液中对DNA静电场灵敏度提升53%!
✨文章标题:A Conjugated Oligoelectrolyte Exhibiting Room Temperature Spin-Correlated Radical Pair Character for Biological Sensing ✉️作者:Ricardo Javier Vázquez* 等 🔗链接:https://pubs.acs.org/doi/10.1021/jacs.5c10750
💡 从“痛点”到“突破”:量子生物传感的“水土不服”难题
在生命科学的前沿,我们正试图用最精密的“尺子”——量子技术,来衡量生物世界中那些转瞬即逝、极其微弱的信号。这门学问被称为“量子生物传感” 。想象一下,如果能以前所未有的分辨率,捕捉到DNA、蛋白质等生物分子在特定状态下产生的微弱电场或磁场变化,那将彻底革新我们对疾病、遗传和药物反应的理解。
然而,要让高高在上的“量子”走进湿漉漉的细胞世界,一直存在一个巨大的“水土不服”难题。
目前的顶级量子探针,比如钻石中的氮-空位(NV)中心,虽然性能卓越,但它们大多是固体传感器,需要将生物分子固定在钻石表面才能检测。这对于研究在水溶液中自由扩散的生命体——比如你我体内的DNA或蛋白质——来说,几乎毫无用武之地。我们需要一种水溶性、能在室温下工作,并且具备量子特性的分子探针。
这次,科学家们找到了一个完美的有机分子解决方案:一种名为COE-CbzBP的共轭低聚电解质。它不仅水溶性好、生物相容性高,更关键的是,它在室温下竟然能产生自旋关联自由基对(SCRP),这是一种关键的“量子”特征,使其成为一种极具潜力的分子量子比特(Qubit)。这篇发表在《JACS》上的研究,正是实现了这种分子量子探针在生物体环境中的突破性应用。
🔬 核心方法与技术细节:分子“扭曲”带来的量子魔术
COE-CbzBP究竟是如何在水溶液中实现这一“量子魔术”的?一切都藏在它的分子结构设计中,尤其是其 “扭曲”的几何构型 。
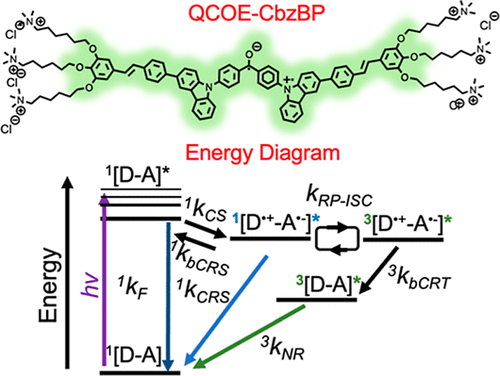
🔑 关键机制:从激子到自由基对的“跳跃”
SCRP,即自旋关联自由基对,是这种分子探针的核心。它不是一个普通的自由基,而是由两个空间分离但自旋量子纠缠的自由基离子组成的。想象一下,一个电子从分子中的“供体”(Donor,即咔唑Cbz)部分,瞬间跳到了“受体”(Acceptor,即二苯甲酮BP)部分,形成了带正电的阳离子自由基 和带负电的阴离子自由基 。这个自由基对的初始状态通常是单线态()。
而量子传感的关键,在于这个单线态 必须能够高效地转化为三线态()。只有当它处于三线态时,才能被电子顺磁共振(EPR)检测到,并对周围环境的磁场效应(MFE)和电场效应(EFE)产生灵敏的响应,从而实现传感。
🤯 “扭曲”带来的三大核心优势
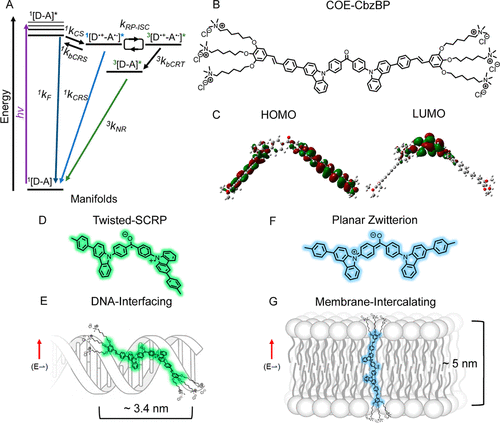
COE-CbzBP分子设计的精妙之处,就在于在供体(咔唑)和受体(二苯甲酮)之间的氮-碳(N-C)连接处,故意引入了一个部分共轭中断。这个设计直接促成了分子在激发态下形成一个扭转的分子内电荷转移(TICT) 几何构型。
这种TICT构型带来的优势,是实现室温SCRP的关键:
最小化单线态-三线态能隙()。传统的分子通常具有较大的 ,这使得从 到 的自旋转换(即系间窜越)在室温下难以发生。TICT构型通过最大程度地分离最高占据分子轨道(HOMO)和最低未占据分子轨道(LUMO)的空间分布,显著减少了轨道间的重叠。轨道重叠的减少,直接最小化了电子交换能 ,而 正是与 成正比()。
最小化自由基对交换耦合()。 是决定 和 能量差的关键,它与 直接相关()。一个小的 值是分子量子比特的“入场券”,因为它极大地促进了光诱导的自旋流形混合,从而产生更大的自旋极化信号。
有利的电荷分离吉布斯自由能()。最小化 和 只是理论基础,实际的电荷转移过程必须在热力学上可行。通过雷姆-韦勒(Rehm-Weller)方程计算,在水溶液中电荷分离(形成自由基对)是接近热中性的(),但在DNA环境中则变得热力学上有利()。这意味着在生物环境中,形成量子态的SCRP是“顺理成章”的。
简而言之,COE-CbzBP就像一个拥有“可调关节”的有机探针。在水溶液中,它采取扭曲(TICT) 构型,激活了量子特性;而在某些僵硬的环境中,例如脂质双分子层(脂质体)中,它被迫采取平面构型,量子特性则被关闭。这种几何依赖性的开关,就是其生物传感的“秘诀”。
📊 数据背后的创新与颠覆性:DNA的“电场”指纹
这项研究的颠覆性在于,它首次证明了这种有机分子SCRP在室温和水溶液中,能够对自由扩散的生物大分子(DNA)的静电场产生响应。
💎 突破1:室温下的超小能隙与量子激活
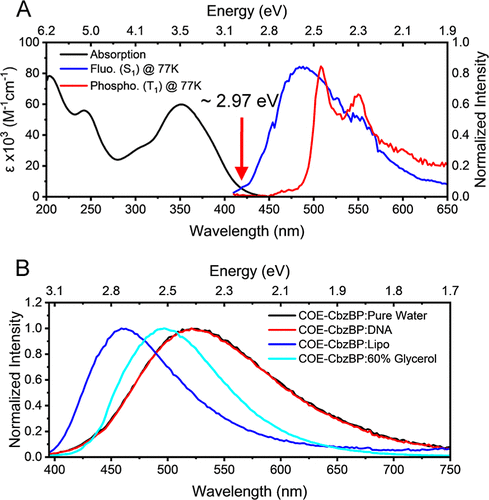
通过门控光致发光光谱法,科学家们在77 K的低温下,精确测量了COE-CbzBP的荧光峰(,)和磷光峰(,)。
结果令人振奋:它得出了一个极小的单线态-三线态能隙 。
这个数值至关重要,它对应的自由基对交换耦合 仅为 。这个 值只比室温下的玻尔兹曼热能 或 ) 大约 倍。这意味着室温下的热能就足以克服这个微小的能垒,驱动单线态和三线态之间的有效混合( thermally activated spin mixing),从而高效地生成SCRP,并使其在室温下具有自旋极化的特性。
这一实验结果,是打破传统固态传感器局限、实现室温、水溶性量子生物传感的关键奠基石。
⚡ 突破2:DNA静电场的精确“指纹”识别
实验的真正高潮,发生在将探针引入生物环境时,特别是与DNA的相互作用。
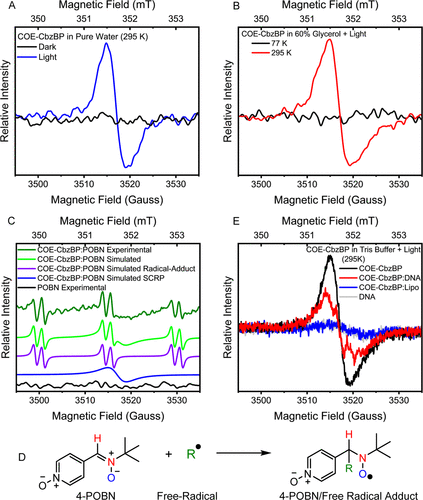
科学家们使用连续波电子顺磁共振(CW-EPR) 光谱来监测COE-CbzBP的自旋极化信号。
纯水溶液中(光照): COE-CbzBP显示出一个清晰的单峰EPR信号。
脂质体环境中(光照): 未观察到任何自旋极化信号。脂质双分子层作为一种刚性、非极性环境,迫使COE-CbzBP采取平面的、类分子三线态的构型,导致更高的 ,从而抑制了SCRP的形成。
DNA环境中(光照): 令人震惊的现象发生了——原本的单峰EPR信号,竟然分裂成了明显的双峰。
这种EPR信号分裂被科学家们归因于DNA的静电场-自旋耦合效应。DNA分子周围的静电场强度,据估计在2纳米范围内可以达到惊人的 。当COE-CbzBP以扭曲的TICT构型与DNA结合时,这个强大的局部电场能够调制SCRP的交换耦合()和超精细耦合(),就像对量子态施加了一个“电场压力”,从而导致EPR谱线发生分裂。
通过瞬态吸收光谱(TAS)也佐证了这一点。在DNA存在下,SCRP的寿命被显著延长( 从 延长到 )46。这种寿命的延长,正是DNA静电场延迟了三线态自由基对的反向电子转移(back-electron transfer, ),使其更稳定。相比之下,在脂质体中,蓝移的TAS信号则倾向于分子三线态而非自由基对,寿命也明显更短。
📈 突破3:几何构型对量子性能的决定性影响
量子化学模拟为上述现象提供了理论支撑。模拟结果显示,COE-CbzBP在:
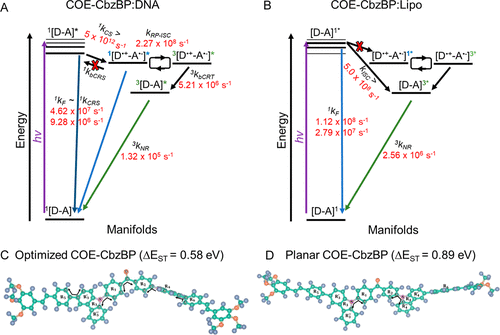
TICT优化构型(类DNA环境): 约为 。
平面限制构型(类脂质体环境): 飙升至 。
这意味着,从TICT到平面构型的转变,直接将 提高了约53%。
这一巨大的能隙差异,完全解释了为什么在脂质体这种僵硬环境中,SCRP无法形成。它强有力地证明了分子几何构型和局部静电场是决定COE-CbzBP量子比特行为的核心要素。
此外,为了排除环境粘度的影响(流变效应),研究人员在甘油溶液中进行了EPR实验。结果显示,高粘度只会导致EPR谱线增宽,而不是像DNA那样发生分裂。这最终锁定了结论:DNA的静电效应才是导致量子探针自旋动力学发生扰动的主导因素,而非简单的粘度或刚性。
🔮 应用展望、局限性与未来路线图:从检测DNA到量子信息科学
🧬 应用场景:量子生物探针的未来
这项研究不仅是一个化学或物理学的成就,它为量子生物传感开辟了全新的道路。
核酸环境的量子传感: COE-CbzBP可以直接利用DNA强大的静电场来产生一个独特且可测量的EPR信号分裂。这使其成为探测细胞核或线粒体等富含核酸环境中生物事件的理想探针。例如,它可以用来实时监测DNA的构象变化、损伤修复或与蛋白质的相互作用,这些过程都伴随着局部电场的微妙变化。
疾病诊断和药物筛选: 具备量子敏感度的探针,有望实现对疾病生物标志物(如特定突变的DNA序列)的超高灵敏度检测。药物与靶标DNA或蛋白质结合时的电场变化,也可以被精确量化,极大地加速药物筛选过程。
🚧 客观局限性与挑战
尽管取得了重大突破,但该研究仍存在一些局限性,指明了未来的努力方向:
信号强度与实际应用: 目前的CW-EPR信号是相对较弱的(相对于更成熟的固态NV中心)。虽然探针已证明了量子特性,但在复杂的、低浓度的真实细胞环境中,信号的信噪比和检测深度仍需提高。
TICT构型的控制: 探针的量子特性依赖于扭曲(TICT)构型。虽然水溶液中该构型是自发形成的,但要将其稳定且高效地引入到活体细胞等更复杂的环境中,还需要进一步的表面修饰和递送策略。
量子相干时间: 自由基对的寿命虽然长于普通激发态,但要达到真正的量子计算或长距离量子传输所需的相干时间(coherence time),还需要在分子设计上进行优化,以进一步减少环境扰动带来的去相干。
🗺️ 未来路线图:构建模块化分子量子体系
未来的工作将集中在利用这一设计原则,构建模块化的TICT-量子比特平台。通过替换供体(咔唑)和受体(二苯甲酮)的化学结构,科学家可以精确调控 和 的大小,从而将探针的最佳工作温度和电场灵敏度进行定制化设计。这一思路不仅服务于生物传感,更直接呼应了**量子信息科学(QIS)**对室温、溶液可处理的分子量子比特的需求。
这次的突破,象征着有机化学正在为量子技术贡献更灵活、更温和的解决方案。COE-CbzBP就像是打开了量子生物学新世界的一把钥匙,让我们对生命体内的 “电场语言” 有了前所未有的了解。这种从分子层面实现量子感知的能力,必将成为未来生命科学研究中最锋利的工具之一。