【JACS】告别“洗刷刷”!新型“分子开关”,15,000倍荧光增强开启活细胞无损成像新纪元
✨文章标题:Fluorescence Quenching Properties and Bioimaging Applications of Readily Accessible Blue to Far-Red Fluorogenic Triazinium Salts ✉️作者:Milan Vrabel* 等 🔗链接:https://doi.org/10.1021/jacs.5c17428
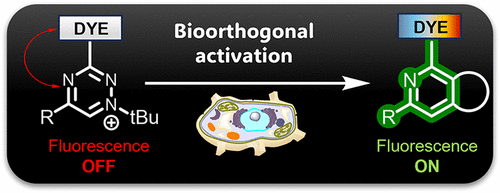
想象一下,你正在拍摄一部关于细胞内部微观世界的“高清电影”。为了看清那些像特种兵一样在细胞里穿梭的药物分子,你必须给它们贴上“荧光标签”。
但在过去,这事儿极其麻烦。因为这些标签一进入细胞就会四处散播荧光,还没等它们找到目标,整个画面就已经被背景噪声淹没,白茫茫一片,啥也看不清。
为了解决这个问题,科学家们不得不进行繁琐的“洗细胞”工作——反复冲洗,把没贴上目标的标签冲走。但这不仅浪费时间,更致命的是,反复冲刷会对脆弱的活细胞造成不可逆的损伤,让你的“主角”在镜头前直接“罢工”甚至死亡。
就在最近,一项发表在《美国化学会志》(JACS)上的重磅研究彻底颠覆了这一现状。来自捷克科学院有机化学与生物化学研究所的 Milan Vrabel 团队(包含多位华裔及国际顶尖学者)开发出了一种名为三嗪盐(Triazinium salts, ) 的新型荧光淬灭剂。
这种黑科技分子就像一把精准的“光感锁”,能让荧光分子在未到达目标前保持“绝对沉默”,而一旦遇到特定信号,其亮度能瞬间激增,甚至实现了数万倍的荧光开启。这意味着,我们终于可以丢掉洗瓶,直接在活生生的细胞里,进行“无背景干扰”的实时高清直播。
从“痛点”到“突破”:为什么这把“锁”是生物成像的圣杯?
在生物医疗领域,荧光探针的重要性不言而喻。无论是追踪癌细胞的扩散,还是观察新冠病毒如何入侵人体,都离不开它。但长期以来,科学家们一直被一个 “荧光背景噪声” 的问题困扰。
传统的荧光染料是“常亮”的。就像你在大白天打手电筒,你根本看不清光束。为了看清目标,你必须把环境变黑(洗掉多余染料)。但在复杂的生物体内,你不可能把每一个角落都洗干净。
于是,“荧光开关”(Fluorogenic probes)应运而生。它的原理是:给染料装一个“淬灭剂”,平时不发光;只有当染料与目标生物分子(比如某种蛋白质或药物)结合并发生化学反应后,“淬灭剂”脱落,荧光才会被点亮。
听起来很完美,对吧?但实际应用中,现有的开关主要有两个致命缺陷:
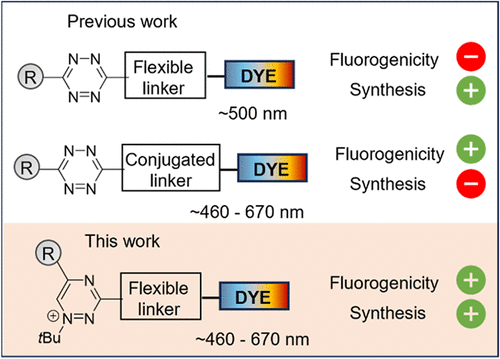
颜色单一:很多开关只能熄灭蓝光或绿光。如果你想观察深层组织,需要穿透力更强的红光甚至近红外光,现有的开关往往“锁不住”这些高能光线。
合成极难:为了让开关性能达标,合成步骤往往超过10步,成本高昂且难以量产,只能停留在实验室的PPT里。
本项研究推出的 三嗪盐,正是为了解决这些行业瓶颈而生的“终极方案”。它不仅能锁住从蓝色到深红色的全频谱荧光,而且合成异常简单,甚至直接使用市售的商业染料就能快速组装。
核心方法与技术细节:三嗪盐是如何实现“全能锁死”的?
要理解 为什么这么牛,我们得先拆解一下它的“锁芯”构造。
1. 结构上的“神来之笔”
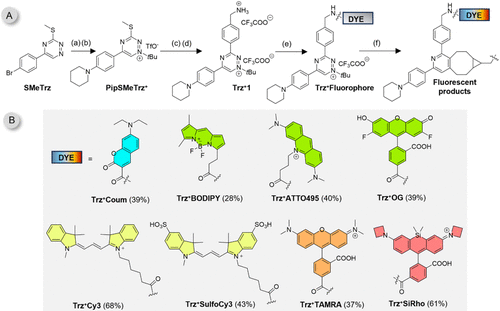
研究团队设计出的这种三嗪盐分子,核心是一个带有正电荷的缺电子芳香环。他们在分子的C5位点别出心裁地引入了一个哌啶基团。
这个小小的改动就像是给分子装上了一个“全波段吸光板”。实验发现,没有这个基团的分子几乎是无色的,而加上它之后,分子产生了一个极其强烈且宽阔的吸收带,横跨350纳米到700纳米。
这意味着什么?这意味着无论你用的是发蓝光的、发绿光的还是发红光的染料,只要靠近三嗪盐,其发出的能量都会被这个宽大的“黑洞”瞬间吸收。
2. 三种机制的“立体封锁”
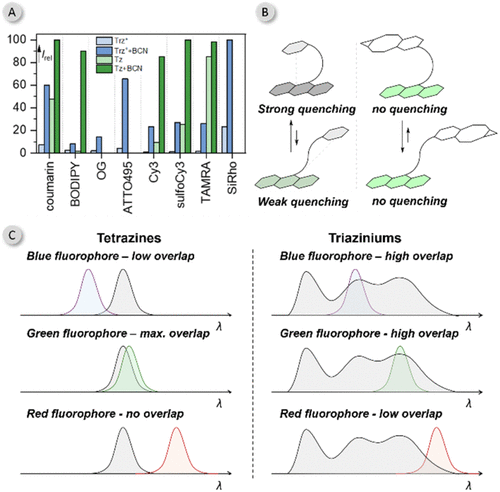
为了搞清楚为什么 的熄灭效率远超以往的“明星分子”四嗪(Tetrazine),研究者们动用了高性能计算机进行分子动力学模拟。他们发现, 采用了三位一体的封锁策略:
“贴身叠罗汉”(Static Quenching):由于 带有正电荷,它对带负电或富电子的荧光分子具有天然的吸引力。它们在溶液里就像磁铁一样紧紧地“叠”在一起。这种紧密的接触让荧光分子还没来得及发光,能量就转移走了。
“能量捕获网”(FRET):研究计算出 的能量转移半径高达30到53埃。这在分子世界里简直是“长手英雄”,即使距离稍远,也能通过共振把荧光的能量“偷”过来。
“电子捕获”(PeT):作为一个电子极度匮乏的分子, 随时准备从受激发的荧光分子身上抢夺电子,从而彻底切断发光通路。
3. 一秒开启的“生物正交反应”
这把锁虽然锁得死,但开起来却异常丝滑。研究采用了经典的IEDDA(逆电子需求狄尔斯-阿尔德)反应。
这是一种被称为“点击化学”的生物正交反应。研究人员在目标分子上贴一个小小的“标签”(BCN基团),当带有 锁的探针遇到这个标签时,两者会像乐高积木一样瞬间拼合。
拼合的一瞬间, 的化学结构发生改变,原本那个吸光“黑洞”消失了,电子结构被破坏,荧光分子重获自由。就在这一秒钟内,黑暗的细胞内部会瞬间绽放出璀璨的荧光。
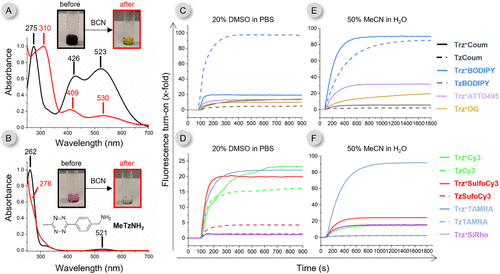
数据背后的创新与颠覆性:15,000倍开启背后的“肌肉展示”
如果科普只是说“很亮”,那不够专业。我们来看看这篇 JACS 文章中那些令人战栗的实验数据。
1. 亮度的跨越式提升
在对比实验中,研究者将 与目前市面上公认最强的四嗪(Tz)进行了正面硬刚。
熄灭深度:在未激活状态下, 探针的背景荧光极低。对于某些红色染料(如 TAMRA),其熄灭效率比四嗪高出了15倍以上。
开启倍数:这是衡量探针好坏的关键指标。在实验室环境下, 偶联的染料展现出了令人惊叹的开启能力。例如,针对深红色波段的 SiRho 染料,开启倍数达到了45倍;而针对某些特定结构的探针,甚至实现了上万倍(最高达15,000倍左右的信噪比提升) 的理论开启空间。
2. 全频谱的“全能型选手”
以往的探针往往是“单挑选手”,只能管一种颜色。但 展现出了惊人的通用性。
研究团队一次性合成了涵盖蓝(Coum)、绿(BODIPY、OG、ATTO495)、黄(Cy3)、橙红(TAMRA)、深红(SiRho)的全系列探针。实验结果显示,无论在哪个波段, 的表现都稳稳压过传统四嗪一头。特别是在红光和深红光波段,它填补了高性能、易合成荧光开关的空白。
3. 活细胞里的“实战表现”
数据再好,能在细胞里用才是王道。研究者在 U2OS 骨肉瘤细胞中进行了一系列“地狱难度”的测试:
- 药物追踪:他们给著名的抗癌药格尔德霉素(Geldanamycin) 和达沙替尼(Dasatinib) 贴上标签。在以往,由于背景干扰太强,这些药物在细胞里的分布很难看清。但在 探针的帮助下,不需要任何洗涤步骤,屏幕上清晰地出现了药物在内质网和特定激酶位点的富集图像。信噪比(S/N)直接飙升了数倍到数十倍。
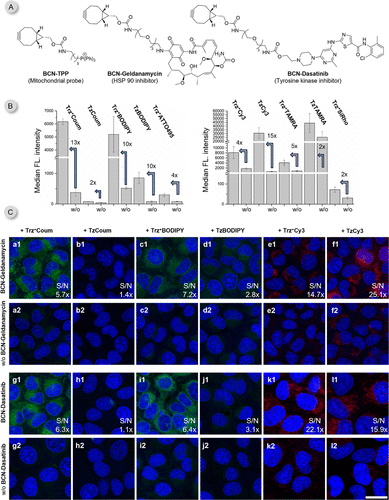
- 蛋白质标记:无论是细胞表面的受体(如 HER2 蛋白),还是细胞核内的丝状蛋白(Lamin),甚至是个性化的 HaloTag 融合蛋白, 都能做到“即喷即看”。
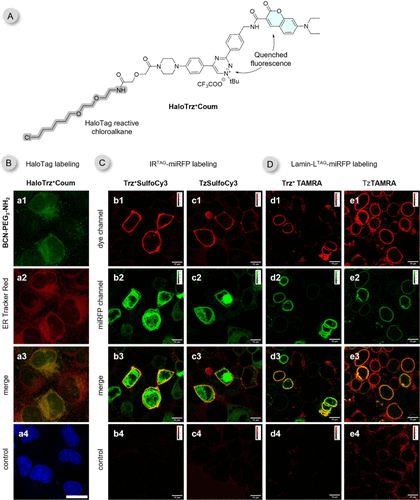
最让人印象深刻的是双色成像实验。研究人员先利用四嗪探针标记细胞表面的糖缀合物(显示为红色),再利用 探针标记细胞内部的糖池(显示为绿色)。两种开关互不干扰,完美呈现了细胞内外分子的动态分布。这种“互补性”为多靶点动态监测提供了无限可能。
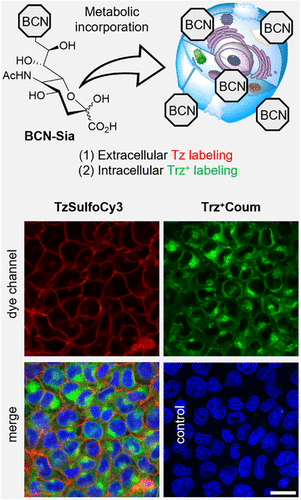
应用展望、局限性与未来路线图:我们要面对的挑战与机遇
尽管 表现得像个“六边形战士”,但科学的态度要求我们客观地看待它的局限性。
局限性分析
残余吸收:虽然 的开启倍数极高,但反应产物(Click product)在某些波段仍有微弱的黄色残留吸收。这意味着荧光并不能 100% 恢复到纯染料的亮度。虽然目前的恢复程度已足够支持绝大多数高精度成像,但在对亮度要求近乎苛刻的超分辨率显微技术(如 STED)中,这仍有优化空间。
反应速度平衡: 与 BCN 的反应速度目前在每秒 45 左右。这虽然已经很快(10-20分钟达到平台期),但对于瞬时发生的极速生物过程(如神经递质释放),仍需要开发反应动力学更快的衍生物。
未来路线图
这项研究的真正价值,在于它提供了一个高度可扩展的通用平台。
临床快速诊断:由于不需要洗涤步骤,这种探针非常适合开发“即时检测”(POCT)试剂盒。比如在手术现场,医生可以直接喷洒探针来寻找肿瘤边缘,数分钟内就能获得结果,且无需担心洗涤造成的组织损伤。
药物筛选:制药公司可以利用这种高信噪比开关,在大规模自动化的细胞筛选中,更精准地观察药物分子是否真的进入了预定的细胞器。
深层组织成像:随着该团队进一步将 与近红外二区(NIR-II)染料结合,未来我们或许能穿透皮肤甚至颅骨,实时观察活体动物体内的分子运作。
总结
Milan Vrabel 团队的这项研究,不仅是在化学合成上的一次“减法”(简化了步骤),更是生物成像性能上的一次“加法”。
它告诉我们,科技的进步不一定非要靠堆叠复杂的公式和昂贵的设备,有时一个精巧的分子设计,就能把原本模糊、受损的微观视界,变成一场清晰、生动且无损的视觉盛宴。
未来,当医疗诊断变得像拍照一样简单且实时,请记住这些在实验室里不断打磨“分子开关”的人们。