【JACS】1小时检出10个细菌!AIE材料打造“液体镜片”,颠覆百年病原体检测法
✨文章标题:Fluorescence Transduction of Liquid Crystal Ordering Transitions for Biosensing ✉️作者:Alberto Concellón* 等 🔗链接:https://doi.org/10.1021/jacs.5c16679
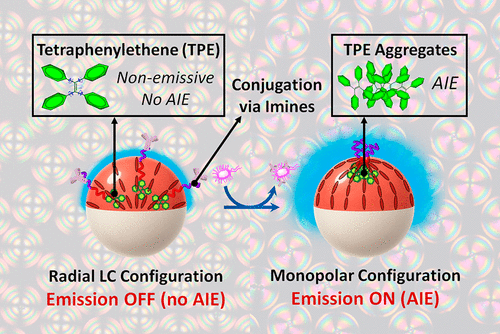
当液晶遇到荧光,生物传感的灵敏度极限被再次刷新。
在食品安全和临床诊断领域,如何快速、准确地捕获微量的病原体,一直是一个巨大的挑战。传统方法往往需要数小时甚至数天的培养扩增,步骤繁琐,且依赖大型仪器。有没有一种方法,能像测血糖一样简便,却能灵敏地捕捉到液体中极微量的细菌呢?
近日,国际顶级期刊《美国化学会志》(JACS)发表了一项突破性研究,科学家们巧妙地将液晶材料与荧光技术结合,开发出一种高灵敏度的生物传感器。该技术仅需约1小时,就能检测出每毫升液体中低至10个的沙门氏菌,灵敏度比传统液晶传感方法提升高达1000倍,为快速病原体检测打开了新的大门。
从“痛点”到“突破”
当前生物传感技术的核心痛点,在于“信号转导”的便携性与定量能力。
许多先进的传感器虽然灵敏度高,但其读出的信号(如需要偏振光显微镜观察的光学纹理变化)难以量化,且依赖笨重的专业设备,极大地限制了其在现场、基层的应用。
液晶,这种我们熟悉又陌生的物质,正是解决这一痛点的理想候选者。 它既像液体一样可以流动,又像晶体一样具有分子的方向性排列(即“取向序”)。这种独特的“软”秩序使得液晶对外界刺激极其敏感,尤其是其表面发生的分子级事件,能被放大为肉眼可见的光学变化。
过去二十多年,基于液晶的生物传感器不断发展,但其读出方式始终局限于偏振光显微镜。研究者需要透过复杂的纹理图案来判断结果,难以精确量化,更无法实现便携式检测。
这项研究的颠覆性突破在于,它成功地为液晶的有序性转变“翻译”了一种全新的语言——荧光。 研究团队设计了一种智能高分子表面活性剂,使其能在液晶微滴中根据不同的有序状态,自动切换荧光信号的“开”与“关”。从而将复杂的液晶拓扑结构变化,转化为简单、可直接用便携式荧光仪读取的定量光信号。
这一突破,相当于为强大的液晶传感系统装上了一枚“傻瓜式”的指示灯,使其从实验室的深闺走向广阔的实际应用成为可能。
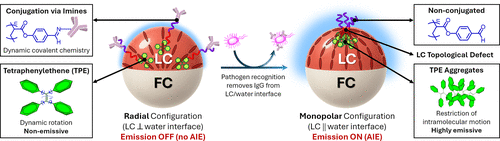
核心方法:给液晶装上“荧光开关”
那么,这个精巧的“荧光开关”是如何实现的呢?关键在于两大核心设计:“智能聚合物” 和 “Janus微滴反应器”。
智能聚合物:集探测、信号转换于一身
研究团队设计了两种结构相似的两亲性嵌段共聚物(P1和P2)。它们就像一个个微小的“潜水员”,一部分喜欢待在疏水的液晶中,另一部分则喜欢亲水环境。
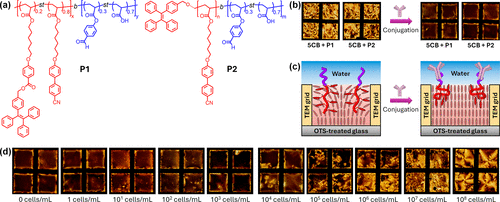
这些“潜水员”的非凡之处在于:
动态共价“抓手”:其亲水端带有醛基,能够通过可逆的亚胺化学与抗体(如抗沙门氏菌IgG)上的氨基发生反应。这种连接既牢固又可逆,为后续的竞争性置换埋下伏笔。
聚集诱导发光(AIE)“信号灯”:其疏水端引入了四苯基乙烯(TPE) 基团。TPE有一个神奇的特性:当分子分散时,它不发光;但当分子聚集在一起,运动受限时,就会发出强烈的荧光。这正是信号的来源。
聚合物结构的设计暗藏玄机。 P1将TPE作为侧基无规分布在链上,而P2只在末端连接一个TPE。这一差异导致了它们在后续性能上的显著区别。
Janus微滴:纳米级缺陷的放大效应
研究没有使用简单的液晶液滴,而是构建了更为复杂的 “Janus乳液”。每个微滴内部是“一分为二”的:一半是向列相液晶(5CB),另一半是氟碳油(FC)。
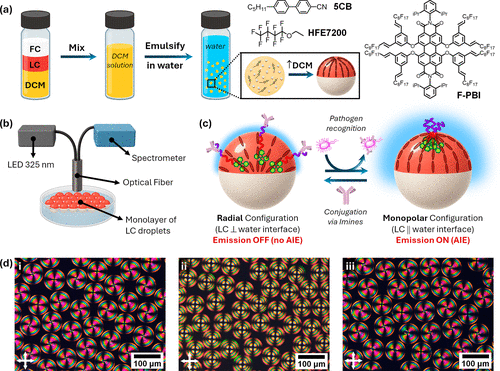
这种结构之所以强大,是因为液晶在球形约束下会产生拓扑缺陷——即分子排列方向无法定义的特殊点。Janus微滴中的液晶可以呈现两种关键构型:
径向构型:聚合物均匀分布在液晶与水的整个界面上,分子分散,TPE不发光,此为 “关”状态。
单极构型:聚合物被驱动并富集在尺寸仅约10纳米的拓扑缺陷点,TPE高度聚集,发出强烈荧光,此为 “开”状态。
整个传感过程如同一场精彩的“分子拔河”比赛:
初始状态(OFF):智能聚合物携带抗体,修饰在Janus微滴表面。此时液晶为径向构型,聚合物均匀分布,荧光关闭。
识别状态(ON):当目标病原体(如沙门氏菌)出现,其表面的抗原会与抗体发生更强结合,将抗体从聚合物“抓手”上竞争性地“拔”走。
信号转换:抗体的脱落导致聚合物在界面上的构象改变,触发液晶从径向构型向单极构型转变。聚合物瞬间聚集到缺陷点,TPE发光,信号开启。
这一设计将生物识别事件(抗体-抗原结合)与物理有序性转变(液晶构型变化)和信号放大(AIE荧光)三级放大效应串联起来,实现了对极低浓度病原体的超高灵敏度检测。
数据背后的创新与颠覆性
实验数据有力地证明了该平台的卓越性能。
灵敏度:突破极限,达到10 cells/mL
研究人员用灭活的沙门氏菌(HKST)进行了测试。如图4所示,随着细菌浓度的增加,荧光强度(对于性能更优的P2聚合物)呈现出清晰的剂量依赖性增强。
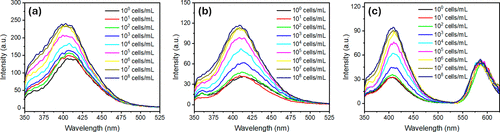
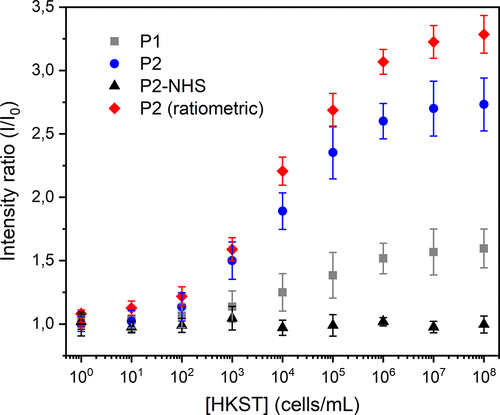
最关键的是检测限的突破。 基于P2聚合物的传感器,检测限达到了惊人的每毫升10-100个细菌(10-10² cells/mL)。相比之下,基于传统偏振光读出的液晶薄膜传感器,检测限通常在10⁴-10⁵ cells/mL。这意味着新方法的灵敏度提升了整整1000倍。
P2为何优于P1? 数据表明,P2在“关”状态下的荧光本底更低,信噪比更高。这是因为末端的单个TPE在界面分散时更不易发生非特异性聚集,而P1的侧基TPE则容易“漏光”。这体现了分子水平设计的精确性对整体性能的决定性影响。
特异性与可靠性:双重保险
任何优秀的传感器都必须具备高特异性。控制实验证实,只有使用特异性抗体时,才能观察到细菌触发的荧光信号。使用非特异性抗体或使用形成不可逆连接的聚合物,均无响应。
更巧妙的是,研究者引入了“比率型检测”来提升可靠性。 他们在Janus微滴的氟碳油相中加入了一种惰性的参考染料(F-PBI)。检测时,同时读取TPE的荧光(信号)和参考染料的荧光(内标),并计算两者的比值。
这种方法可以自动校正微滴数量、光照强度波动等变量带来的误差,使得即使在液滴大小不一的混合物中,也能获得稳定、可重复的定量结果,大大降低了实际应用的难度。
颠覆性意义:从“看纹理”到“读数字”
这项工作的颠覆性体现在三个层面:
读出方式的革命:将液晶传感从依赖专家判读的“看纹理”时代,推进到了仪器自动“读数字”的时代。这使得快速、定量、便携的检测成为可能。
信号放大策略的创新:首次将AIE现象与液晶拓扑缺陷的分子富集效应相结合,创造了一种全新的信号放大路径,实现了极高的灵敏度。
平台的通用性与模块化:其核心原理是通用的。只需更换聚合物上所连接的抗体类型,理论上就可以检测任何一种病原体或生物分子,如新冠病毒、大肠杆菌、癌症标志物等。
应用展望、局限性与未来路线图
尽管这项技术前景广阔,但走向实际应用仍需克服一些挑战,并沿着清晰的路线图前进。
潜在应用场景
食品安全现场快检:用于餐饮、食品加工厂对沙门氏菌、李斯特菌等的快速筛查。
水质监测:实时监测饮用水或环境水中的病原体污染。
床边诊断(POCT):开发成便携式检测卡或设备,用于诊所、社区医院对传染病的快速诊断。
生物反恐与安全:检测空气中的生物威胁剂。
当前局限性
复杂样本基质干扰:研究指出,高浓度的非靶标蛋白(如牛血清白蛋白)可能会与抗体竞争结合位点,从而降低检测灵敏度。在实际样本(如血液、食物匀浆)中,可能存在更多干扰物质。
可逆连接的稳定性:动态亚胺键在复杂化学环境中的长期稳定性需要进一步验证。
大规模生产与标准化:智能聚合物的合成与Janus微滴的大规模、均一化制备是产业化的技术门槛。
未来发展路线图
短期(1-3年):优化聚合物结构,开发对复杂样本基质抗干扰能力更强的探针。例如,使用比亚胺键更稳定、特异性更高的动态共价化学。
中期(3-5年):与微流控技术结合,实现Janus微滴的高通量、标准化生产,并集成成一次性检测芯片。
长期(5年以上):开发多靶标同时检测(多重检测)平台,并探索将其与智能手机摄像头结合,打造真正低成本、便携式的居家诊断设备。
结语
这项研究不仅是液晶传感领域的一个技术突破,更展示了跨学科融合的强大力量。它巧妙地将高分子化学、软物质物理、光学和生物检测技术融为一体,将一个原本复杂的科学现象,变成了一个简单可靠的解决方案。
正如研究人员所言,这项工作为液晶有序性转变的荧光转导建立了一个可推广的、便携的传感范式。当科学家们成功地为这些敏感的“液体镜片”配上了会说话的“荧光指示灯”,我们距离随时随地、快速洞察微观病原世界的那一天,无疑又近了一大步。