【JACS】突破1500纳米:电子对称性调控的铒(III)-酞菁复合物实现高分辨率体内生物传感
文章标题:Electronic-Symmetry-Tuned Emission Beyond 1500 nm in Erbium(III)-Phthalocyanine Complexes for High-Resolution In Vivo Biosensing
通讯作者:Shangfeng Wang, Fan Zhang
文章链接:https://doi.org/10.1021/jacs.5c13688
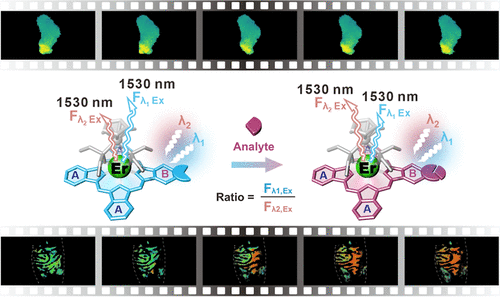
文章概要
引言与研究背景
在生物医学成像领域,如何在复杂的组织环境中实现高分辨率、低背景的体内化学传感一直是重大挑战。近红外二区(NIR-II,1000–2000 nm)尤其是超过1500 nm的波段,因其散射减少和自发荧光极低,被认为是理想的成像窗口。然而,迄今为止尚无分子探针能够在这一波段实现有效的体内传感。本研究提出了一种全新的策略:通过电子对称性调控(Electronic-Symmetry-Tuned Emission, ESTE),在单功能化的铒(III)-酞菁复合物中实现超过1500 nm的高亮度发射,从而建立了一个可用于动态、定量和解剖分辨的分子传感平台。
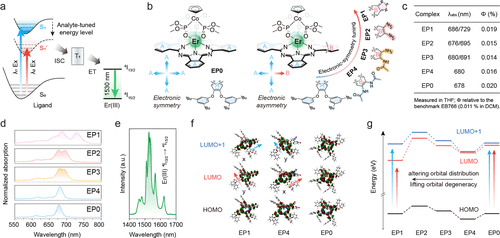
核心机制:电子对称性调控
研究团队合成了对称型(EP0)和非对称型(EP1–EP4)铒(III)-酞菁复合物。通过在外围芳香环引入不同取代基,打破分子电子对称性,进而改变激发光谱,而保持1530 nm的单带发射。该机制的关键在于配体三重态能量向铒离子的高效转移(效率超过80%),并通过对称性扰动实现激发依赖的发射强度调控。这种对称性控制的激发光谱调节定义了ESTE机制,为分子探针的设计提供了普适原则。
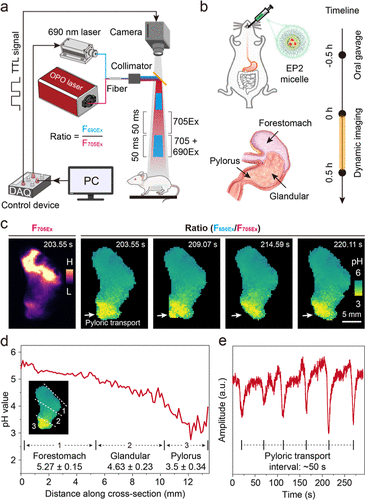
pH传感的验证
研究者选择了含有邻苯二胺取代基的EP2作为模型探针。该分子在不同pH条件下表现出明显的激发光谱变化:在酸性环境下,电子对称性恢复,导致激发峰由双峰转为单峰。通过690 nm与705 nm双波长激发,EP2实现了线性比率型1530 nm发射响应,从而能够精确反映pH变化。在组织散射模拟实验中,探针在不同深度仍保持稳定的比率信号,证明其在复杂环境下的可靠性。进一步的动物实验显示,EP2能够动态监测小鼠胃部的pH分布,揭示了进食与禁食状态下胃酸分泌和蠕动的差异。
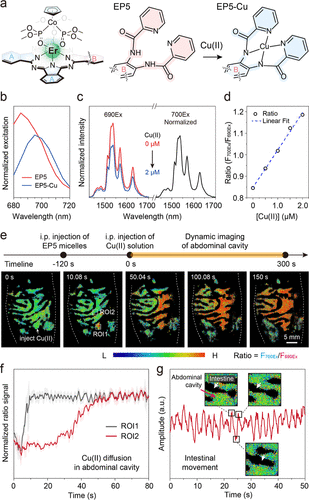
铜离子传感的扩展
为了验证ESTE机制的普适性,研究团队设计了含有二吡啶甲酰胺基团的EP5,用于响应Cu(II)。该探针在与铜离子结合后激发光谱发生红移,并在690 nm与700 nm激发下表现出线性比率型1530 nm发射响应。动物实验显示,EP5能够高分辨率地追踪小鼠腹腔中铜离子的扩散动态,甚至清晰描绘肠道轮廓和蠕动频率。这一成果展示了该平台在金属离子动态监测中的潜力。
技术优势与性能对比
与传统有机染料相比,这些铒(III)-酞菁复合物具有显著优势:
- 发射亮度提升约20倍;
- 发射寿命延长至微秒级,比常规染料高出五个数量级;
- 在体内条件下表现出良好的稳定性与低毒性。
这些性能使其成为突破1500 nm波段的首个分子探针平台,能够在深层组织中实现高分辨率、定量化的化学与生理过程成像。
结论与展望
本研究首次提出并验证了电子对称性调控的分子发光机制,成功在超过1500 nm的波段实现了体内高分辨率生物传感。通过设计不同的单功能化酞菁复合物,研究者不仅实现了pH和Cu(II)的动态监测,还为未来开发更多响应性探针提供了通用策略。这一平台有望推动深层组织化学过程的研究,并在疾病诊断、药物递送和代谢监测等领域发挥重要作用。
综上所述,该工作不仅在分子光学探针设计上提出了新的理论框架,也在实际应用中展示了突破性的成果,为NIR-II成像和体内生物传感开辟了新的方向。