【J. Med. Chem.】10项结构优化造就新一代长效胰淀素类减重药:Petrelintide研究全解读
文章标题:Development of Petrelintide: a Potent, Stable, Long-Acting Human Amylin Analogue
通讯作者:Henrik Fischer Munch
文章链接:https://doi.org/10.1021/acs.jmedchem.5c01185

文章概要
近年来,肥胖症已成为全球公共健康危机,2022年全球约有8.9亿成年人患有肥胖。尽管GLP-1类药物如semaglutide和tirzepatide在减重方面取得显著疗效,但副作用和耐受性问题导致约半数患者在治疗6个月内停药。因此,开发作用机制不同、稳定性更高、可与现有药物联合使用的新型减重药物成为迫切需求。
胰淀素(amylin)是一种由胰岛β细胞分泌的37个氨基酸多肽,具有延缓胃排空、抑制胰高血糖素分泌和增强饱腹感等作用,是调节能量平衡的关键激素。然而,天然胰淀素在水溶液中易聚集成纤维状结构,化学稳定性差,半衰期短,限制了其药用潜力。2005年FDA批准的短效胰淀素类似物pramlintide需每日多次注射,且只能在酸性条件下配制,使用不便。
本研究报道了新一代胰淀素类似物Petrelintide的开发过程。研究团队以人胰淀素为骨架,通过多轮结构优化,成功设计出一种具有高效能、长效性、化学稳定性强且可在中性pH条件下配制的肽类药物。其关键改进包括:
- 防止纤维化:采用N-甲基化修饰Gly24和Ile26,替代传统的引入脯氨酸策略,有效抑制β-淀粉样纤维形成。
- 增强受体活性:将C端氨基酸由酪氨酸替换为脯氨酸或羟脯氨酸,显著提高对胰淀素受体(AMY3R)和降钙素受体(CTR)的激动效力。
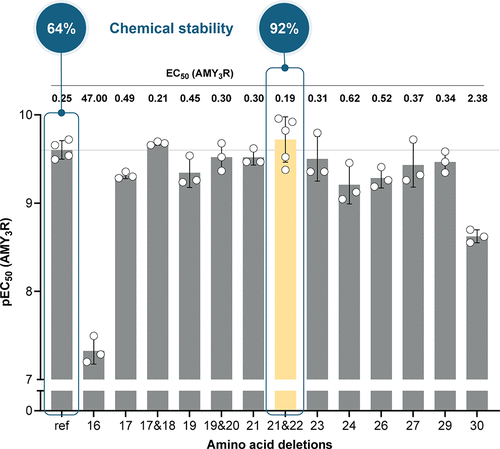
- 提升化学稳定性:删除易脱酰胺的Asn21和Asn22,并替换其他易降解的天冬酰胺和谷氨酰胺残基,使化学稳定性从原始胰淀素的40%提升至90%以上。
- 解决二聚体问题:发现原始分子在中性pH下易形成二聚体,通过将Cys2-Cys7的二硫键替换为更稳定的内酰胺桥(lactam bridge),彻底消除二聚体生成。
- 优化内酰胺桥结构:系统评估桥长和酰胺键位置,发现酰胺键靠近第2位氨基酸且桥长为6–8原子时,受体活性最佳。
- 保持高水溶性:所有优化后的肽类在pH 7或7.5条件下均可溶解超过200 μM,适合皮下注射。
- 延长半衰期:在大鼠体内,Petrelintide的半衰期达33.8小时,远超pramlintide,支持每周一次给药。
- 显著减重效果:单次注射Petrelintide可使大鼠体重在96小时内减少约10%;在肥胖模型中,每隔一天注射15 nmol/kg,20天内累计食物摄入减少23.6%,体重增长控制在4.4%以内(对照组为16.9%)。
- 中性pH配方兼容性:Petrelintide在多种缓冲体系(pH 6.1–7.4)中稳定性良好,无纤维化或聚合现象,适合与semaglutide等药物联合配制。
- 联合配方稳定性验证:与semaglutide共配制后,Petrelintide的降解速率和粒径无显著变化,证明其具备联合治疗潜力。
综上所述,Petrelintide通过多项结构优化,成功克服了胰淀素类药物在稳定性、配方兼容性和药效持续性方面的瓶颈。其在体内外均表现出优异的药理特性,已进入临床II期试验阶段,未来有望成为肥胖治疗领域的重要新药,尤其适用于与GLP-1类药物联合使用,实现更高效、更持久的减重效果。