🔬【JACS】突破3大瓶颈!14种新型短波近红外(SWIR)荧光染料助力多通道活体成像革命
文章信息
📚文章标题:Excitation-Matchable Shortwave Infrared Quinolinium Fluorophores: Decoding Spatiotemporal Interactions with Multiplexed Bioimaging 作者:Yongkang Yao等 期刊:Journal of the American Chemical Society 链接:https://doi.org/10.1021/jacs.5c10749
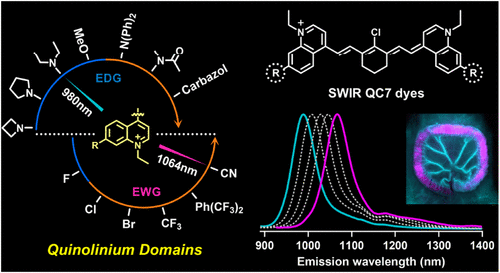
短波红外(SWIR, 1000–2000 nm)成像技术因其深组织穿透力和低背景干扰,正逐步成为多通道活体生物成像的理想选择。然而,传统染料在亮度、光谱分离度和激光兼容性方面存在显著限制,严重制约了其在复杂生物体系中的应用。近期,《美国化学会志》发表的一项研究提出了突破性解决方案:构建一个包含14种新型染料的SWIR荧光库,基于可调节的喹啉阳离子骨架,实现了激发波长可匹配的多通道成像,为解码时空生物交互提供了强有力的工具 1。
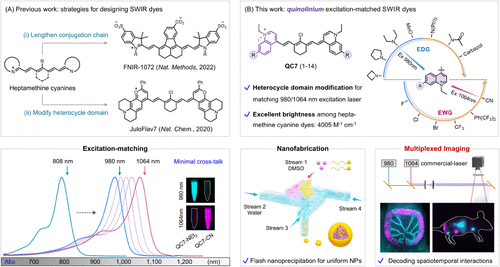
🧪一、从“染料核心”出发:构建可调节的喹啉阳离子骨架
传统SWIR染料多依赖吲哚类结构,其激发波长集中在780–800 nm,难以实现多通道成像。本研究创新性地引入喹啉阳离子作为“染料核心”,通过系统性电子给/吸修饰,成功合成了14种喹啉衍生物,仅需两步反应,原料易得,合成简便。
这些衍生物与七甲链结合后,形成了一系列喹啉基SWIR氰碱染料(QC7系列),其最大吸收波长覆盖975–1046 nm,涵盖了980 nm和1064 nm两种常见激光波段。其中,QC7-NEt₂在980 nm激发下亮度最高,而QC7-CN则在1064 nm激发下表现最佳,构成了理想的正交激发染料对。
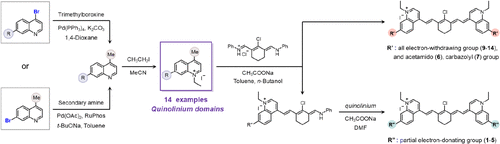
🌈二、光谱调控与亮度优化:实现高分辨率成像
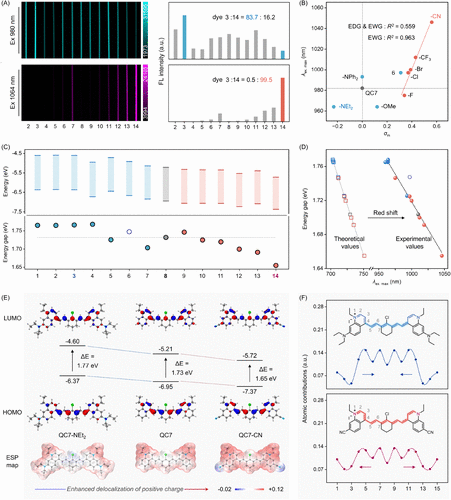
研究团队通过Hammett参数分析和密度泛函理论(DFT)计算,系统揭示了不同取代基对染料吸收波长的影响规律。电子吸基(如氰基)可显著红移吸收峰,而电子给基则影响较小。
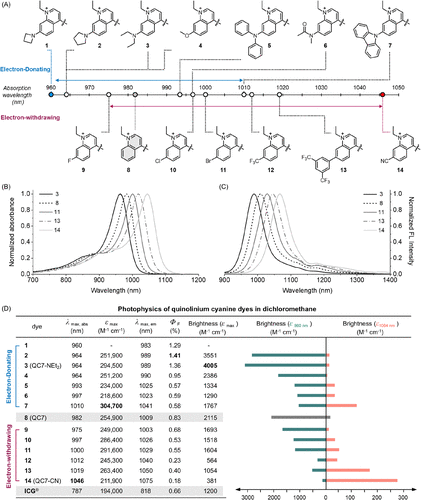
在亮度方面,QC7-NEt₂的亮度高达4005 M⁻¹·cm⁻¹,在N-杂环七甲氰碱染料中处于领先水平。通过宽场成像实验验证,在980 nm激发下,QC7-NEt₂信号强度远高于QC7-CN;而在1064 nm激发下,QC7-CN则几乎独占信号。这种显著的激发差异确保了多通道成像中的低串扰。
⚗️三、闪蒸纳米沉淀法(FNP):制备高均一性荧光纳米颗粒
为解决染料在水中溶解性差的问题,研究采用FNP技术将染料包封于PLGA-b-PEG聚合物中,制备出粒径均一、亮度增强的荧光纳米颗粒。与传统超声沉淀法相比,FNP制备的颗粒在粒径、分散性和亮度方面均表现更优:
- QC7-NEt₂颗粒平均直径从172 nm优化至115 nm,亮度提升1.7倍;
- QC7-CN颗粒平均直径从148 nm优化至112 nm,亮度提升1.4倍。
这种高性能纳米颗粒为活体成像提供了稳定可靠的探针载体。 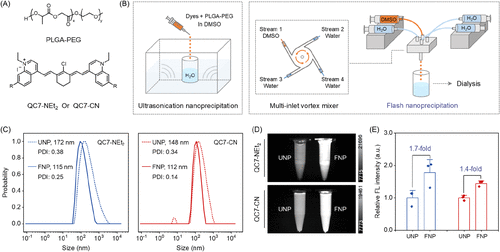
🐭四、活体成像实证:血管、淋巴、肠道一网打尽
研究在小鼠模型中进行了多种成像实验,展示了染料在不同组织中的应用潜力:
血管成像:静脉注射QC7-NEt₂后,可清晰观察全身血管网络,包括腹部毛细血管和脊柱静脉,分辨率高达百微米级。
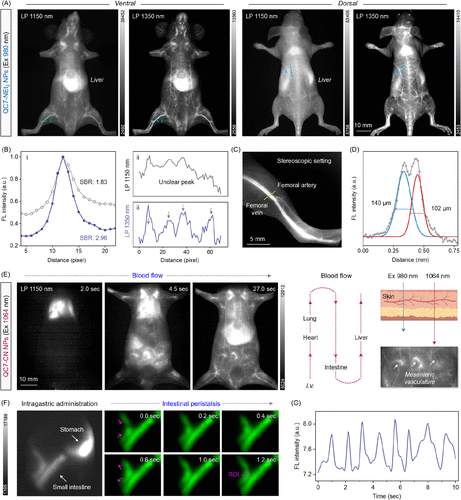
肠道成像:口服QC7-CN后,可动态追踪肠道蠕动过程,清晰显示胃、小肠、回盲部等结构。
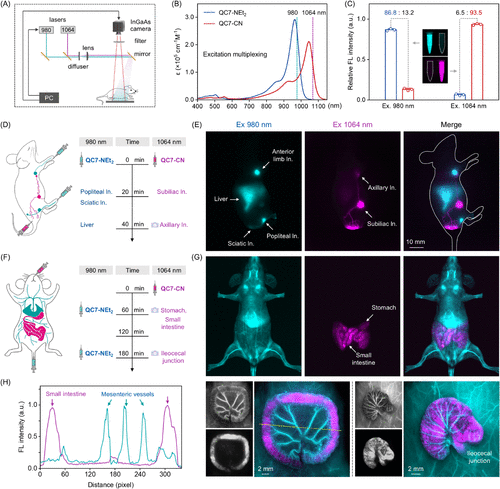
淋巴成像:通过不同注射部位实现前肢、后肢和股部淋巴结的双通道成像,展示了淋巴系统的精细结构。
这些成像结果均在980 nm和1064 nm激光激发下实现,验证了染料对的正交激发能力和低串扰特性。
🎯五、三通道成像初探:引入ICG拓展成像维度
在QC7-NEt₂和QC7-CN的基础上,研究进一步引入临床常用染料ICG(808 nm激发),构建三通道成像体系。通过不同注射方式,分别标记肝脏、淋巴系统和肠道,实现了三维空间的生物分布可视化,为复杂生理过程的研究提供了新工具。 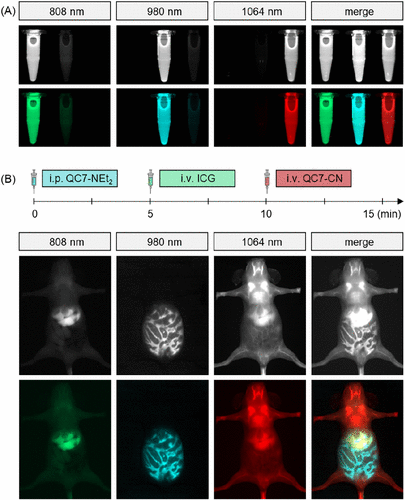
🧭六、总结与展望:开启SWIR成像新纪元
本研究通过构建14种喹啉基SWIR染料,突破了传统染料在亮度、光谱分离度和激光兼容性上的三大瓶颈。其合成简便、性能优异、适配商业仪器,具备广泛的应用潜力。未来,这一染料库有望在肿瘤转移、免疫细胞迁移、血管功能评估等领域发挥重要作用,推动SWIR成像技术迈入多通道、高分辨率、动态可视的新纪元。