文章信息
📚文章标题:Metabolic Hijacking by Engineered Probiotics Reprograms Tumor Metabolism and Immune Microenvironment for Self-Reinforcing Photodynamic Immunotherapy 作者:Shurong Qin等 期刊:Journal of the American Chemical Society 链接:https://doi.org/10.1021/jacs.5c10242
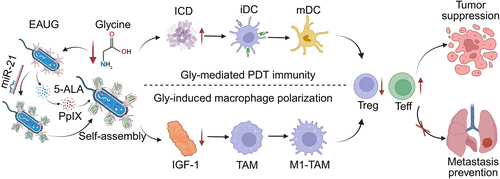
🚀【JACS】“双重打击”:1种益生菌+1种纳米材料,激活5种免疫机制,实现超90%肿瘤抑制率!
癌症治疗正迎来一场革命性突破。近日,《美国化学会志》发表了一项前沿研究,展示了一种由工程化益生菌与纳米材料构成的混合系统,能够同时“劫持”肿瘤代谢并激活免疫系统,实现自增强光动力免疫治疗(PDT)。本文将为您详细解读这一创新策略的设计原理、实验结果及其在肿瘤治疗中的潜力。
🧬1种益生菌如何“劫持”肿瘤代谢?
研究团队以常见益生菌——大肠杆菌Nissle 1917(EcN)为基础,进行基因工程改造,使其具备两个关键能力:
- 表达谷氨酰-tRNA还原酶(hemA)和苹果酸合酶B(maeB),可合成5-氨基乙酰丙酸(5-ALA),这是光敏剂PpIX的前体;
- 通过微流控芯片筛选,使其能以甘氨酸为唯一碳源生长,从而在肿瘤微环境中高效消耗甘氨酸。
甘氨酸在肿瘤中高度富集,是抗氧化剂谷胱甘肽(GSH)的合成原料。该菌株通过“吃掉”甘氨酸,削弱肿瘤细胞的抗氧化防御,为后续光动力治疗创造条件。
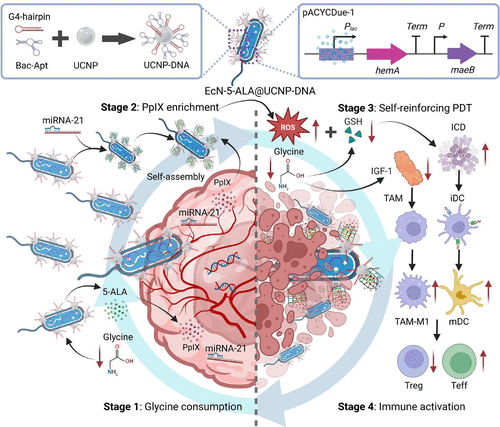
💡1种纳米材料如何精准释放光敏剂?
研究者将上述益生菌与上转换纳米粒子(UCNP)结合,构建出名为EAUG的混合系统。UCNP具备以下功能:
- 响应近红外光(980 nm)激发,释放可激活PpIX的可见光;
- 表面修饰了miRNA-21响应的G4-发夹DNA结构,能在肿瘤细胞中形成G-四链体,捕获并富集PpIX;
- 同时携带细菌适配体,实现与益生菌的稳定结合。
这一设计确保PpIX在肿瘤内高效积累,并在外部光照下释放大量活性氧(ROS),诱导肿瘤细胞死亡。 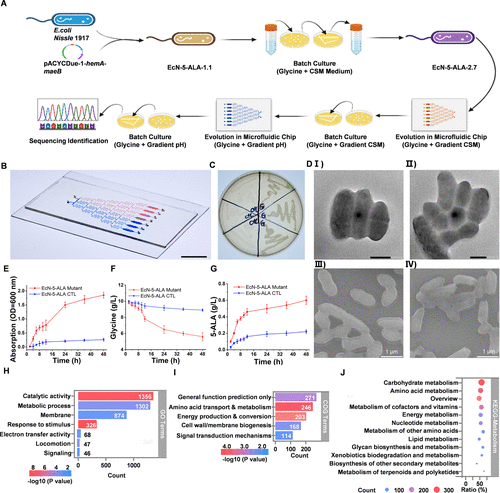
🔥双重代谢重编程,激活5种免疫机制
EAUG系统不仅直接杀伤肿瘤细胞,还通过代谢干预和ROS诱导,激活多种免疫机制:
- 免疫原性细胞死亡(ICD):ROS诱导HMGB1释放,促进抗原呈递;
- 树突状细胞(DC)成熟:CD80/CD86表达显著上升;
- 巨噬细胞极化:甘氨酸耗竭降低IGF-1表达,促使M2型向M1型转化;
- 效应T细胞激活:CD8+ T细胞数量显著增加;
- 调节性T细胞(Treg)抑制:Treg比例明显下降,减轻免疫抑制。
这一“代谢+免疫”双重打击策略,构建了一个自增强的抗肿瘤免疫循环。 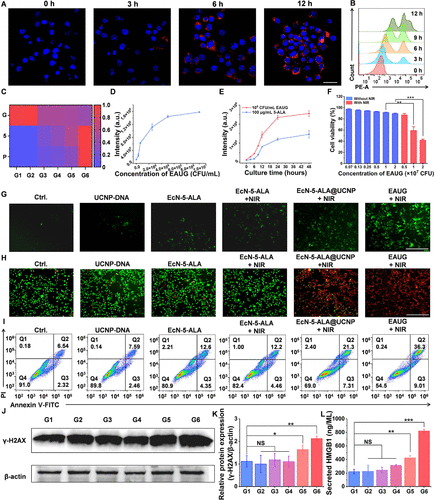
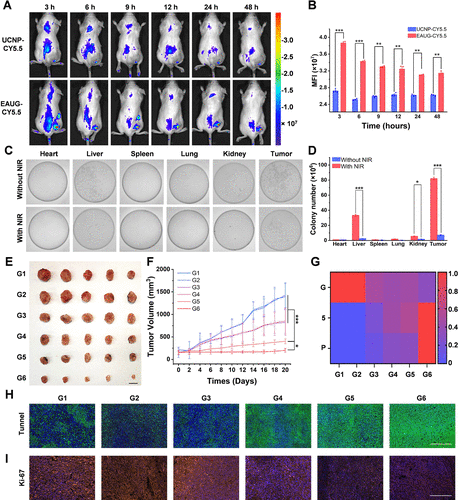
🧪体内实验:肿瘤抑制率超90%,转移显著减少
在小鼠乳腺癌模型中,EAUG系统展现出卓越的治疗效果:
- 肿瘤体积在21天内显著缩小,G6组(EAUG+NIR)抑制率超过90%;
- TUNEL和Ki-67染色显示肿瘤细胞凋亡和增殖显著减少;
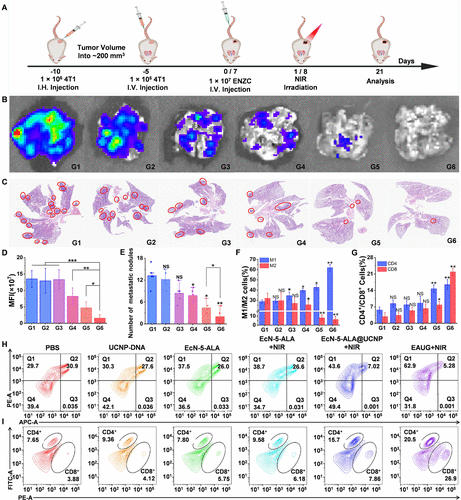
- 肺转移模型中,EAUG组肺部结节数量显著减少,生存期显著延长;
- 体重和器官组织学分析显示治疗安全性良好,无明显毒性。
🌐未来展望:从实验室走向临床的关键一步
EAUG系统的成功,标志着代谢重编程与光动力治疗的深度融合。其优势包括:
- 高度特异性:通过miRNA-21响应和甘氨酸代谢,实现肿瘤靶向;
- 可控性强:外部光照可精确调控治疗时间和强度;
- 免疫协同:激活多种免疫细胞,构建持久抗肿瘤反应;
- 安全性高:益生菌来源天然,纳米材料可控释放,副作用低。
未来,该策略有望拓展至其他肿瘤类型,结合免疫检查点抑制剂或CAR-T疗法,打造多模态癌症治疗平台。
📌结语:1种益生菌+1种纳米材料,开启癌症治疗新纪元
这项研究不仅展示了微生物工程与纳米技术的协同潜力,更为癌症治疗提供了一个可控、安全、高效的新范式。随着技术成熟与临床验证的推进,EAUG系统或将成为下一代肿瘤治疗的核心武器。