【Angew.Chem.】 光驱动癌细胞焦亡:单激子驱动的细胞内光氧化还原催化研究
文章标题:Singlet Exciton Drives Intracellular Photoredox Catalysis for Pyroptosis in Cancer Cells
通讯作者:Xiaojun Peng
文章链接:https://doi.org/10.1002/anie.202525323
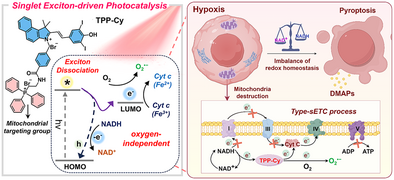
文章概要
引言
光动力治疗(PDT)是一种依赖光敏剂(PS)产生活性氧(ROS)来杀伤病变细胞的精准治疗方式。然而,肿瘤组织常处于缺氧状态,传统依赖氧的光敏剂在此环境下疗效显著下降,导致耐药与复发问题。尽管已有研究尝试通过携氧纳米载体或联合缺氧激活前药来改善,但仍存在毒副作用和复杂调控难题。为突破这一瓶颈,研究团队提出了基于单激子驱动的新型光氧化还原催化机制(Type-sETC),并设计了线粒体靶向光敏剂TPP-Cy,实现了在缺氧条件下依然高效的光催化治疗。
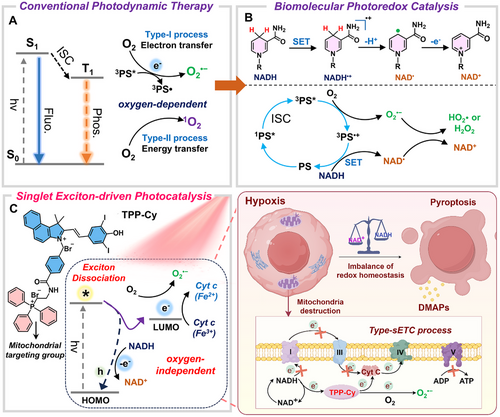
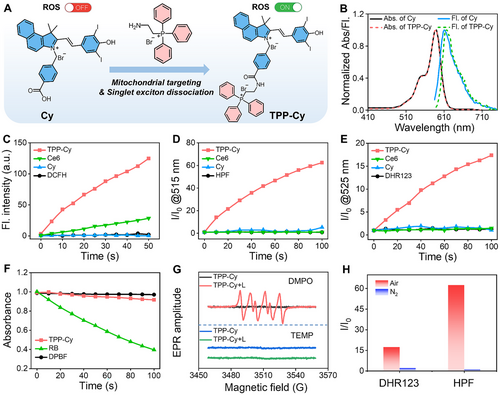
主要实验及结论
研究首先通过结构修饰将TPP基团引入碘花青染料,赋予其线粒体靶向能力。实验表明,TPP-Cy在光照下能高效产生活性自由基(•OH与O₂•⁻),并直接催化关键线粒体分子NADH与细胞色素c(Cyt c),打断电子传递链(ETC),引发能量危机。与传统三重态依赖的光敏剂不同,TPP-Cy通过单激子解离实现电子转移,避免了能量损耗与竞争反应,催化效率显著提升。
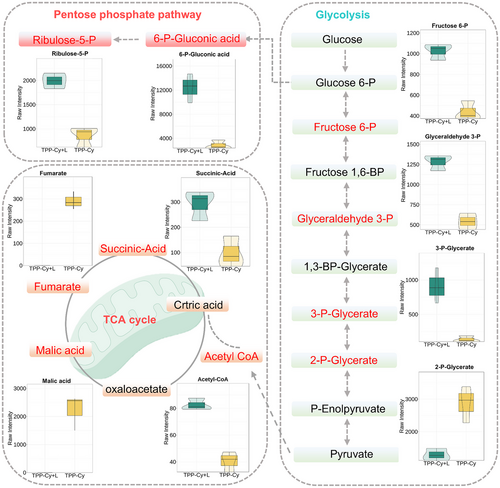
进一步的代谢组学与能量分析显示,TPP-Cy不仅阻断了线粒体氧化磷酸化,还导致三羧酸循环(TCA)中间产物异常积累,糖酵解与磷酸戊糖途径补偿失效,最终诱导癌细胞全面代谢崩溃。更重要的是,TPP-Cy触发的细胞死亡并非传统的凋亡,而是免疫原性焦亡。实验观察到细胞膜膨胀、乳酸脱氢酶释放、Caspase-3/GSDME通路激活,以及ATP、CRT、HMGB1等损伤相关分子释放,证实其能有效激活抗肿瘤免疫反应。
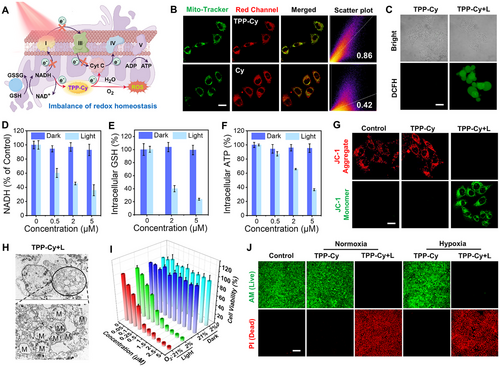
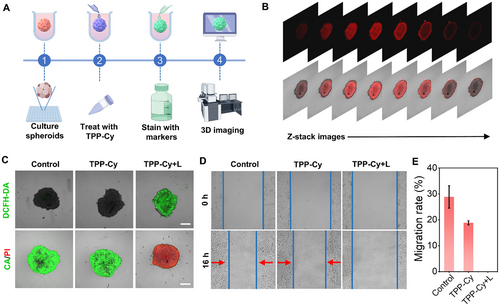
在三维肿瘤球模型与细胞迁移实验中,TPP-Cy展现出良好的穿透性与显著的抗迁移作用,进一步验证了其在复杂肿瘤微环境中的治疗潜力。
总结及展望
本研究首次提出单激子驱动的光氧化还原催化机制,成功开发出具备“氧自适应”功能的线粒体靶向光敏剂TPP-Cy。其独特的双通路机制既能在有氧条件下产生活性氧杀伤肿瘤,又能在缺氧环境中直接催化线粒体关键分子,诱导能量危机与免疫原性焦亡,从而突破了传统PDT的氧依赖限制。该成果不仅为缺氧肿瘤治疗提供了新思路,也为光催化在生物治疗领域的应用奠定了理论框架。未来,TPP-Cy有望成为兼具肿瘤清除与免疫激活的双重策略药物,推动光动力治疗在临床中的广泛应用。