【Adv.Mater.】靶向脂滴的仿生脂质体显著提升白血病化疗-铁死亡联合疗法效果
文章标题:Lipid Droplet‐Targeted Biomimetic Liposomes Potentiate Chemo‐Ferroptosis Therapy in Leukemia
通讯作者:Xiao Dong
文章链接:https://doi.org/10.1002/adma.202515716
文章概要
引言
白血病是一类起源于骨髓和造血系统的恶性肿瘤,常伴随造血功能衰竭、器官浸润及预后不良。尽管免疫治疗如CAR-T已取得进展,但诱导化疗仍是急性髓系白血病(AML)和急性淋巴细胞白血病(ALL)的首选方案。然而,约三分之二的患者在首次完全缓解后两年内复发,五年生存率不足30%。复发的关键原因在于骨髓内残留的耐药白血病细胞(LCs)和白血病干细胞(LSCs)。铁死亡作为一种依赖铁离子的程序性细胞死亡方式,因其对耐药细胞的敏感性而成为潜在的新型治疗策略。然而,研究发现化疗药物阿糖胞苷(Ara-C)会诱导骨髓白血病细胞脂滴(LDs)积累,从而降低其对铁死亡的敏感性。
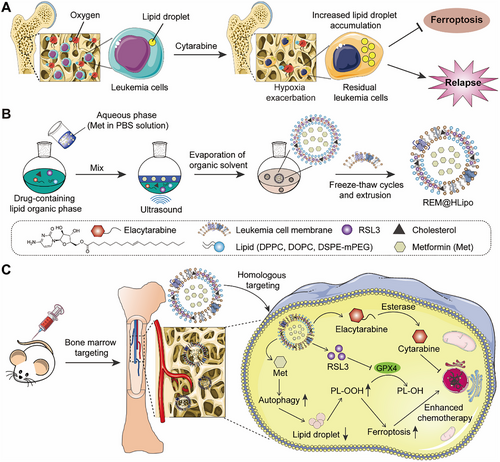
主要实验及结论
研究团队设计了一种仿生脂质体(REM@HLipo),其融合了白血病细胞膜并共同包载三种药物:铁死亡诱导剂RSL3、阿糖胞苷前药elacytarabine以及脂滴破坏剂二甲双胍(Met)。该系统利用同源膜靶向特性精准递送至骨髓白血病细胞。实验结果显示:
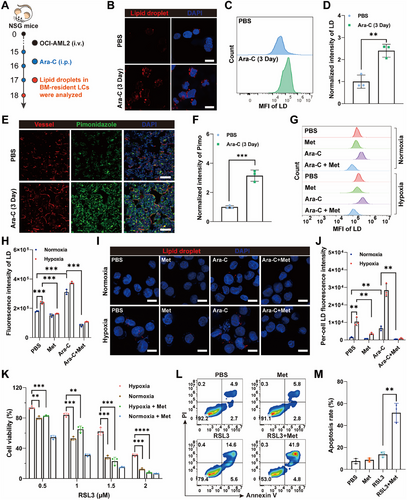
- Ara-C治疗显著增加骨髓白血病细胞脂滴积累,导致铁死亡抵抗;而Met可通过激活AMPK途径诱导自噬,减少脂滴并释放多不饱和脂肪酸(PUFAs),增强其氧化敏感性。
- REM@HLipo在AML和ALL小鼠模型中表现出强效的抗白血病作用,显著降低骨髓白血病细胞及白血病干细胞比例,并有效抑制脾肿大。
- 机制研究表明,REM@HLipo通过脂滴破坏增强PUFA氧化,协同RSL3诱导铁死亡,同时与Ara-C化疗形成强效协同作用。
- 安全性评估显示,该纳米平台在小鼠体内未引起明显肝肾毒性,具有良好生物相容性。
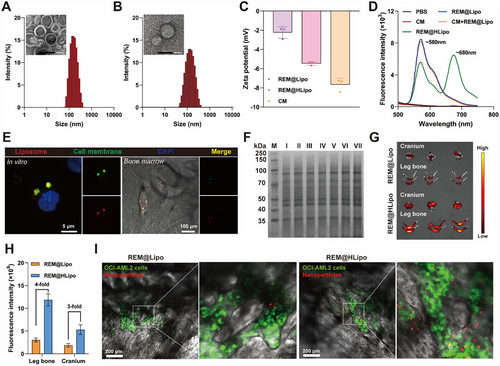
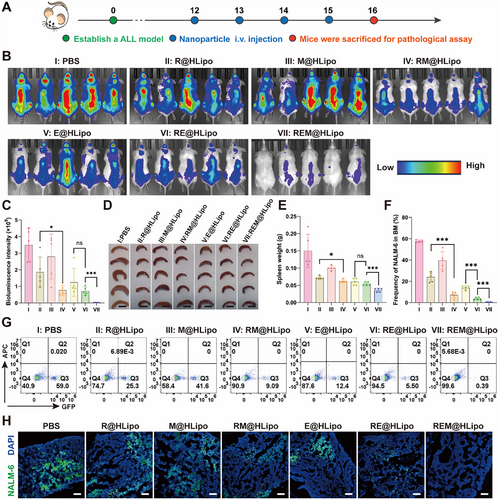
总结及展望
本研究揭示了化疗诱导的脂滴积累是白血病细胞铁死亡耐受的重要机制,并提出通过二甲双胍破坏脂滴、联合化疗与铁死亡诱导剂的仿生脂质体策略,有效消除骨髓耐药白血病细胞及干细胞。该成果不仅为白血病复发的防治提供了新思路,也提示未来可进一步探索治疗诱导的代谢重编程,如氨基酸和核苷酸代谢改变,作为新的治疗靶点。此类仿生纳米药物平台有望成为复发或难治性白血病的重要治疗选择。