【Adv.Mater.】 200倍药物富集!声学节点时空调控助力膀胱癌精准治疗
文章标题: In Vivo Target Drug Enrichment Based on Spatiotemporal Acoustic Node Modulation (STANM) for Bladder Cancer Treatment
通讯作者: Yuanyi Zheng
文章链接: https://doi.org/10.1002/adma.202517740
文章概要
引言
化疗是膀胱癌常见的治疗方式,但药物在肿瘤部位的有效浓度往往不足,仅有约1%的剂量能到达肿瘤组织。 这不仅限制了疗效,还会因药物在体内循环导致心脏、肾脏、肝脏等器官损伤。为解决这一难题,研究团队提出了一种基于时空声学节点调控(STANM) 的新方法,通过动态声场驱动药物载体微粒在体内富集至肿瘤位置,从而实现高效、精准的药物递送。
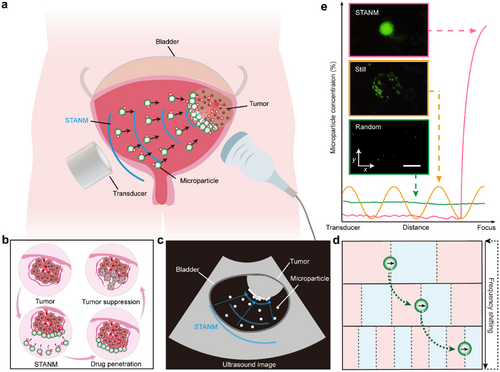
主要实验及结论
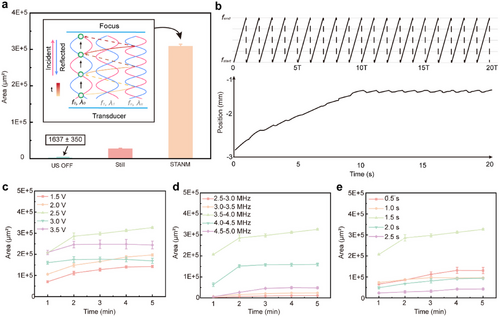
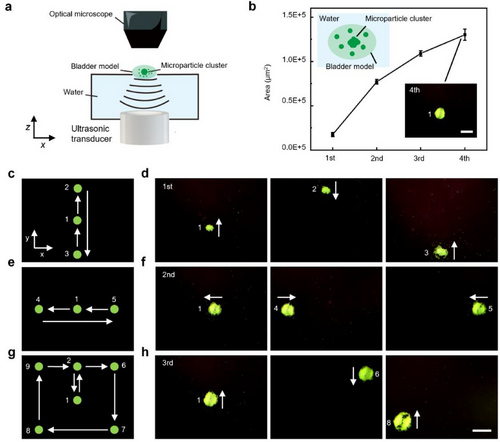
研究首先在体外膀胱模型中验证了 STANM 的富集性能。与无声场对照组相比,STANM 能够实现约200倍的微粒浓度提升,相较于传统静态声场也提高了约10倍。通过调节声场的电压、频率范围和频率切换周期,团队优化了富集效果,最佳条件下微粒在数分钟内即可快速聚集于目标区域。进一步实验显示,STANM 不仅能富集药物载体,还能操控其在二维平面内的移动,实现对药物微粒簇的精准操控。
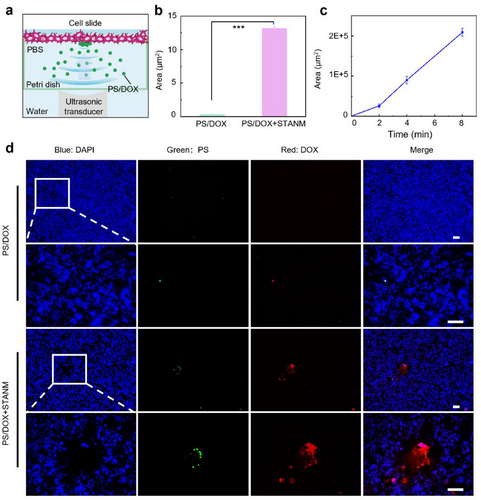
在体外细胞实验中,STANM 显著提高了化疗药物阿霉素(DOX)在膀胱癌细胞上的富集效率,药物分布面积提升约40倍。随后在小鼠膀胱癌模型中,研究团队将 DOX 负载于聚苯乙烯微粒(PS/DOX),并结合 STANM 进行治疗。结果显示,PS/DOX+STANM 组的肿瘤重量较传统化疗降低了72.43%,较对照组下降超过80%,肿瘤体积仅为对照组的22%。组织学分析进一步证实肿瘤组织出现明显坏死与出血,显示出强效的抗肿瘤作用。
此外,研究还对 STANM 的生物安全性进行了评估。实验结果表明,在治疗过程中小鼠的主要器官未出现明显病理损伤,血液学和生化指标与正常组无显著差异,说明该系统具有良好的生物相容性。
总结及展望
本文提出并验证了一种无需生物标记的声学驱动药物富集系统 STANM,通过动态调控声学节点实现药物载体在体内的精准聚集,显著提升了膀胱癌化疗的疗效。该方法不仅在小鼠模型中展现出强效的抗肿瘤作用,还具备良好的安全性。未来,研究团队计划进一步优化声场参数,结合声学全息透镜实现多点药物操控,并探索在大型动物模型及临床试验中的应用前景。这一突破为膀胱癌及其他实体瘤的精准治疗提供了全新的技术路径。