【Angew.Chem.】 超声触发分子活化:在小鼠体内实现精准药物释放的新突破
文章标题:Remote Molecule Activation in Living Mice Triggered by Therapeutic Ultrasound
通讯作者:Xinyuan Fan
文章链接:https://doi.org/10.1002/anie.202525894
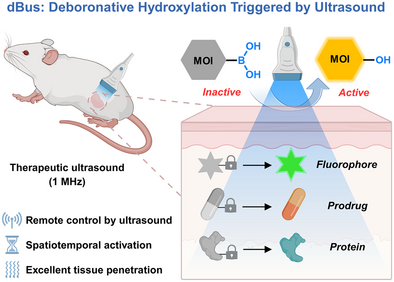
文章概要
引言
在生物医学研究与临床治疗中,如何在活体内实现分子的远程、非侵入式精准调控一直是重大挑战。传统的光学方法虽然具备时空可控性,但受限于组织穿透力和光毒性;X射线虽能深入组织,但存在辐射风险。相比之下,超声波因其深层穿透力、低损伤和操作简便性,成为理想的外源刺激手段。本文提出了一种全新的化学策略——超声触发的去硼羟基化反应(dBus),通过临床相关的治疗超声在体内生成羟基自由基,从而实现对硼酸保护分子的精准激活。
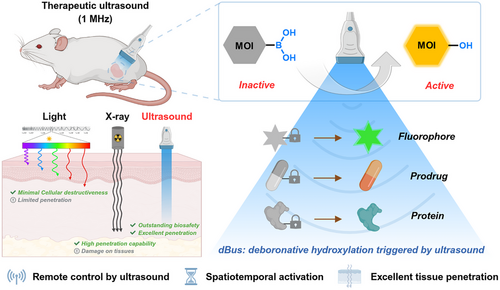
主要实验及结论
研究首先验证了超声在水溶液中可驱动硼酸基团转化为羟基,恢复荧光分子的活性。机理研究表明,羟基自由基是该反应的核心驱动力。随后,作者将该策略应用于多类功能分子:
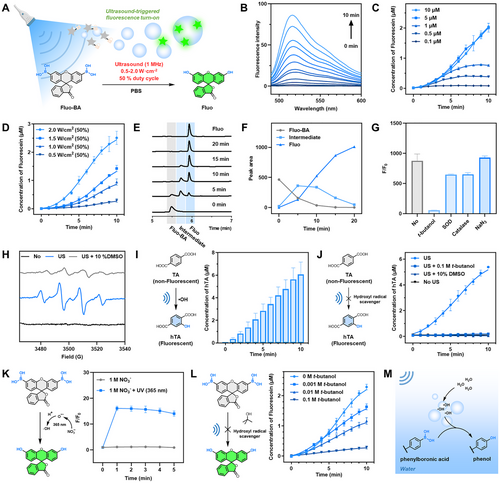
- 小分子药物:如多柔比星(Dox)和喜树碱衍生物(SN38),在硼酸保护下失活,经超声激活后恢复药效,实现远程控释。
- 功能探针:如生物素标记探针,在超声作用下生成活性中间体,可与蛋白质共价结合,实现复杂环境下的分子标记。
- 大分子体系:包括肽类和蛋白质,实验显示超声可在温和条件下释放活性肽段或恢复蛋白功能,且不破坏整体结构。
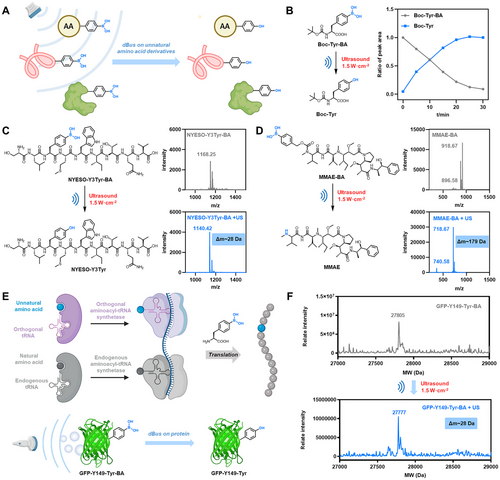
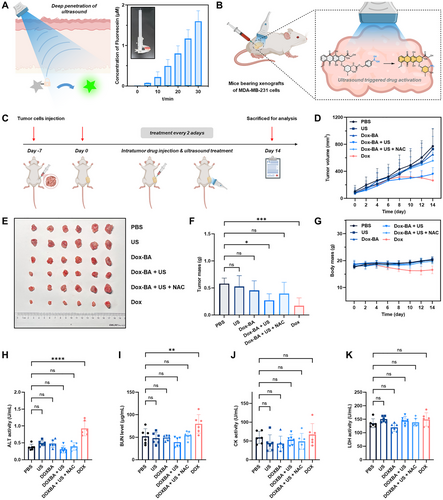
在动物实验中,研究团队将硼酸保护的多柔比星前药注射至肿瘤小鼠体内,并施加治疗超声。结果显示,药物在肿瘤局部被激活,显著抑制肿瘤生长,同时避免了系统性毒性。与直接给药相比,超声激活的前药组小鼠体重稳定,肝肾功能指标正常,体现出更高的安全性与精准性。
总结及展望
本文提出的dBus策略不仅在化学层面建立了超声触发的通用反应平台,更在生物医学应用中展示了远程、非侵入式的药物精准释放。其优势在于:
- 深层组织穿透与高生物相容性
- 操作简便、成本低廉,兼容现有超声设备
- 可广泛应用于小分子药物、探针及大分子体系
未来,该方法有望扩展至系统性给药结合局部超声激活,实现更精准的化疗与免疫治疗。同时,局部释放免疫调节剂或激活免疫相关前药,可能为肿瘤微环境中的免疫治疗提供新思路。dBus不仅是化学反应的突破,更是精准医学与声药学发展的重要里程碑。