【JACS】新型琥珀酸纳米材料,增加渗透压,触发焦亡途径,上调组织相容性复合体,抑制肿瘤免疫逃逸
总结
研究开发了一种基于琥珀酸钠纳米颗粒(C₄H₄Na₂O₄ NPs)的新型肿瘤免疫治疗方法,通过诱导细胞焦亡和上调MHC-I表达,显著增强了抗肿瘤免疫反应,抑制肿瘤生长和转移。
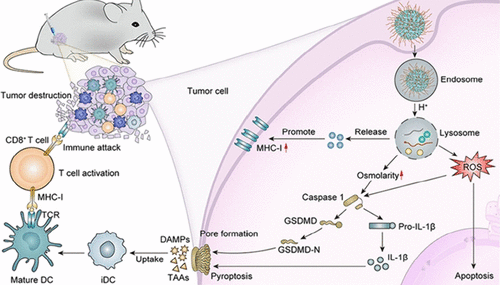
摘要
尽管免疫治疗在临床应用中前景广阔,但其效果常因低免疫反应和肿瘤免疫逃逸而受限。本研究介绍了一种简单且无药物的无机纳米材料——琥珀酸钠纳米颗粒(C₄H₄Na₂O₄ NPs),通过快速微乳液法制备。C₄H₄Na₂O₄ NPs进入肿瘤细胞后,释放高浓度的Na⁺和琥珀酸根离子,导致细胞内渗透压增加,触发焦亡途径,释放细胞内容物、炎症因子和损伤相关分子模式(DAMPs),从而增强免疫反应。此外,C₄H₄Na₂O₄ NPs通过上调主要组织相容性复合体-I(MHC-I)表达,抑制肿瘤免疫逃逸。综合作用下,C₄H₄Na₂O₄ NPs通过焦亡诱导的免疫激活和MHC-I表达上调,显著抑制肿瘤生长和转移,为肿瘤免疫治疗提供了新的策略。
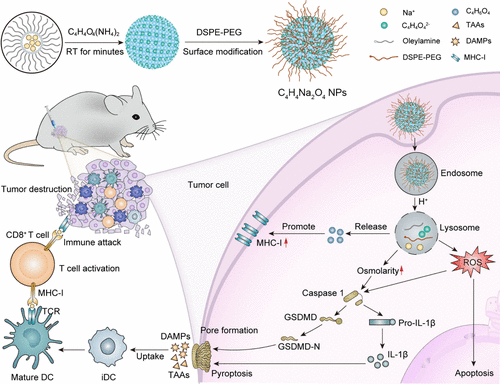
研究结果分类展示
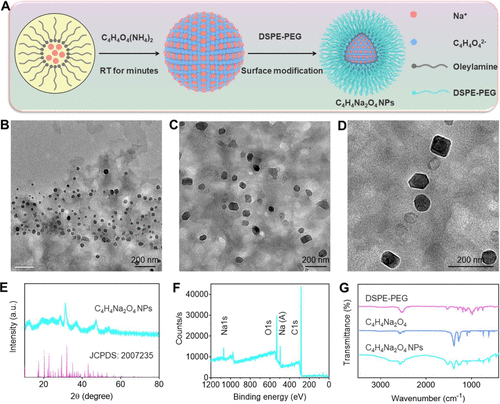
纳米颗粒的制备与表征
- 合成方法:通过快速微乳液法在室温下制备C₄H₄Na₂O₄ NPs,使用琥珀酸铵和油酸钠作为主要原料。
- 表征方法:利用透射电子显微镜(TEM)、X射线衍射(XRD)和X射线光电子能谱(XPS)对纳米颗粒进行表征,确认其结构和成分。
焦亡诱导与细胞毒性
- 细胞摄取:C₄H₄Na₂O₄ NPs在4T1细胞中表现出显著的摄取能力,释放Na⁺和琥珀酸根离子。
- 焦亡诱导:C₄H₄Na₂O₄ NPs通过离子超载触发氧化应激、线粒体破坏和caspase-1/GSDMD介导的焦亡,释放大量细胞内容物和炎症因子。
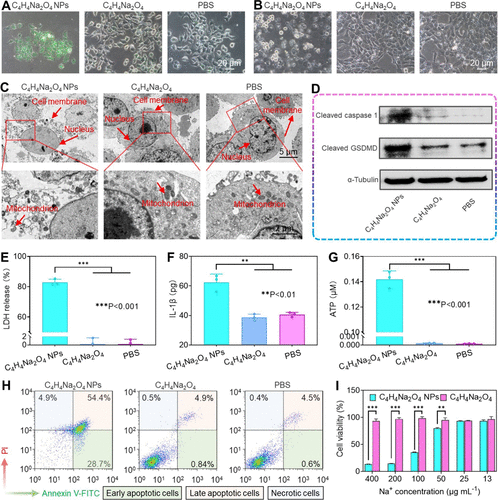
- 细胞毒性:C₄H₄Na₂O₄ NPs在体外实验中表现出浓度依赖的细胞毒性,显著抑制4T1细胞增殖。
MHC-I表达上调
- MHC-I表达:C₄H₄Na₂O₄ NPs通过琥珀酸根离子积累,上调4T1细胞表面的MHC-I表达,促进抗原呈递和CD8⁺ T细胞识别。
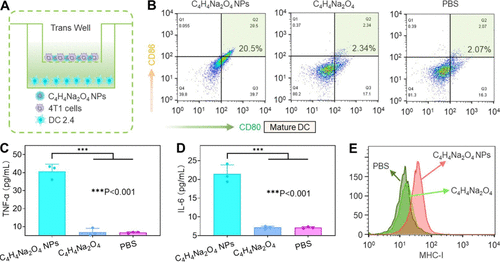
体内免疫激活与抗肿瘤效果
免疫激活:C₄H₄Na₂O₄ NPs在小鼠肿瘤模型中显著激活树突状细胞(DCs)和CD8⁺ T细胞,增强抗肿瘤免疫反应。
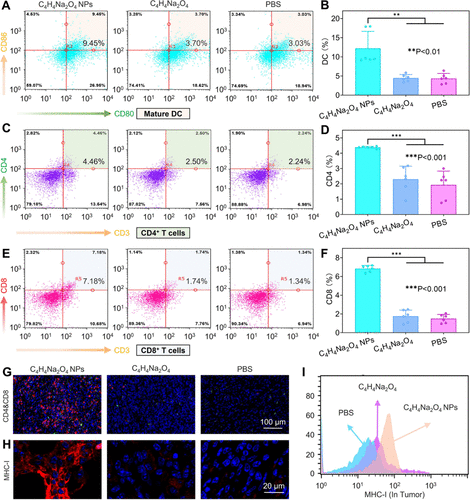
抗肿瘤效果:C₄H₄Na₂O₄ NPs在4T1乳腺肿瘤小鼠模型中显著抑制肿瘤生长和转移,表现出优异的治疗效果和生物安全性。
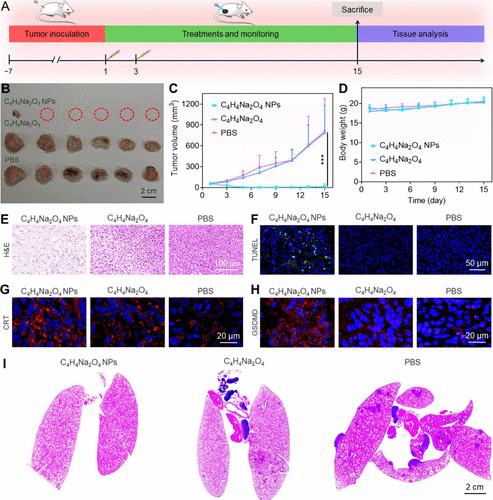
这项研究展示了琥珀酸钠纳米颗粒在增强肿瘤免疫治疗中的巨大潜力,为未来的肿瘤治疗提供了新的思路和方法。详细信息可以在这里找到。
参考文献
Zheng, P.; Wang, G.; Liu, B.; Ding, H.; Ding, B.; Lin, J. Succinate Nanomaterials Boost Tumor Immunotherapy via Activating Cell Pyroptosis and Enhancing MHC-I Expression. J. Am. Chem. Soc. 2025, jacs.4c09566. https://doi.org/10.1021/jacs.4c09566.