【Adv.Mater.】信噪比高达45.25,TADF特性的三重态荧光引导的PDT显著抑制肿瘤
简介
本研究提出了一种创新性的光动力治疗(PDT)策略,利用骨架同源纳米颗粒实现三重态荧光引导的PDT。该体系由具有热激活延迟荧光(TADF)特性的亲脂性核心和暴露于氧气的光敏剂壳层构成,有助于提高时间分辨成像(TRI)精度,并同步增强PDT效果。研究结果表明,该方法在深度肿瘤治疗中表现出较高的信噪比和优异的光动力效应。
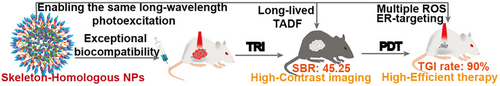
摘要
光动力治疗(PDT)在抗肿瘤治疗中具有重要价值,但由于生物组织本身的自发荧光和PDT产物的干扰,传统的荧光成像难以提供精确的治疗指导。为解决这一难题,本研究设计了一种骨架同源纳米颗粒,以TADF核心提供长寿命荧光信号,引导PDT过程。该纳米颗粒通过合理的分子设计和自组装策略,确保相同波长的光激发用于TRI和PDT,同时减少相分离,提高光敏剂的稳定性。实验结果表明,该纳米颗粒在肾癌模型中实现了高信噪比(45.25)和显著的肿瘤抑制效果,验证了该策略在生物医学治疗中的潜力。
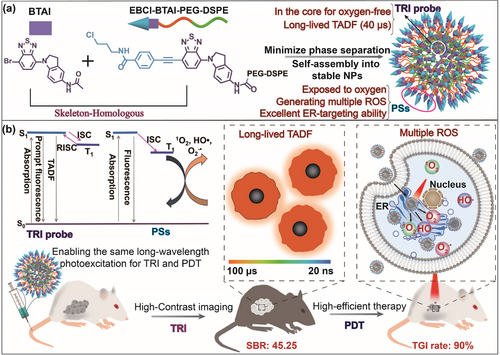
研究结果与讨论
分子设计与光物理特性
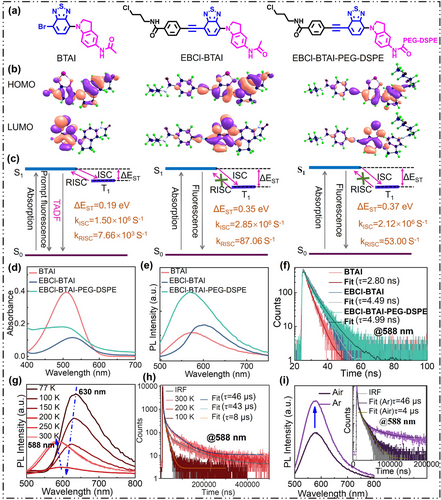
研究团队基于供体-受体(D-A)骨架,优化了π-共轭桥结构,以调控最高占据分子轨道(HOMO)与最低未占据分子轨道(LUMO)的分布,影响自旋轨道耦合和单重-三重态能级间隙(ΔE ST)。实验测定了关键分子BTAI、EBCl-BTAI及EBCl-BTAI-PEG-DSPE的荧光特性,证实BTAI具有明显的TADF现象,而后两者则主要表现出光敏剂的特性。
TADF与活性氧(ROS)生成
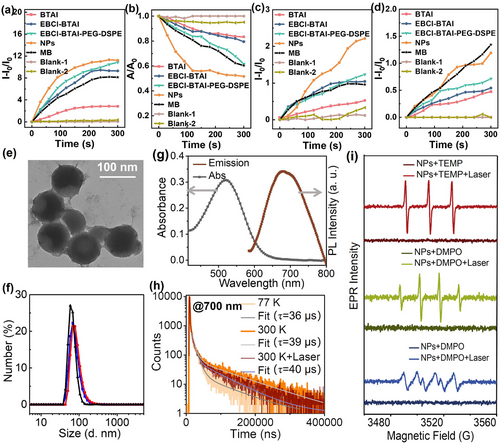
基于光敏剂的电子跃迁特性,研究进一步探讨了纳米颗粒的ROS生成能力。实验采用不同ROS指示剂检测发现,EBCl-BTAI及其衍生物能够高效地产生单线态氧(¹O₂)、超氧自由基(O₂⁻•)及羟自由基(HO•),而BTAI因其快速的反向系间窜跃(RISC)过程,其ROS产量较低。
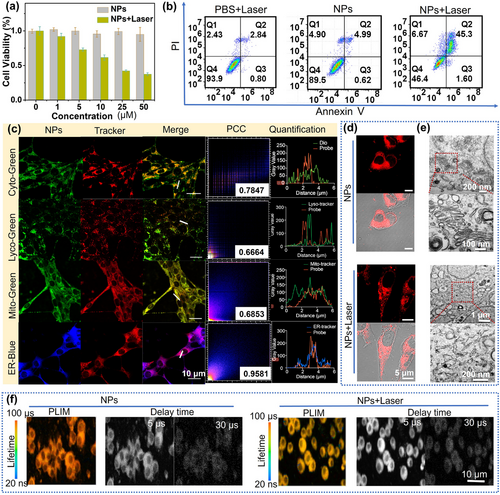
在细胞水平的TRI与PDT
纳米颗粒在体外4T1癌细胞中的表现经过详细评估。细胞摄取实验显示该纳米颗粒优先靶向内质网(ER),并在局部生成ROS以诱导细胞凋亡。荧光寿命成像(PLIM)显示该纳米颗粒在整个PDT过程中持续保持长寿命荧光信号,验证了其在时间分辨成像中的应用价值。
体内长寿命TRI引导PDT
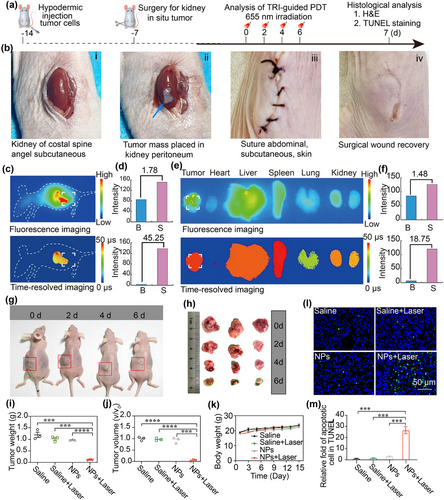
在小鼠肾癌模型中,纳米颗粒经静脉注射后迅速富集于肿瘤部位,并且长寿命TRI能够消除生物组织的背景干扰,实现精准的肿瘤定位。相比传统荧光成像,TRI的信噪比提高至45.25,明显提升了治疗可视化效果。在PDT过程中,该纳米颗粒表现出显著的肿瘤抑制率(高达90%),并在组织染色实验中确认了肿瘤细胞的广泛凋亡。安全性评估表明,该纳米颗粒对其他器官无毒性影响。
结论
本研究通过分子优化及纳米自组装策略,成功实现了TADF引导的PDT,解决了传统光动力治疗过程中成像干扰的问题。在细胞及动物模型中验证了该纳米颗粒的高效能和精准度,未来有望应用于深度肿瘤的诊断与治疗,为光动力治疗的发展提供新思路。