【Adv.Mater.】超声驱动的治疗平台,增强衰老骨髓间充质干细胞的修复,缓解慢性炎症
简介
全球人口老龄化日益加剧,骨组织修复能力随着年龄增长而下降。骨髓间充质干细胞(BMSCs)的衰老影响骨再生,而针对衰老MSC功能恢复的精准治疗策略仍然有限。本研究基于物理热刺激原理,开发了一种超声驱动的可植入信号转换治疗平台,以稳定的热信号作用于骨损伤部位,改善BMSCs线粒体功能,促进骨修复。
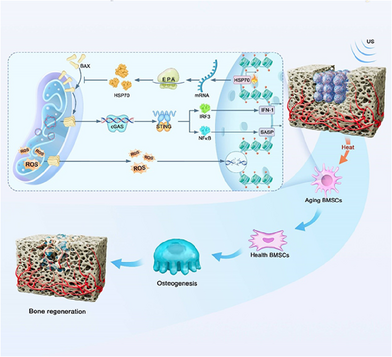
摘要
衰老微环境中的慢性炎症和再生能力缺失阻碍骨组织修复。研究发现,物理热刺激能有效延缓BMSCs衰老过程,并设计了一种超声驱动的信号转换治疗平台,利用聚多巴胺包覆金纳米棒(PDA@GNRs)作为核心组件,嵌入甲基丙烯酸凝胶微球(GMPG),实现局部热信号传导。在体外实验中,该平台可双向调节线粒体活性,减少氧化应激和mtDNA泄漏,抑制cGAS-STING通路激活,缓解慢性炎症。在大鼠股骨缺损模型中,该治疗平台显著提高骨密度,为老年骨组织修复提供了一种新策略。
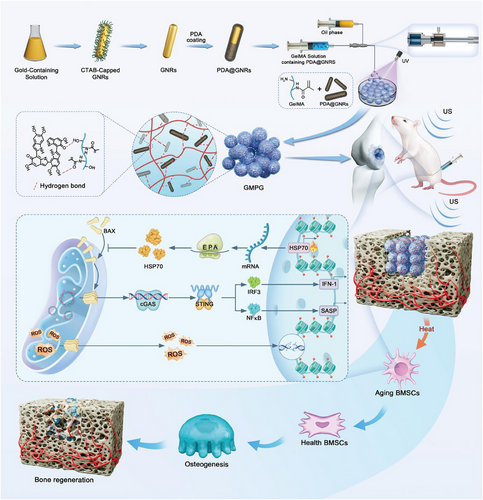
研究结果与讨论
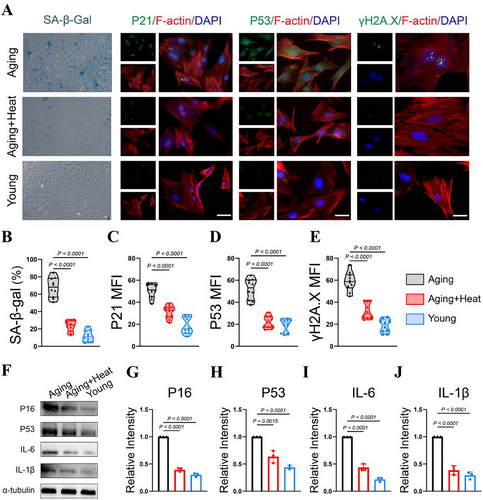
热刺激对BMSCs衰老逆转的评估
研究使用β-半乳糖苷酶染色和免疫荧光标记p21、p53基因,发现热刺激组细胞衰老标志显著减少。此外,γH2A.X荧光信号减弱,表明DNA损伤得到改善。WB分析进一步证实关键衰老表型的缓解。
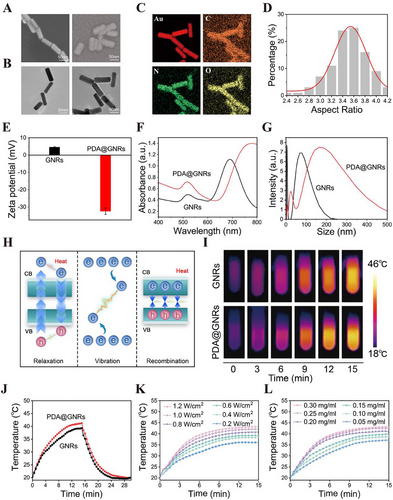
PDA@GNRs的制备及表征
TEM与SEM显示GNRs尺寸均匀,PDA涂层均匀包覆,EDS光谱证实PDA@GNRs的元素组成。DLS分析表明PDA@GNRs稳定性增强,紫外吸收峰红移,进一步证实PDA涂层成功。
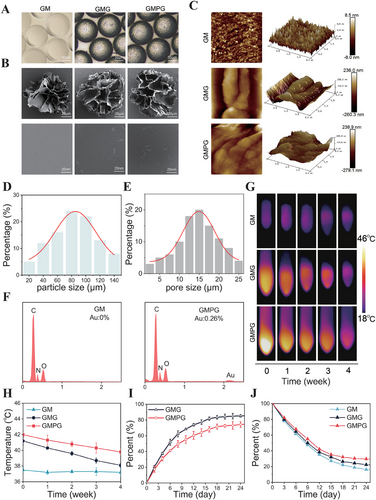
GMPG的合成及性能评估
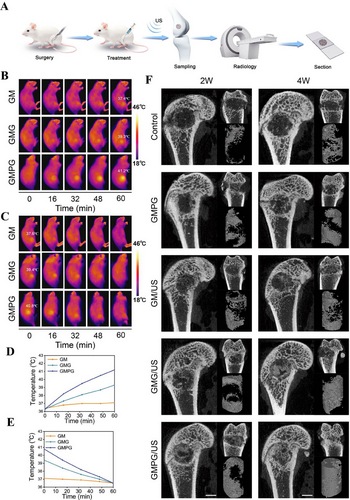
GMPG显现出较高的表面粗糙度,提高了热信号传导能力。体外释放实验表明PDA@GNRs在GMPG中的释放较慢,维持长期热疗效果。降解实验确认其稳定性,可长期支持骨组织修复。
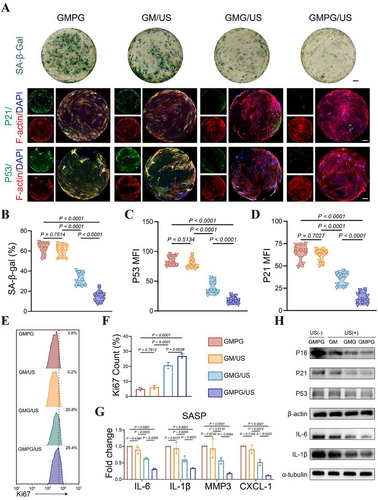
GMPG/US对BMSCs衰老表型的改善
SA-β-gal染色结果显示GMPG/US组衰老细胞数量明显减少,Ki67流式细胞检测表明细胞增殖能力增强。qRT-PCR及WB分析发现该平台显著抑制衰老相关分泌表型(SASP)因子的表达。
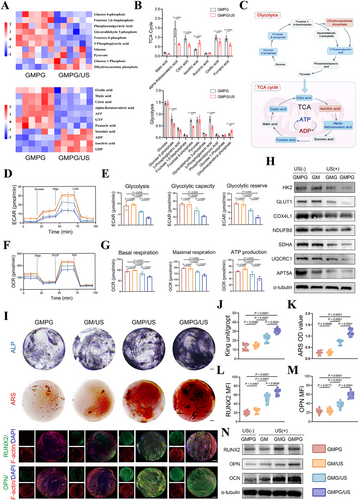
GMPG/US对衰老细胞代谢及成骨功能的影响
LC-MS代谢组学分析揭示GMPG/US降低糖酵解及TCA循环关键代谢物水平,减少细胞氧化应激。细胞呼吸检测表明GMPG/US降低基础呼吸和ATP合成能力。此外,免疫荧光及WB分析确认GMPG/US促进RUNX2、OPN表达,提高BMSCs的成骨分化潜力。
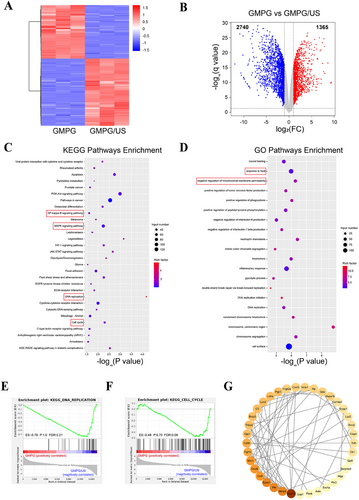
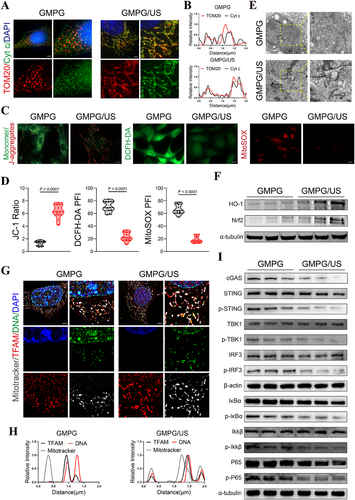
GMPG/US改善线粒体功能及内容物泄漏
HIS-SIM显示GMPG/US组线粒体膜通透性减少,JC-1探针标记表明线粒体膜电位恢复。DCFH-DA和MitoSOX荧光检测显示氧化应激降低。免疫金标记TEM及凝胶电泳验证GMPG/US减少mtDNA泄漏,抑制cGAS-STING通路活化。
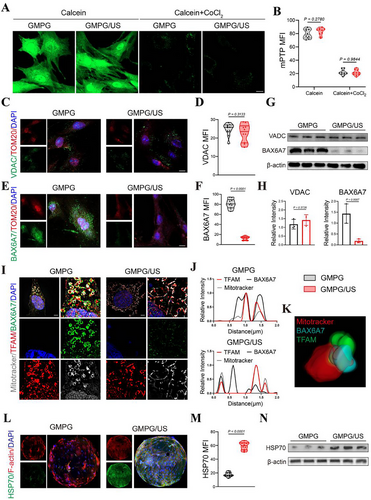
GMPG/US对BAX介导的线粒体膜通透性的调控
BAX免疫荧光染色和WB分析表明GMPG/US减少BAX表达,稳定线粒体膜通透性,有助于衰老BMSCs功能恢复。
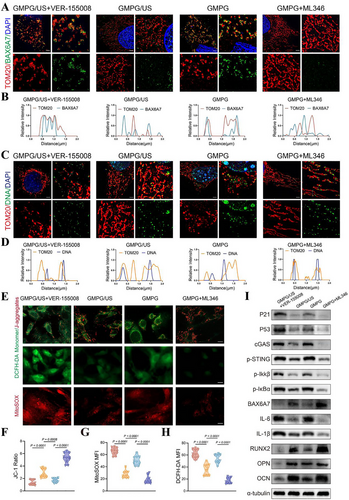
结论
本研究开发了一种基于信号转换的治疗平台,通过超声驱动的稳定热信号调节衰老BMSCs线粒体功能,恢复其成骨能力。该平台在体外及大鼠骨缺损模型中均表现出显著的骨修复效果,为老龄骨病治疗提供了新思路。未来研究可进一步优化材料构成,提升临床转化潜力。