【Adv.Mater.】突破性研究:干细胞衍生“触须”载体实现阿尔茨海默病的非侵入性光遗传治疗
在治疗神经退行性疾病的探索中,神经激活光遗传技术因其能够“重启”退化神经元而备受关注。然而,该技术仍面临持久侵入性及病理环境修复不足的挑战,限制了其临床应用。最近,一项发表在《Advanced Materials》期刊上的研究提出了一种创新策略——利用诱导多能干细胞(iPSCs)分化生成“触须”干细胞(TenSCs),并进一步制备其衍生的囊泡(TenSCev)作为光遗传学元素的功能载体。这种载体不仅能精准靶向神经元,还具备病理环境修复能力,实现了无创、可控的神经激活,并有效改善阿尔茨海默病(AD)及衰老小鼠的认知功能。
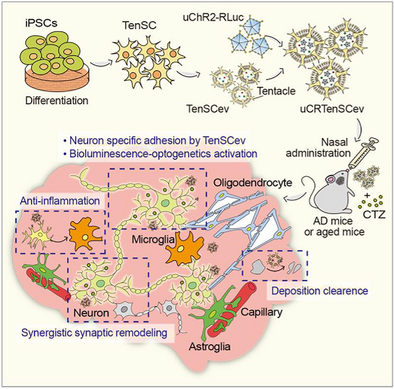
1. 阿尔茨海默病治疗的困境及光遗传学技术的潜力
阿尔茨海默病是一种高发病率且呈现渐进性恶化的神经退行性疾病,目前仍缺乏有效手段能够完全延缓或阻止其病程发展。光遗传技术通过精准雕刻神经元,利用光敏通道蛋白(如ChannelRhodopsin,ChR2)激活神经元,从而促进神经递质释放、突触重塑及神经响应,这为阿尔茨海默病的治疗提供了可能性。然而,其侵入性操作(如病毒注射及光纤植入)及对病理环境改善能力的不足,严重限制了该技术的进一步发展。因此,研究人员尝试开发新的功能载体,以解决这些问题。
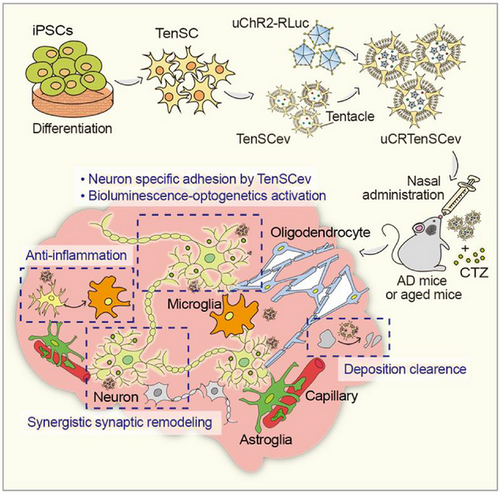
2. “触须”干细胞与衍生囊泡:光遗传载体的革新
研究团队提出了一种新的细胞分化策略,通过特殊的诱导程序,使iPSCs分化为具有神经靶向能力并能够修复病理环境的“触须”干细胞(TenSCs),并从其细胞膜制备TenSCs衍生囊泡(TenSCev),用于运载光遗传学病毒,使治疗实现非侵入式神经调控。
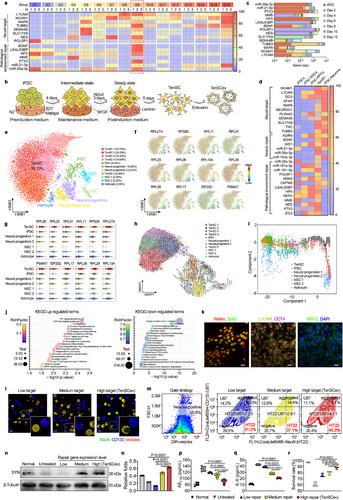
实验表明,这些“触须”细胞及其衍生囊泡在表达神经靶向相关基因及病理修复相关基因方面均具有显著优势。研究人员利用单细胞转录组测序(scRNA-seq)对TenSCs进行详细解析,并确认其处于特殊的分化状态,具备独特的功能基因表达谱。此外,TenSCev的生物学特性验证显示,它能选择性地靶向神经元,并改善病理环境,如神经营养支持、清除病理沉积(如β-淀粉样蛋白),以及抑制炎症反应,从而实现光遗传技术的优化应用。
3. “触须”囊泡协助光遗传学实现非侵入式神经激活
为了避免传统光遗传技术的侵入性操作,该研究将光遗传学病毒去壳处理,使之更易进入细胞核,提高转染效率,并将其加载到TenSCev中,以形成uCRTenSCev。体外实验显示,uCRTenSCev能有效将光遗传学组件递送至目标细胞,并在CTZ(底物)作用下,触发光敏离子通道ChR2,促使钙离子大量内流,从而激活神经元。实验进一步表明,这种非创伤性的激活策略不仅能精准靶向病灶区域,还能控制神经元激活的时间及剂量,提升治疗的安全性和可控性。
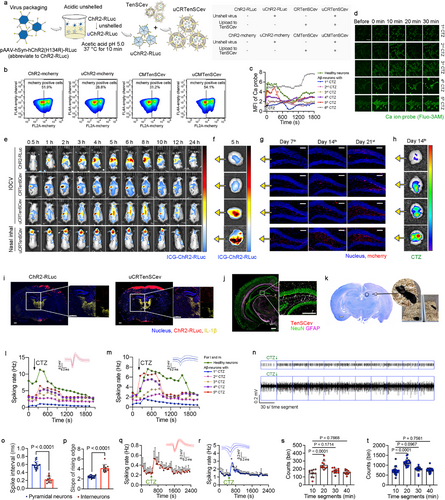
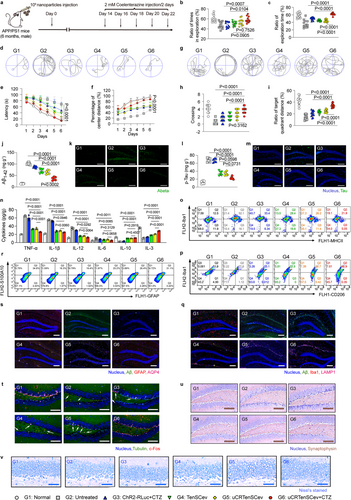
在体内实验中,研究人员通过APP/PS1阿尔茨海默病模型小鼠,验证了uCRTenSCev的治疗效果。结果显示,采用鼻胃给药方式后,uCRTenSCev能优先靶向大脑炎症区域,选择性附着于神经元,并有效激活位于病变区域的神经元。同时,实验记录了小鼠脑区神经元的电生理信号,证实该治疗方案能在20分钟内快速激活神经元,并在重复刺激过程中逐渐改善神经元响应能力,展现了优异的治疗潜力。
4. 协同治疗:光遗传学与病理环境修复的双重作用
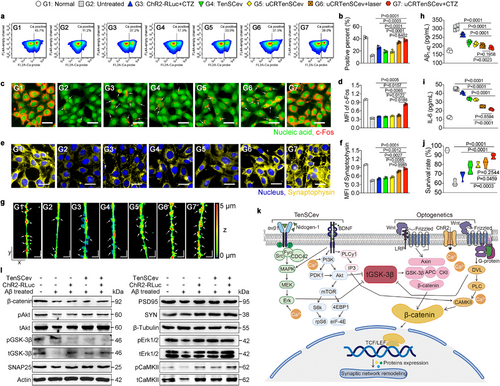
研究进一步探讨了TenSCev对光遗传治疗的增强效果。结果表明,光遗传学通过经典WNT及WNT/Ca2+信号通路激活神经元,而TenSCev中的生长因子(如BDNF、Nidogen-1等)则通过AKT及MAPK信号通路放大这一激活作用。此外,TenSCev还能促进β-淀粉样蛋白的降解,抑制炎症因子,从而创造有利于神经网络重塑的环境。这种协同治疗策略显著提高了神经元存活率,并成功避免了传统光遗传技术可能引发的不适当神经活动。
5. 治疗效果验证:改善阿尔茨海默病小鼠认知功能
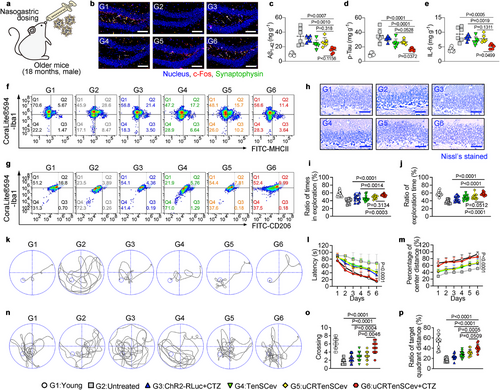
为了进一步验证该策略对阿尔茨海默病的治疗效果,研究人员进行了行为学测试,包括新物体识别实验(NOR)及莫里斯水迷宫实验。结果表明,接受uCRTenSCev治疗的小鼠在认知和记忆能力方面表现明显改善。它们对新物体的探索欲望增加,在水迷宫实验中学习速度加快,找到目标平台的能力显著增强。此外,实验数据表明,uCRTenSCev能够有效修复突触连接,提高神经元的传递效率,从而改善小鼠的认知表现。
6. 结论与临床应用展望
该研究通过利用干细胞分化生成功能性生物材料,开发了一种非侵入式光遗传治疗策略,不仅实现了可控神经激活,还成功改善了病理环境,为阿尔茨海默病及其他神经退行性疾病的治疗提供了新的希望。这种创新的细胞分化及光遗传学结合策略,未来可能在其他神经系统疾病的研究与临床应用中发挥重要作用。此外,研究中提出的“特异性生物材料的生成”概念,也可能在药物递送载体的开发上开启新的方向。
这项突破性的研究表明,利用干细胞生成的特殊载体可以有效提高光遗传技术的临床适用性,或将开启神经疾病治疗的新篇章。未来,随着研究的进一步深入,该策略可能成为神经调控与神经修复技术的重要发展方向。
参考文献
Zhai, Y.; Gao, F.; Shi, S.; Zhong, Q.; Zhang, J.; Fang, J.; He, F.; Zhang, Y.; Li, Y.; Liu, F.; Xue, B.; Gu, Y.; Li, S. Noninvasive Optogenetics Realized by iPSC‐Derived Tentacled Carrier in Alzheimer’s Disease Treatment. Advanced Materials 2025, 2419768. https://doi.org/10.1002/adma.202419768.