【JACS】同时激活细胞铁死亡、焦亡及膨胀死亡三种非凋亡性路径,对氧气无依赖,新型光催化剂增强抗肿瘤免疫反应
简介
该研究提出一种创新的氧气无依赖光催化剂(EBSe),旨在克服传统光动力疗法在治疗缺氧性实体瘤中的局限性。通过近红外光诱导,EBSe能够激活细胞铁死亡、焦亡及膨胀死亡三种非凋亡性路径,从而增强抗肿瘤免疫反应。
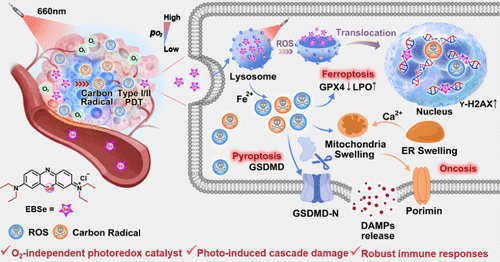
摘要
传统光动力疗法因对氧气的依赖性及缺氧导致的抗凋亡性和免疫抑制微环境,难以对实体瘤产生有效治疗效果。本文开发了一种基于二硒和乙基改造的新型光催化剂EBSe,兼具高光毒性和优异的光毒性指数,能够在缺氧和常氧条件下有效产生多种活性氧种类,并诱导光致溶酶体-细胞核转移和多重器官损伤,从而启动铁死亡、焦亡及膨胀死亡。实验在4T1肿瘤模型中验证了该路径协同机制对抗肿瘤免疫的促进作用,为光动力疗法临床转化提供了新思路。
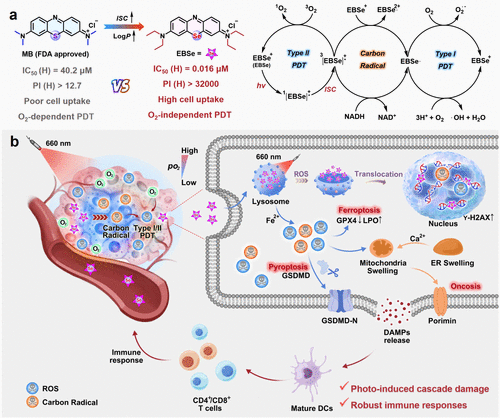
研究结果与讨论
光催化剂的设计与合成
研究者通过硒替代及乙基修饰,对FDA批准使用的光敏剂MB进行优化。EBSe表现出更高的细胞摄取效率、更强的氧化能力以及显著提升的光毒性。
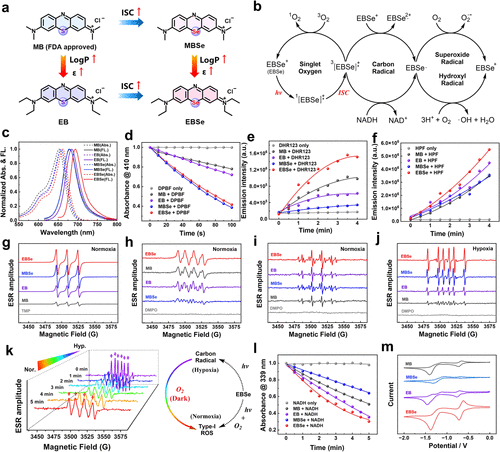
光催化性能与细胞毒性实验
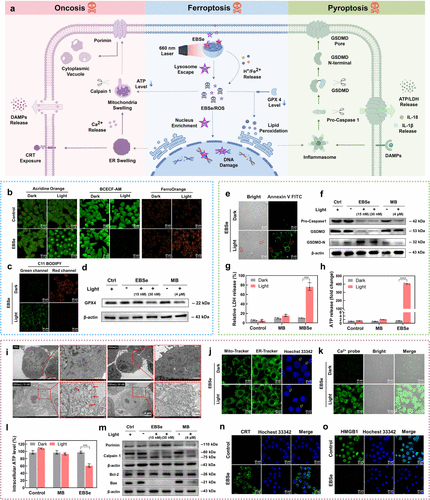
EBSe在缺氧条件下对4T1细胞的光毒性提升超过2500倍,同时展现了非凋亡性细胞死亡路径的诱导能力,包括铁死亡(GPX4水平下降及脂质过氧化累积)、焦亡(GSDMD相关蛋白激活及细胞膜泡状突起)以及膨胀死亡(线粒体和内质网异常肿胀)。
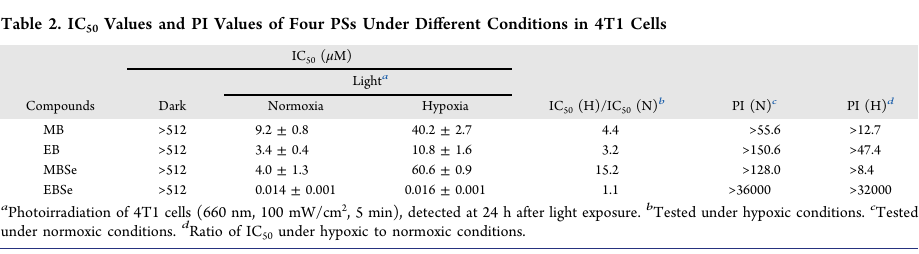
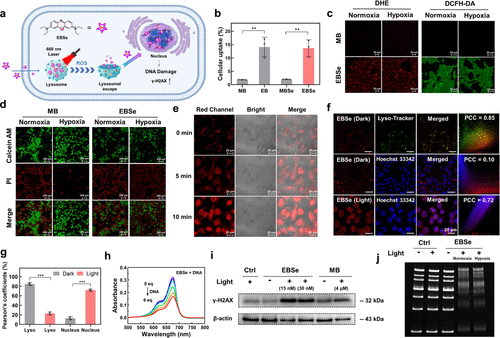
器官损伤与免疫激活
EBSe光照后从溶酶体转移至细胞核,导致DNA损伤显著增加,同时触发多种器官亚结构损伤。这些损伤协同作用最终激活抗肿瘤免疫反应,表现为细胞因子的释放、肿瘤细胞的溶解以及免疫系统的激活。
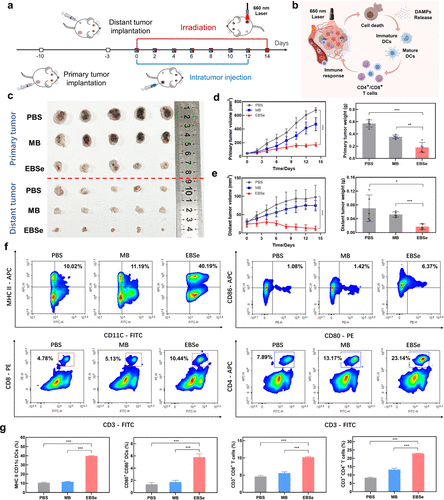
结论
EBSe是一种兼具氧气无依赖及非凋亡性细胞杀伤路径的新型光敏剂,在体内实验中显著增强了肿瘤免疫反应。该研究为克服缺氧性实体瘤治疗中的挑战提供了新思路,同时具备未来临床转化的潜力。
参考文献
Yao, S.; Xu, F.; Wang, Y.; Shang, J.; Li, S.; Xu, X.; Liu, Z.; He, W.; Guo, Z.; Chen, Y. Photoinduced Synergism of Ferroptosis/Pyroptosis/Oncosis by an O2 -Independent Photocatalyst for Enhanced Tumor Immunotherapy. J. Am. Chem. Soc. 2025, jacs.4c17268. https://doi.org/10.1021/jacs.4c17268.