【JACS】超亮余辉纳米系统:眼科治疗的新突破——基于环丁烷-二氧杂环丁烷的创新治疗策略
引言
全球范围内,年龄相关性黄斑变性(AMD)已成为导致老年人失明的主要因素之一。其中,湿性AMD约占严重视力损害病例的80%,其病理机制主要涉及脉络膜新生血管(CNV)的异常增生。传统治疗手段,如抗血管内皮生长因子(VEGF)药物虽能一定程度上抑制CNV,但治疗效果存在较大的个体差异,且长期VEGF抑制可能影响眼部细胞的生理稳态。因此,寻找更高效、安全的替代疗法成为眼科研究的重要方向。
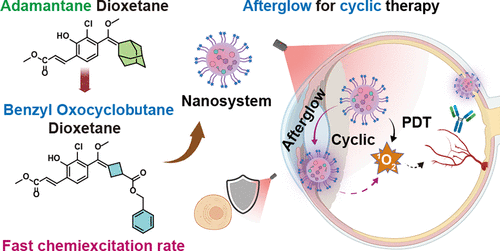
光动力疗法(PDT)是另一种针对CNV的治疗策略,其中FDA批准的光敏剂维替泊芬(Verteporfin,Ver)在690 nm激光照射下可产生单线态氧(¹O₂),从而损伤病理性血管。然而,由于维替泊芬的化学稳定性较低且具有高度疏水性,其治疗潜力受到限制。此外,长时间的激光照射可能导致周围眼组织损伤,导致患者疼痛和不适。针对这一问题,研究者提出了一种基于余辉效应的新型治疗策略,即在光照结束后,持续利用余辉光源激活光敏剂,使其进入激发态并产生¹O₂,从而减少外部激光照射,降低眼组织损害。
研究创新点
在传统的二氧杂环丁烷光化体系中,由于金刚烷-二氧杂环丁烷的空间位阻较大,化学激发效率受限,导致电子转移受阻,降低余辉效能。本研究创新性地在二氧杂环丁烷骨架中引入低空间位阻的环丁烷基团,其中苄氧环丁酮-二氧杂环丁烷(MPCO)因其最低空间位阻表现出最优异的余辉特性。实验结果表明,MPCO的相对化学激发速率较金刚烷-二氧杂环丁烷提高了35.7倍,余辉强度增加了59倍,总余辉发射量提升了三个数量级。这一突破使得同等浓度下,MPCO基纳米系统所产生的¹O₂数量比游离维替泊芬高近五倍。
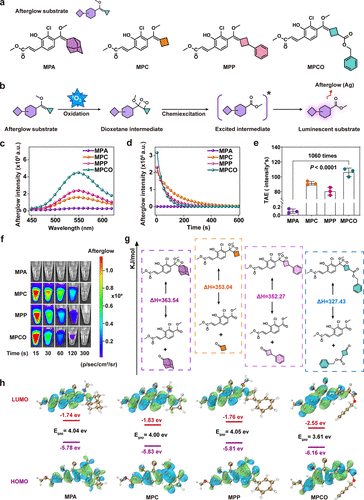
在CNV小鼠模型中,该纳米系统的循环治疗使病变面积减少64.9%,显著优于游离维替泊芬的39.3%减少率。此外,由于余辉激活不依赖于激光照射,该策略有效降低了眼部组织损伤风险,为AMD及其他视网膜疾病的治疗提供了一种安全、有效的新路径。
余辉纳米系统的构建与特性
研究者进一步构建了一种超亮余辉纳米系统(APDT@cRGD NPs),其核心成分包括:
- MPCO(超亮余辉分子)
- BTD540(荧光供体)
- 维替泊芬(Ver)(光敏剂)
- DSPE-PEG-cRGD(靶向修饰,提高CNV区域选择性)
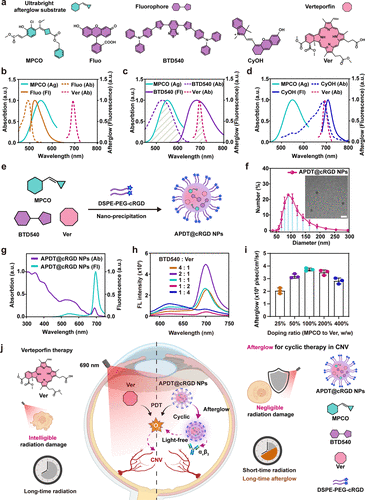
实验数据显示,APDT@cRGD NPs的平均粒径约90±30 nm,采用动态光散射(DLS)及透射电子显微镜(TEM)确认其球形结构。光谱分析结果表明,该纳米系统的吸收峰位于400、540和680 nm,分别对应MPCO、BTD540和维替泊芬的光谱特征,并在700 nm处表现出强余辉信号。这表明,在690 nm激光激活后,该纳米系统可实现高效能量转移,使维替泊芬在无需外部光源的情况下持续产生¹O₂。
余辉纳米系统的治疗机制
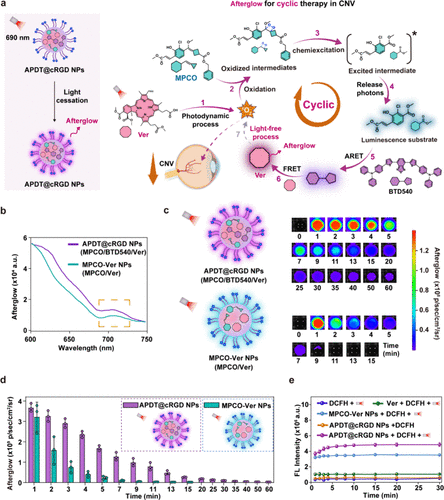
该纳米系统的循环治疗机制包括以下几个关键步骤:
- 维替泊芬受激光照射产生¹O₂
- ¹O₂诱导MPCO氧化并进入化学激发态
- MPCO释放余辉光子,能量经BTD540传递至维替泊芬
- 维替泊芬二次受激,产生更多¹O₂
- 重复循环,实现持续光动力治疗
相比仅含有MPCO和维替泊芬的纳米系统,APDT@cRGD NPs的余辉强度提高约1.65倍,且余辉持续时间延长四倍,能量传递链路的优化大幅提高了整体治疗效果。
体内靶向与治疗效果
实验进一步评估了APDT@cRGD NPs的生物靶向性。利用荧光标记技术发现,该纳米系统具有较强的CNV区域靶向性,相比不含cRGD修饰的纳米系统,其在CNV区域的聚集量提高了1.93倍。此外,在HUVECs(人脐静脉内皮细胞)实验中,该纳米系统在690 nm激光照射下产生的¹O₂量比游离维替泊芬高2.29倍,从而显著增强抗血管增生作用。
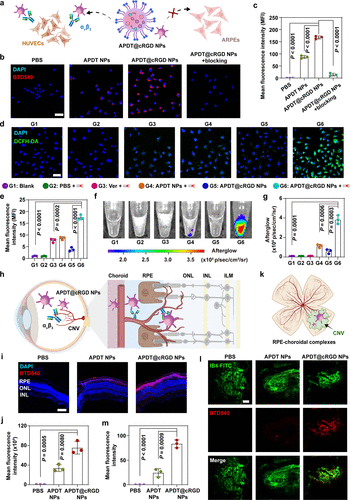
在CNV小鼠模型中,APDT@cRGD NPs成功靶向CNV区域,并在激光照射后持续释放余辉,实现循环光动力治疗,最终病灶面积减少64.9%,远优于游离维替泊芬(39.3%)。
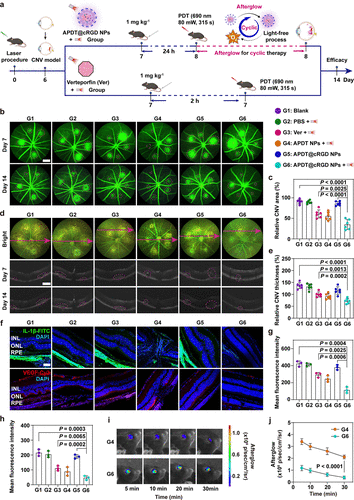
研究意义与未来展望
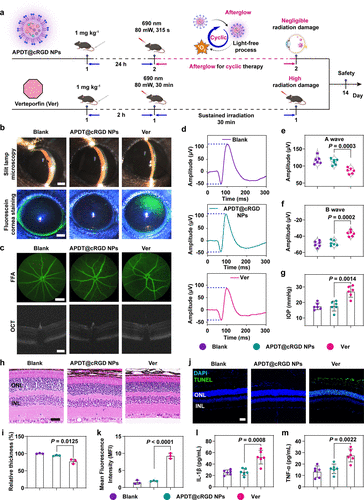
该研究证明了基于低空间位阻环丁烷-二氧杂环丁烷的新型余辉纳米系统在眼科疾病治疗中的巨大潜力。通过优化余辉激发效能,该系统不仅提高了光动力疗法的效率,还成功规避了传统激光照射可能引发的眼组织损伤,为CNV及其他视网膜疾病提供了一种创新性的非激光依赖治疗方案。未来,该策略可扩展应用于其他光动力治疗领域,如抗肿瘤治疗及神经退行性疾病干预,为医学界带来更多突破性进展。
参考文献
Zhang, J.; Shi, H.; Qin, X.; Wang, P.; Ling, Y.; Jin, X.; Cui, M.; Song, B.; Wang, H.; He, Y. Sterically Controlled Cyclobutane-Dioxetane Ultrabright Afterglow Nanosystem for Cyclic Therapy of Choroidal Neovascularization in Mice. J. Am. Chem. Soc. 2025, jacs.5c05187. https://doi.org/10.1021/jacs.5c05187.