【JACS】520纳米绿光激活:双气体疗法显著提升MRSA伤口愈合效率
抗生素耐药性正成为全球医疗难题,尤其是由耐甲氧西林金黄色葡萄球菌(MRSA)引发的慢性伤口感染。近日,《美国化学会志》发表的一项研究提出了一种创新的治疗策略——利用绿光触发一分子同时释放一氧化氮(NO)和一氧化碳(CO),实现抗菌与组织修复的双重功效。
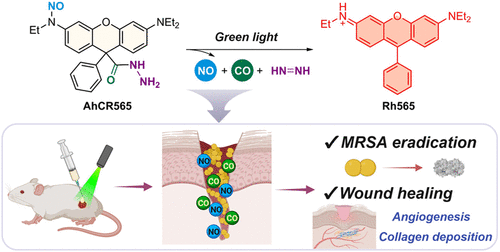
一分子双气体:AhCR565的设计突破
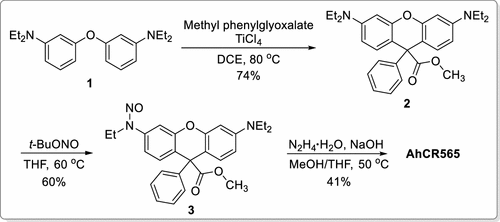
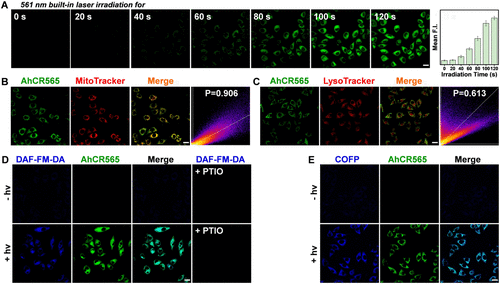
研究团队设计了一种名为AhCR565的分子平台,其核心结构为酰肼封闭的罗丹明染料,结合光敏的N-亚硝胺基团。该分子在520–560纳米绿光照射下,启动级联反应,精准释放NO与CO,同时激活荧光信号,实现气体释放的实时追踪。
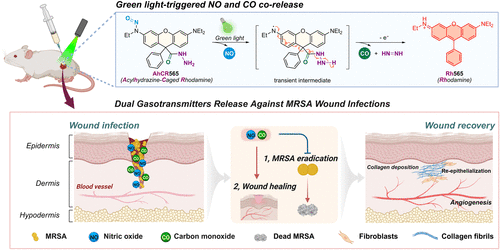
这种“同步释放+自校准”的机制,解决了传统双气体系统释放不同步、定位不精准的问题,为临床应用提供了更安全、可控的治疗手段。
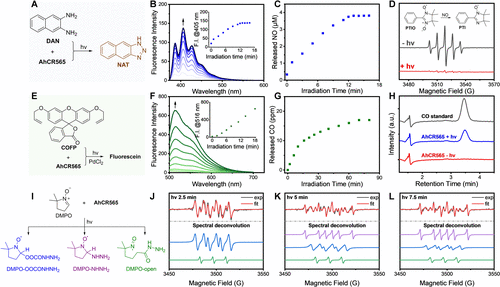
NO与CO:协同抗菌与加速愈合
NO与CO在抗菌方面各具优势:
- NO:抑制细菌呼吸链、破坏生物膜、增强氧化应激;
- CO:干扰细菌酶活性、促进巨噬细胞清除病原体。
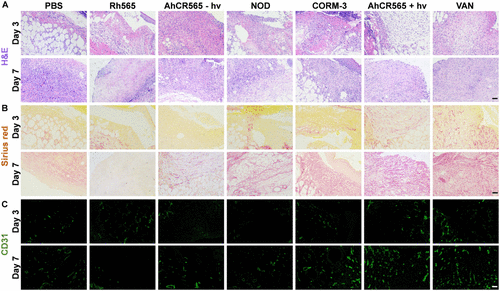
更重要的是,两者还能促进血管扩张、细胞增殖与胶原合成,从而加速伤口修复。AhCR565的协同释放机制在MRSA感染的海洋动物皮肤模型中展现出显著疗效,既清除感染,又促进组织再生。
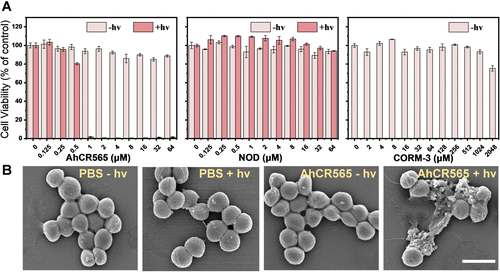
光控疗法:精准、安全、非侵入
相比传统抗生素,光控气体释放具备以下优势:
- 非侵入性:无需注射或手术;
- 时空精准:光照区域限定释放位置;
- 低毒性:避免系统性副作用;
- 抗药性低:气体类抗菌机制不易诱导耐药。
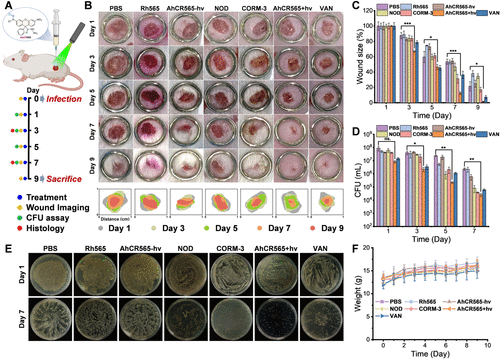
该研究不仅展示了AhCR565在MRSA治疗中的潜力,也为多气体联合疗法开辟了新路径。
展望:从“气体华尔兹”到临床应用
此前研究已在青光眼治疗中验证了级联型NO/CO释放系统的有效性。此次AhCR565的成功应用,标志着该策略在感染性疾病领域的拓展。未来,类似分子平台有望应用于糖尿病溃疡、术后感染等复杂伤口治疗,甚至推动个性化光控药物的发展。
在抗生素逐渐失效的时代,520纳米绿光点亮的不只是分子,更是伤口愈合的新希望。