【Biomaterials】💥突破80%脑炎死亡率!最新纳米药物显著改善蛛网膜下腔出血疗效
近年来,蛛网膜下腔出血(Subarachnoid Hemorrhage,SAH)以其高致残率和高死亡率(超过80%)成为全球脑血管疾病的重要难题之一。近期,《Biomaterials》杂志发表了一项突破性研究,一种新型纳米仿生药物平台——B@COF DT-R,通过精准打击NLRP3炎症小体,有效抑制神经细胞焦亡(pyroptosis),显著改善SAH后的脑部损伤和神经功能恢复,带来治疗策略的新曙光。
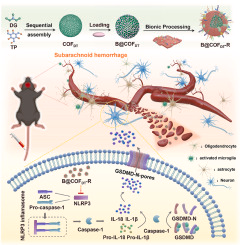
🔬研究亮点一览
- 双重功能材料:使用胍基基团的共价有机框架(COF),兼具药物载体和抗氧化作用。
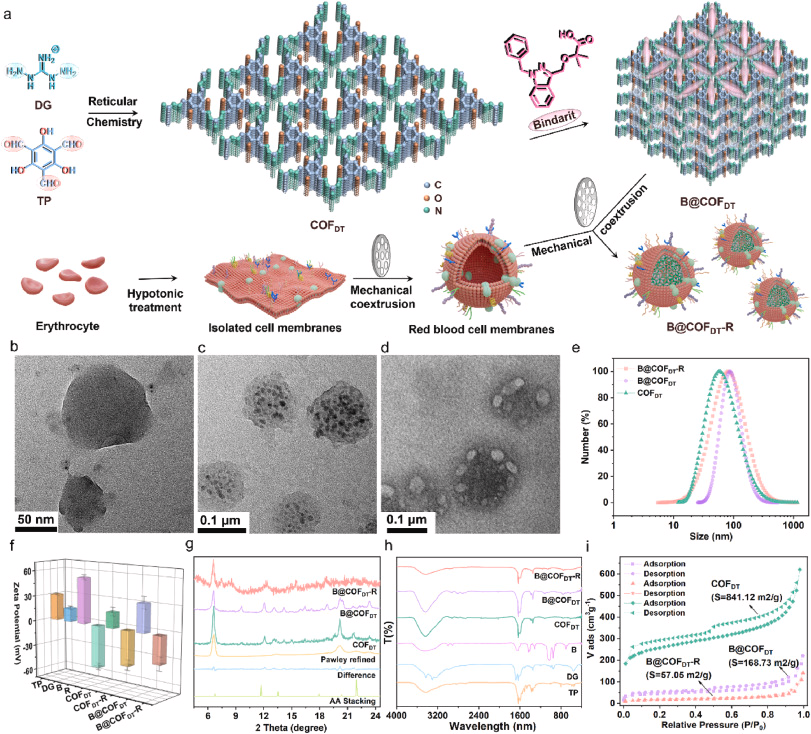
- 智能释药系统:对酸性pH环境响应释放,确保药物精准释放于炎症区域。
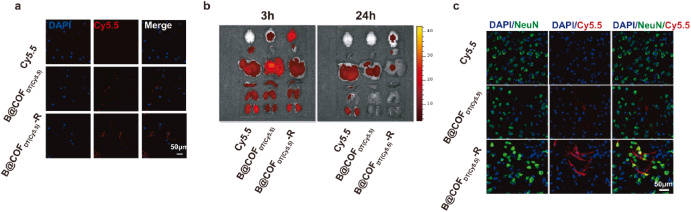
- 高效BBB穿透:COF材料被红细胞膜包覆(B@COF DT-R),增强血脑屏障穿透能力。
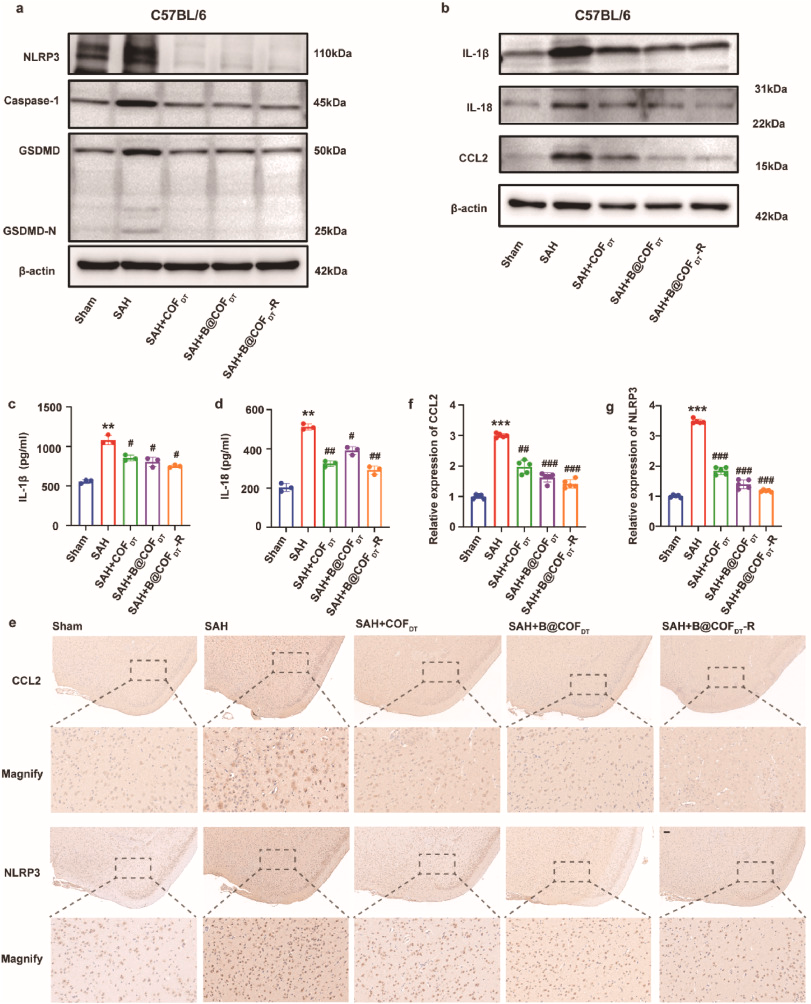
- 靶向炎症通路:有效干预NLRP3/Caspase-1/GSDMD轴,阻断SAH后引发的细胞焦亡过程。
🧠 SAH发病机制中的“焦亡”角色
SAH发作后,体内会出现剧烈的神经炎症反应,主要表现在:
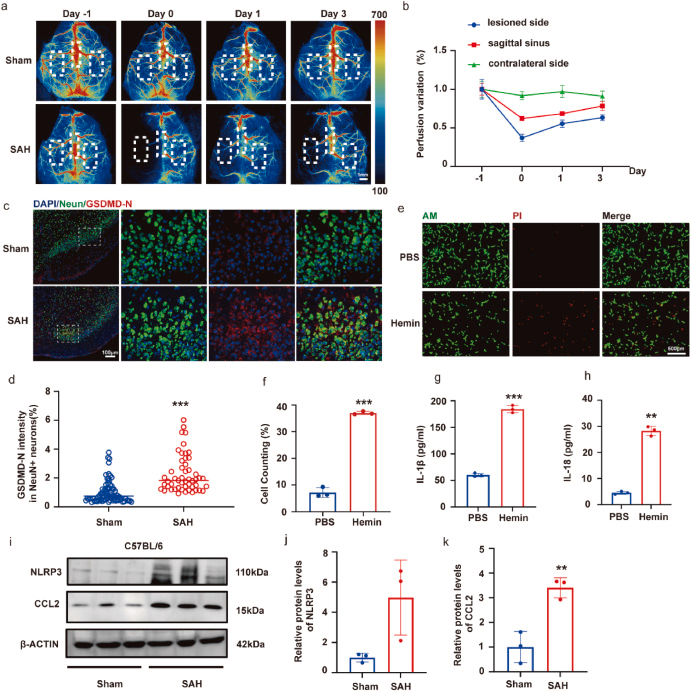
- 血脑屏障受损,水肿和脑灌注下降;
- **焦亡(Pyroptosis)**机制启动,激活NLRP3炎症小体;
- 炎症因子(如IL-1β和IL-18)大量释放,加重神经元损伤。
研究发现,NLRP3和CCL2蛋白在SAH后显著升高,提示它们在炎症反应中居核心地位。
💊 B@COF DT-R 的设计与治疗机制
B@COF DT-R的设计关键如下:
- 载药策略:以COF为框架,装载抗炎药物Bindarit;
- 仿生技术:外包裹红细胞膜,提升体内稳定性并避免免疫清除;
- 靶向作用机制:Bindarit作为CCL2抑制剂,能减少NLRP3活化,从而减少焦亡;
- 酸敏释放:在脑部炎症区域(pH约为6.0)时释放率可达66.13%,而正常组织中仅为25.69%,大幅提升疗效的专一性和安全性。
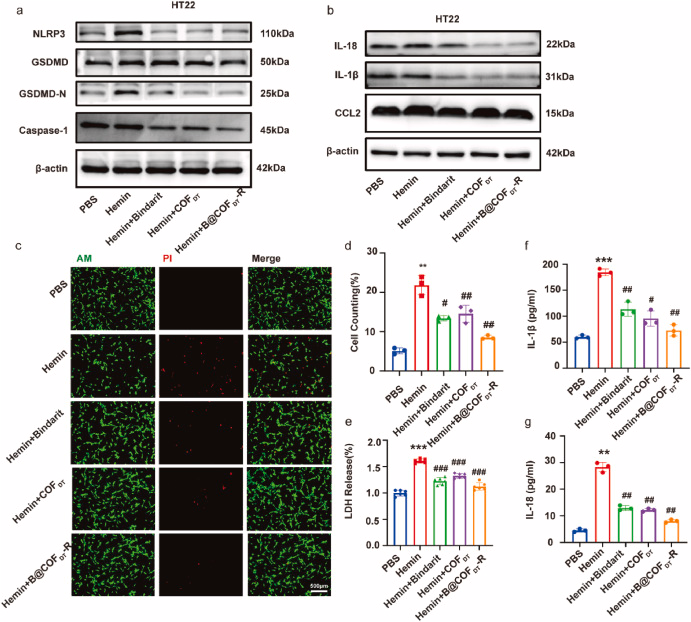
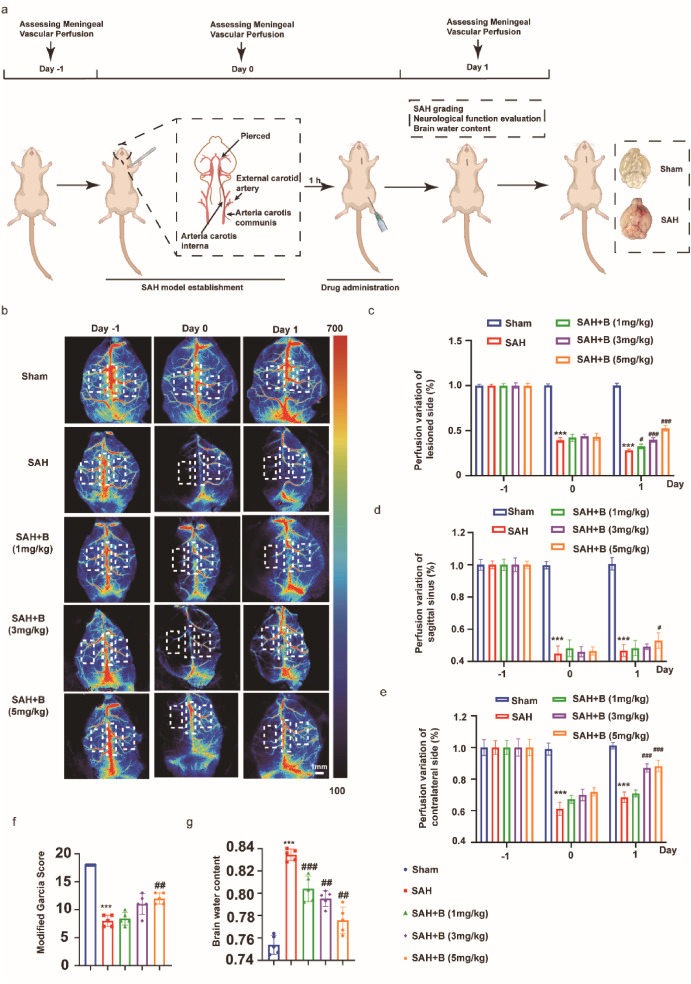
📈实验证实显著疗效
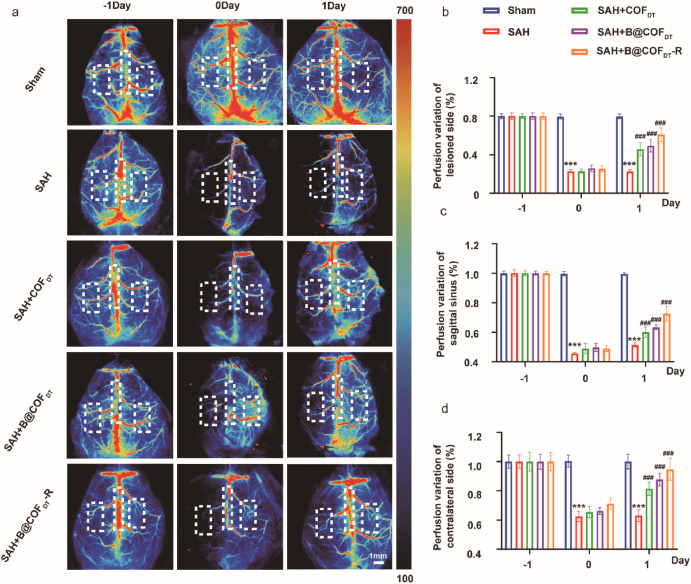
- Bindarit在不同剂量(1, 3, 5 mg/kg)下均能改善SAH模型小鼠的脑灌注和神经行为;
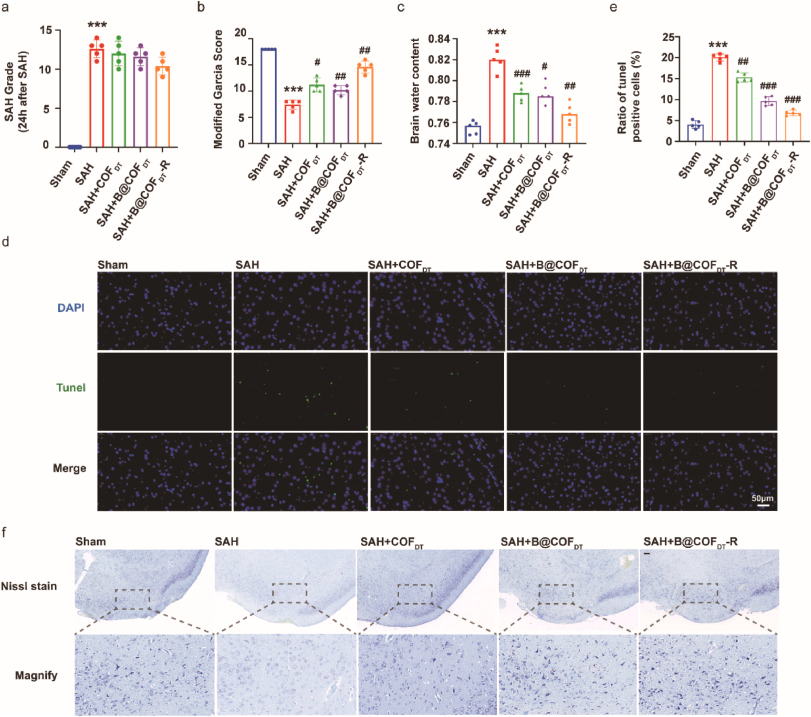
- 脑组织水含量显著降低,提示脑水肿得到缓解;
- 神经功能评分(Garcia评分)显著回升,反映脑部恢复良好。
✨展望与意义
这项研究成功将高分子材料科学与神经药理学结合,为SAH等脑出血疾病的治疗提供了一种新的精准药物递送方案。特别是通过pH响应+红细胞仿生膜的策略,使药物直达病灶,抑制致命性焦亡过程,为攻克SAH带来实质性突破。
新技术、新思路,或许正是在脑出血治疗上赢得“黄金24小时”的关键所在。
参考文献
Yang, L.; Zhang, S.; Luo, Q.; Shu, H.; Xu, W.; Zhu, X.; Hu, P.; Wu, Y.; Shu, L.; Liu, J.; Luo, M.; Tu, W.; Liu, H.; Lv, S.; Wang, L.; Zhu, X.; Zhu, W.; Yan, T. A pH-Responsive Guanidino-Based Covalent Organic Framework Nanodrugs for Enhanced Neuroprotection against Subarachnoid Hemorrhage by Targeting NLRP3 Inflammasome. Biomaterials 2026, 324, 123467. https://doi.org/10.1016/j.biomaterials.2025.123467.