【JACS】光驱动光酶催化的外消旋体拆分研究
简介
该研究设计了一种新型的人工光酶,通过遗传密码扩展技术改造蛋白质CTB10为光驱动催化剂,实现了对热力学上不利的外消旋体拆分反应。研究旨在提供一种超越传统生物催化能力的新方法。
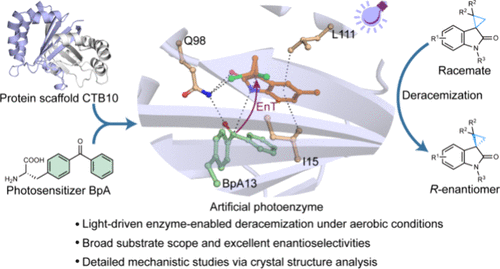
摘要
研究开发了一种以CTB10为骨架的人工光酶,通过光驱动实现了环丙烷外消旋体的高效拆分。使用定向进化优化酶的结构,获得了较高的产率与对映选择性,且对广泛的底物具有适应性。此外,酶-底物复合物的晶体结构揭示了催化反应的关键机制。
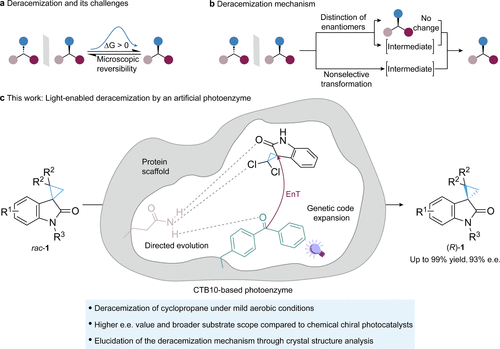
研究结果与讨论
- CTB10光酶构建与优化
基于其疏水口袋和可调节手性空腔的特性,选择性插入光敏剂BpA,成功设计出初始光酶。
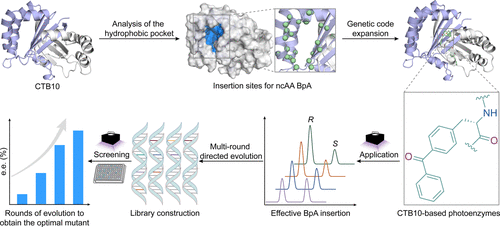
- 光驱动反应机制
首次验证了该光酶通过光照驱动环丙烷的外消旋体拆分,研究了关键位点突变对酶活性及选择性的影响。
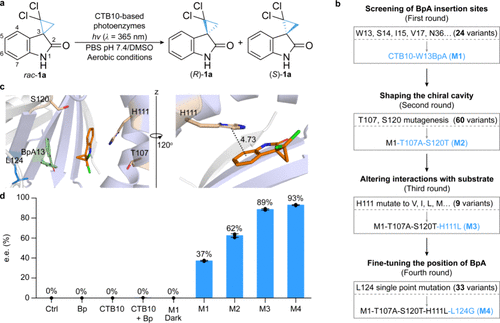
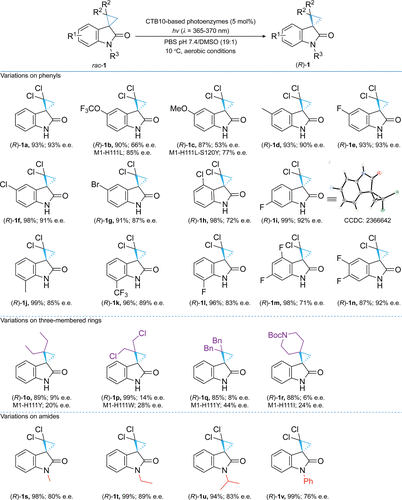
- 底物适应性
该酶在氧化条件下对多种环丙烷衍生物表现出广泛的底物兼容性。
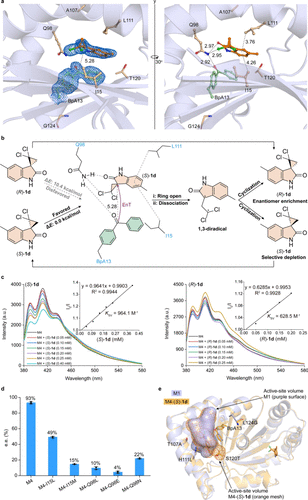
- 光物理特性与酶学分析
通过晶体结构及光谱分析探讨了高选择性背后的能量转移机制,定向进化增强了反应的效率与特异性。
结论
该研究首次实现了光驱动的外消旋体拆分,拓宽了生物催化在不对称合成中的应用潜力。CTB10光酶为复杂催化反应提供了可拓展的蛋白质骨架。
参考文献
Li, M.; Zhang, Y.; Fu, K.; Deng, Z.; Yuan, Z.; Luo, Z.; Rao, Y. Light-Driven Deracemization by a Designed Photoenzyme. J. Am. Chem. Soc. 2025, jacs.4c16521. https://doi.org/10.1021/jacs.4c16521.