【Angew.Chem.】🔬突破传统检测!一文读懂“2种酶+1种DNA酶”打造的超灵敏病毒与癌症诊断平台
在精准医疗和快速诊断日益重要的今天,如何实现对疾病相关蛋白酶的高灵敏度检测,成为科研与临床的共同挑战。近日,《Angewandte Chemie》发表的一项研究提出了一种创新的DNAzyme放大蛋白酶检测平台(DP平台),不仅实现了对新冠病毒(SARS-CoV-2)蛋白酶的准确识别,还成功用于结直肠癌(CRC)组织的分型分析。本文将为您详细解读这一平台的设计原理、性能优势及临床应用潜力。
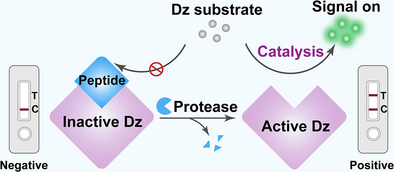
🧬一、DNAzyme放大蛋白酶检测平台的设计原理
传统的蛋白酶检测方法,如ELISA和免疫组化,虽然广泛应用,但存在灵敏度低、操作复杂、无法区分活性酶与前体酶等问题。为解决这些痛点,研究团队设计了一种基于DNAzyme(脱氧核酶)的放大检测系统。
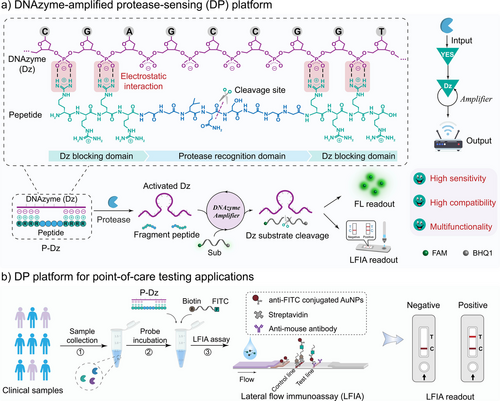
该平台核心由两部分组成:
- 功能性正电荷肽段:含有特定蛋白酶识别序列及富含精氨酸的抑制结构;
- DNAzyme催化元件:带负电荷,可催化核酸底物裂解,产生荧光信号。
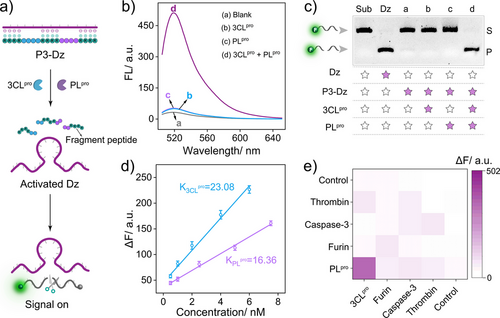
在未加入目标蛋白酶时,肽段与DNAzyme通过静电作用结合,抑制其催化活性。一旦目标蛋白酶(如新冠病毒的3CLpro或PLpro)识别并水解肽段,DNAzyme被释放,恢复活性,进而裂解底物并放大信号,实现高灵敏度检测。
🧪二、单酶激活系统:检测新冠病毒蛋白酶
研究首先构建了单酶激活的DP平台(s-DP),以新冠病毒的3CLpro蛋白酶为模型进行验证。
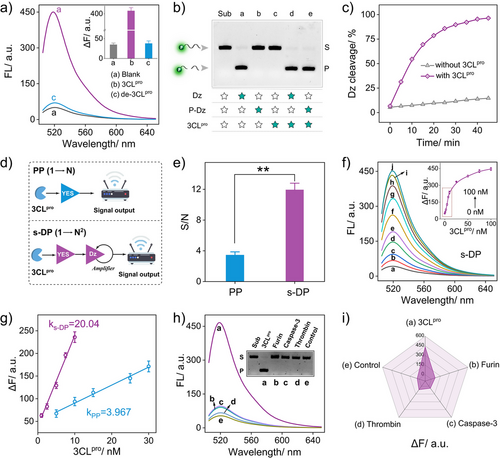
- 在加入3CLpro后,荧光信号显著增强,表明DNAzyme成功激活;
- 与传统非放大平台相比,s-DP的信噪比提升至11.95,是原系统的3.5倍;
- 检测限(LOD)低至0.55 nM,比传统方法提升约11.3倍;
- 对其他蛋白酶(如Furin、Caspase-3、Thrombin)无响应,表现出良好的特异性。
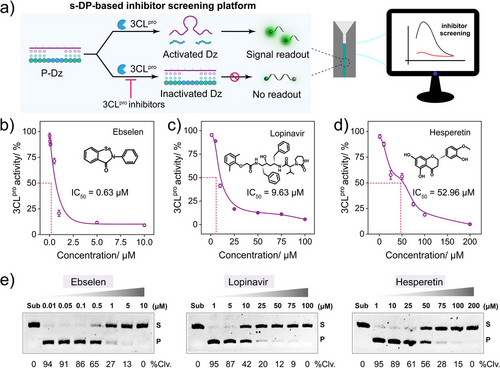
此外,该平台还用于筛选3CLpro抑制剂,成功评估了Ebselen、Lopinavir和Hesperetin三种药物的抑制效果,验证了其在药物筛选中的应用潜力。
🔐三、双酶逻辑门系统:提升检测特异性
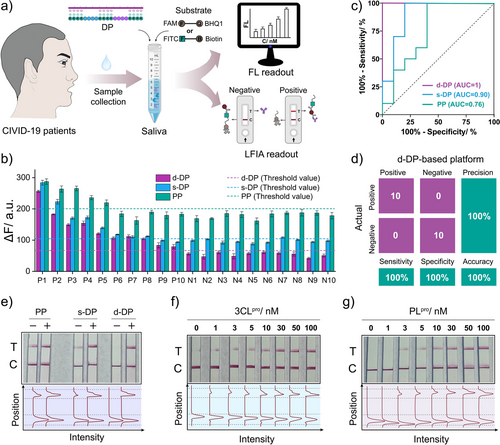
为进一步降低复杂样本中的假阳性风险,研究团队构建了双酶激活的DP平台(d-DP),引入“AND逻辑门”机制:
- 肽段同时包含3CLpro和PLpro两个识别位点;
- 仅在两种酶同时存在时,DNAzyme才被激活,产生荧光信号;
- 在人类唾液和血清中验证,背景信号低,特异性高;
- 检测限分别为0.16 nM(3CLpro)和0.17 nM(PLpro),灵敏度进一步提升。
该系统在20份唾液样本中进行盲测,准确率达100%,ROC曲线AUC值为1.0,远高于传统平台(AUC仅为0.76),显示出卓越的临床诊断性能。
🧫四、平台通用性验证:结直肠癌分型分析
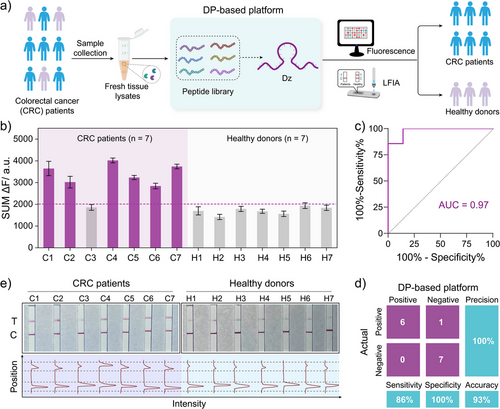
除了病毒检测,该平台还被拓展用于结直肠癌相关蛋白酶的检测:
- 通过转录组和蛋白质组筛选,选定MMP-2、MMP-3、MMP-7、MMP-9和Cathepsin D五种癌症相关蛋白酶;
- 为每种酶设计特异性肽段,构建五种DP传感器;
- 在癌细胞(HT-29)与正常细胞(NCM-460)中检测,癌细胞中酶活性显著升高;
- 多酶联合分析(SUM)提升诊断准确性,PCA分析可清晰区分癌与非癌样本;
- 在14份临床组织样本中检测,准确率达93%,验证了平台的临床实用性。
📦五、POCT应用:与试纸条完美兼容
DP平台的另一个亮点是其与核酸侧流试纸条(LFIA)的高度兼容性:
- DNAzyme裂解产物为核酸片段,可直接用于试纸条检测;
- 与传统肽段平台相比,背景信号更低,信噪比更高;
- 可实现快速、便携的现场检测,适用于资源受限地区。
在LFIA中,d-DP平台可实现对3CLpro和PLpro的浓度响应,检测限分别为1 nM和3 nM,展示了其在POCT场景下的强大潜力。
🧠六、总结与展望
本研究提出的DNAzyme放大蛋白酶检测平台,融合了肽段识别与核酸催化的优势,具备以下显著特点:
- 灵敏度高:检测限远低于传统方法;
- 特异性强:双酶逻辑门有效降低假阳性;
- 通用性强:可定制肽段,适配多种蛋白酶;
- 便携性好:兼容试纸条,适用于POCT;
- 应用广泛:覆盖病毒检测、癌症分型、药物筛选等领域。
未来,该平台有望在更多疾病的早期筛查、个体化治疗监测及公共卫生应急中发挥重要作用,推动精准医疗的进一步发展。